
【题目】常温下向20.00 mL 0.10 mol/L Na2CO3溶液中逐滴加入0.10 mol/L盐酸40.00 mL,所得溶液的pH与加入盐酸体积的关系如表所示:
溶液的pH | 加入盐酸的总体积 |
12 | V(HCl)=0 |
8 | V(HCl)=20.00 mL |
5 | V(HCl)=40.00 mL |
回答下列问题:
(1)20.00 mL 0.10 mol/L Na2CO3溶液中所有阳离子和阴离子的浓度有何关系?______ (用等式表示)。
(2)当V(HCl)=20.00 mL时,溶液呈碱性的原因是________(用离子方程式和必要的文字说明)此时溶液中c(H2CO3)____(填“>”、“<”或“=”)c(CO32—)。
(3)V(HCl)=40.00 mL时,得到H2CO3饱和溶液,且c(H2CO3)=4.0×10-5mol/L。若忽略水的电离及H2CO3的第二级电离,则H2CO3![]() HCO3—+H+的电离常数K1=_____。此时保持其他条件不变,继续加入0.1 mol/L盐酸10.00 mL,K1将_____(填“变大”、“变小”或“不变”)。
HCO3—+H+的电离常数K1=_____。此时保持其他条件不变,继续加入0.1 mol/L盐酸10.00 mL,K1将_____(填“变大”、“变小”或“不变”)。
(4)若向20 mL 0.10 mol/L Na2CO3溶液中加入BaCl2粉末3.94×10-7 g时开始产生沉淀BaCO3,则Ksp(Ba2CO3)= 。
【答案】c(Na+)+c(H+)=2c(CO32—)+c(HCO3—)+c(OH-)Na2CO3+HCl=NaCl+NaHCO3,HCO3—+H2O![]() H2CO3+OH-,HCO3—
H2CO3+OH-,HCO3—![]() H++CO32—,HCCO3—的水解程度大于电离程度2.5×10-6不变9.5×10-9
H++CO32—,HCCO3—的水解程度大于电离程度2.5×10-6不变9.5×10-9
【解析】
(1)根据电荷守恒解答;(2)当V(HCl)=20.00 mL恰好反应生成NaHCO3和NaCl等浓度的混合溶液, 因为溶液中的HCO3-水解程度大于其电离程度,所以溶液呈碱性;(3) V(HCl)=40.00 mL时,得到H2CO3饱和溶液,且c(H2CO3)=4.0×10-5mol/L,此时溶液PH=5,则溶液中c(H+)=10-5mol/L,若忽略水的电离及H2CO3的第二级电离,则溶液中c(HCO3-)和c(H+)近似相等,再根据电离常数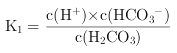 计算;电离平衡常数只受温度影响,温度不变,电离平衡常数不变;(4)计算开始沉淀时C(Ba2+),再根据
计算;电离平衡常数只受温度影响,温度不变,电离平衡常数不变;(4)计算开始沉淀时C(Ba2+),再根据![]() 计算。
计算。
(1)在Na2CO3溶液中,存在平衡:CO![]() +H2O
+H2O![]() HCO
HCO![]() +OH-,HCO
+OH-,HCO![]() +H2O
+H2O![]() H2CO3+OH-,H2O
H2CO3+OH-,H2O![]() H++OH-,根据电荷守恒可得:c(Na+)+c(H+)=c(OH-)+c(HCO
H++OH-,根据电荷守恒可得:c(Na+)+c(H+)=c(OH-)+c(HCO![]() )+2c(CO
)+2c(CO![]() )。答案:c(Na+)+c(H+)=2c(CO
)。答案:c(Na+)+c(H+)=2c(CO![]() )+c(HCO
)+c(HCO![]() )+c(OH-)。
)+c(OH-)。
(2)当加入盐酸20.00 mL时,发生反应:Na2CO3+HCl===NaCl+NaHCO3,HCO![]() +H2O
+H2O![]() H2CO3+OH-,HCO
H2CO3+OH-,HCO![]()
![]() H++CO
H++CO![]() ,因HCO
,因HCO![]() 的水解程度大于电离程度,c(H2CO3)>c(CO
的水解程度大于电离程度,c(H2CO3)>c(CO![]() ),使溶液呈碱性。
),使溶液呈碱性。
(3)H2CO3![]() H++HCO
H++HCO![]() ,K1=
,K1=![]() =
=![]() =
=![]() =2.5×10-6,电离常数只与温度有关,温度不变,K1不变。
=2.5×10-6,电离常数只与温度有关,温度不变,K1不变。
(4)Ksp(BaCO3)=c(CO![]() )·c(Ba2+)=0.10×
)·c(Ba2+)=0.10×![]() ≈9.5×10-9。
≈9.5×10-9。


 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案 激活思维优加课堂系列答案
激活思维优加课堂系列答案科目:高中化学 来源: 题型:
【题目】下列反应最终不能生成三价铁的是( )
A.少量Fe与足量稀HNO3反应B.铁丝在硫蒸气中燃烧
C.Fe(OH)2露置于空气中D.向FeBr2溶液中通入足量Cl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下图所示的实验装置A加热Cu(NO3)2固体,产生红棕色气体,在装置D中收集到无色气体。当反应结束后,试管中残留固体为黑色

(1)装置A发生反应中氧化产物与还原产物的体积比是___________(相同条件下)。
(2)装置B的作用是___________,反应一段时间后,将带火星的木条放入B中,木条复燃,说明该红棕色气体可助燃,原因是______________________。
(3)已知NO2和NaOH溶液反应可生成两种钠盐,装置C中发生的离子方程式为_________。
(4)将反应后试管中的固体加水充分溶解、过滤、洗涤,向滤渣中加入一定量稀硫酸,发现固体全部溶解,得到蓝色溶液,分为两份。
①一份溶液经___________、___________、___________、洗涤得蓝色晶体。
②另一份取20mL溶液,加入过量KI,充分反应后,用0.5000mol·L-1的Na2S2O3溶液来滴定反应产物,终点时消耗Na2S2O3溶液40.00mL,则上述溶液中c(Cu2+)=___________ mol·L-1。(已知2Cu2++4I-=2CuI↓+I2;I2+2S2O32-=21-+S4O62-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Q、X、Y和Z为短周期元素,它们在周期表中的位置如图所示,这4种元素的原子最外层电子数之和为22。下列说法正确的是( )

A.Q的单质具有半导体的性质,Q与Z可形成化合物QZ4
B.Q的最高价氧化物的水化物的酸性比Z的强
C.X氢化物的稳定性比Q强
D.Y的原子半径比X的大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧化钠固体在实验室保存中容易变质。现取一定量的久存氢氧化钠固体样品溶于水,向所得溶液中逐滴加入稀盐酸至过量,生成的CO2(标准状况)与加入的盐酸体积有如图关系

(不考虑CO2在水中的溶解)。试计算:
(1)盐酸的物质的量浓度为________mol/L。
(2)该样品中NaOH与Na2CO3物质的量之比为________。
(3)若该氢氧化钠固体样品溶于水后用于吸收CO2,最多能吸收CO2的体积(标况下)是________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】给定条件下,下列选项中所示的物质间转化均能一步实现的组合是
① FeS2![]() SO2
SO2![]() H2SO4
H2SO4
② SiO2![]() SiCl4
SiCl4![]() Si
Si
③ Al![]() NaAlO2(aq)
NaAlO2(aq)![]() NaAlO2(s)
NaAlO2(s)
④ 1 mol·L1HCl(aq)![]() Cl2
Cl2![]() Ca(ClO)2
Ca(ClO)2
⑤ CuSO4(aq)![]() Cu(OH)2
Cu(OH)2![]() CuO
CuO
⑥ 饱和NaCl溶液![]() NaHCO3
NaHCO3![]() Na2CO3
Na2CO3
A. ①③⑤ B. ①③⑥
C. ②③④ D. ①④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在反应中,X元素的原子将电子转移给Y元素的原子,则下列说法正确的是
①元素X被氧化 ②元素Y被氧化 ③元素X发生还原反应 ④元素Y发生还原反应
A. ①② B. ③④ C. ②③ D. ①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钢铁工业是国家工业的基础,钢铁生锈现象却随处可见,为此每年国家损失大量资金。请回答钢铁腐蚀与防护过程中的有关问题。
(1)钢铁的电化学腐蚀原理如图所示:
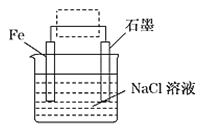
①写出石墨电极的电极反应式____________。
②该装置作简单修改即可成为钢铁电化学防护的装置,请在图虚线框内所示位置作出修改,并用箭头标出导线中电子流动方向____________。
③写出修改后石墨电极的电极反应式________________。
(2)生产中可用盐酸来除铁锈。现将一生锈的铁片放入盐酸中,当铁锈被除尽后,溶液中发生的化合反应的化学方程式_______________________。
(3)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意如图:

①A电极对应的金属是________(写元素名称),B电极的电极反应式是_______。
②若电镀前铁、铜两片金属质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为5.12g,则电镀时电路中通过的电子为______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C、N、S的氧化物常会造成一些环境问题,科研工作者正在研究用各种化学方法来消除这些物质对环境的影响。
(1)已知:2C(s)+O2(g)=2CO(g) ΔH1=-221 kJ·molˉ1
4Al(g)+3O2(g) =2Al2O3(s) ΔH2=-3351 kJ·molˉ1
2Al(g)+N2(g)=2AlN(s) ΔH3=-318 kJ·molˉ1
碳热还原Al2O3合成 AlN 的总热化学方程式是___________________;
(2) “亚硫酸盐法”吸收烟气中的SO2,室温条件下,将烟气通入(NH4)2SO3溶液中,测得溶液pH与含硫组分物质的量分数的变化关系如图所示。

请写出a点时n(HSO3-)∶n(H2SO3)=______,b点时溶液pH=7,则n(NH4+)∶n(HSO3-)=______;
(3)催化氧化法去除NO,一定条件下,用NH3消除NO污染,其反应原理为:4NH3+6NO![]() 5N2+ 6H2O。不同温度条件下,n(NH3):n(NO)的物质的量之比分别为4∶l、3∶l、1∶3时,得到NO脱除率曲线如图所示:
5N2+ 6H2O。不同温度条件下,n(NH3):n(NO)的物质的量之比分别为4∶l、3∶l、1∶3时,得到NO脱除率曲线如图所示:

①请写出N2的电子式________;
② 曲线c对应NH3与NO的物质的量之比是______;
③曲线a中NO的起始浓度为6×10-4mg·m-3,从A点到B点经过0.8s,该时间段内NO的脱除速率为___________mg·m-3·s-1;
(4)间接电化学法可除NO。其原理如上右图所示,写出电解池阴极的电极反应式(阴极室溶液呈酸性)__________________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com