
【题目】下列说法正确的有()个
①将铁屑放入稀HNO3中,证明Fe比H2活泼
②FeCl3腐蚀Cu 制印刷电路板是由于铁比铜的金属性强
③检验溶液中是否含有Fe2+,取少量待检验溶液,向其中加入少量新制氯水,再滴加KSCN 溶液,观察实验现象
④磁性氧化铁溶于稀硝酸的离子方程式为:3Fe2++4H++NO3-==3Fe3++NO↑+3H2O
⑤将NaOH浓溶液滴加到饱和的FeCl3溶液中,制备Fe(OH)3胶体
⑥氢氧化铁与HI溶液反应的离子方程式为: Fe(OH)3+3H+==Fe3++3H2O
⑦铁与水蒸气在高温下的反应产物为Fe2O3 和H2
⑧1mol FeI2与足量氯气反应时转移的电子数为3NA
⑨检验Fe (NO3)2晶体是否氧化变质的方法是将Fe (NO3) 2样品溶于稀H2SO4后,滴加KSCN 溶液,观察溶液是否变红
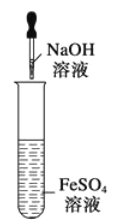
⑩图示装置能较长时间观察到Fe (OH) 2白色沉淀
A. 1 B. 2 C. 3 D. 4
【答案】A
【解析】①将铁屑放入稀HNO3中,硝酸具有强氧化性,生成氮的氧化物而不产生氢气,所以不能证明Fe比H2活泼,故①错误;②FeCl3具有强氧化性,可与Cu发生反应:2Fe3++Cu=2Fe2++Cu2+,与铁、铜的活泼性无关,故②错误; ③加入少量新制氯水,可将亚铁离子氧化成铁离子,所以试剂加入顺序不合理,应先加KSCN溶液无现象、再加氯水,故③错误;④磁性氧化铁为固体,应写成化学式,正确的离子方程式为3Fe3O4+NO3+28H+═9Fe3++14H2O+NO↑,故④错误;⑤将NaOH浓溶液滴加到饱和的FeCl3溶液中反应生成Fe(OH)3沉淀,应向沸水中滴加饱和氯化铁溶液来制备胶体,故⑤错误;⑥氢氧化铁与HI溶液反应生成的Fe3+与I-会发生氧化还原反应,正确的离子方程式为:2Fe(OH)3+6H++2I-=2Fe2++I2+6H2O,故⑥错误;⑦铁与水蒸气在高温下反应的产物是Fe3O4和H2,故⑦错误;⑧ FeI2与足量氯气发生反应的化学方程式为:2FeI2+3Cl2=2FeCl3+2I2,根据方程式可知,1molFeI2消耗1.5molCl2,转移电子3mol,转移的电子数为3NA,故⑧正确;⑨将Fe(NO3)2样品溶于稀H2SO4后,在酸性条件下,NO3-能把Fe2+氧化为Fe3+,滴加KSCN溶液变红,不能说明Fe(NO3)2晶体已经变质,故⑨错误;⑩要较长时间观察到Fe (OH) 2白色沉淀,必须在制取过程中尽可能减少和空气接触,而该装置中生成的Fe(OH)2与空气接触发生反应:4Fe(OH)2+O2+2H2O=4Fe(OH)3,故⑩错误;根据上述分析可知,只有⑧正确,故答案选A。


科目:高中化学 来源: 题型:
【题目】锌是一种应用广泛的金属,目前工业上主要采用“湿法”工艺冶炼锌,某含锌矿的主要成分为ZnS(还含少量FeS等其他成分),以其为原料冶炼锌的工艺流程如图所示: 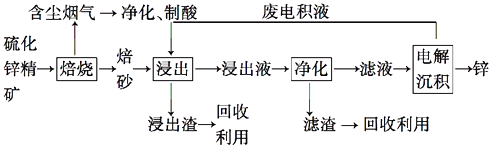
回答下列问题:
(1)硫化锌精矿的焙烧在氧气气氛的沸腾炉中进行,所产生焙砂的主要成分的化学式为 .
(2)焙烧过程中产生的含尘烟气可净化制酸,该酸可用于后续的操作.
(3)浸出液“净化”过程中加入的主要物质为 , 其作用是 .
(4)电解沉积过程中的阴极采用铝板,阳极采用Pb﹣Ag合金惰性电极,阳极逸出的气是 .
(5)改进的锌冶炼工艺,采用了“氧压酸浸”的全湿法流程,既省略了易导致空气污染的焙烧过程,又可获得一种有工业价值的非金属单质.“氧压酸浸”中发生主要反应的离子方程式为 .
(6)我国古代曾采用“火法”工艺冶炼锌,明代宋应星著的《天工开物》中有关于“升炼倭铅”的记载:“炉甘石十斤,装载入一泥罐内,…,然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,…,冷淀,毁罐取出,…,即倭铅也.”该炼锌工艺过程主要反应的化学方程式为 . (注:炉甘石的主要成分为碳酸锌,倭铅是指金属锌)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过溶解、过滤、蒸发等操作,可将下列各组固体物质分离的是()
A. 氯化钾 碳酸钙 B. 氧化铜 二氧化锰
C. 硝酸钠 氢氧化钠 D. 硫酸铜 氢氧化钙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知溶液中,还原性为HSO3->I-,氧化性为IO3->I2>SO42-。在含3 mol NaHSO3的溶液中逐滴加入KIO3溶液,加入KIO3和析出I2的物质的量的关系如图所示,请回答下列问题
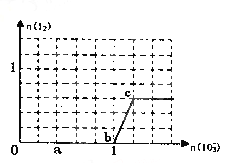
下列问题:
(1)a点处的氧化产物是_________(填化学式,下同),还原产物是_______,a点对应的离子方程式为_____。
(2)当n(I2)达到最大值时,n(IO3-)对应的最小值为____mol,此时反应的离子方程式是_____________。
(3)当溶液中的I-为0.4mol时,加入的KIO3为______mol。
(4)若向100mL 1mol/L的KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】柠檬烯是一种食用香精,其结构简式如图.有关柠檬烯的分析正确的是( ) 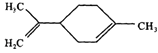
A.柠檬烯的分子式为C10H14
B.它的一氯代物有8种
C.它和丁基苯互为同分异构体
D.一定条件下,它分别可以发生加成、取代、氧化反应,但不能发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:A完全燃烧只生成CO2和H2O,其蒸气密度是相同状况下氢气密度的43倍,分子中H、O原子个数比为3∶1。它与Na或Na2CO3都能反应产生无色气体。
(1)A中含有的官能团的名称是________。
(2)F是A的一种同分异构体,F的核磁共振氢谱图显示分子中有两种不同的氢原子。存在下列转化关系:

写出F的结构简式:____________________。
写出反应①的化学方程式:_______________________________。
写出反应③的化学方程式:__________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com