
【题目】某校化学实验小组设计下图装置制备氯气,图中涉及气体发生、除杂、干燥、收集及尾气处理装置。
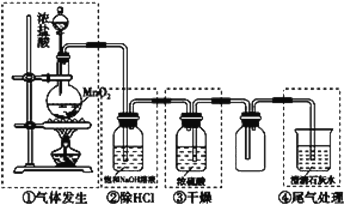
(1)上述装置中,错误的是____________(选填字母)。
A.①②④ B.②③④ C.①③④ D.①②③
(2)写出装置①中发生反应的化学方程式是___________________,将收集到的纯净氯气通入到碘化钾溶液中,再向其中加入四氯化碳振荡后静置,最终的实验现象是_____,发生反应的化学方程式是___________________。
(3)生产氯气的工业称为“氯碱工业”,写出化学方程式______________。
(4)久置氯水的漂白作用会失效,写出发生该反应的化学方程式__________。
(5)工业上用氯气生产漂白粉的化学反应方程式为_____________________。
【答案】B MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O 溶液分层,上层为无色的水层,下层为紫红色的油层 Cl2+2KI=2KCl+I2 2NaCl+2H2O
MnCl2+Cl2↑+2H2O 溶液分层,上层为无色的水层,下层为紫红色的油层 Cl2+2KI=2KCl+I2 2NaCl+2H2O ![]() Cl2↑+ H2↑+2NaOH 2HClO
Cl2↑+ H2↑+2NaOH 2HClO ![]() 2HCl+O2↑ 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
2HCl+O2↑ 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
【解析】
①是实验室制备氯气的装置,用浓盐酸和二氧化锰反应在加热条件下反应,制备得到的氯气中含氯化氢、水蒸气,装置②可以除去氯化氢气体,装置③是干燥氯气的装置,然后利用排空气法收集氯气,最后剩余氯气用碱溶液吸收,防止污染空气,据此分析解答。
(1)题中装置②中氢氧化钠也能除去氯气,应用饱和食盐水除去氯化氢,装置③应该长进短出,装置④中澄清石灰水浓度太低,不能很好的除去氯气,应用氢氧化钠溶液吸收氯气,有错误的装置是②③④,故答案为:B;
(2)装置①中浓盐酸和二氧化锰在加热条件下反应生成氯气,反应的化学方程式为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;将收集到的纯净氯气通入到碘化钾溶液中,发生的反应为Cl2+2KI=2KCl+I2,再向其中加入四氯化碳振荡后静置,碘易溶于四氯化碳,发生萃取,四氯化碳不溶于水,且密度比水大,最终的实验现象为溶液分层,上层为无色的水层,下层为紫红色的油层,故答案为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O;将收集到的纯净氯气通入到碘化钾溶液中,发生的反应为Cl2+2KI=2KCl+I2,再向其中加入四氯化碳振荡后静置,碘易溶于四氯化碳,发生萃取,四氯化碳不溶于水,且密度比水大,最终的实验现象为溶液分层,上层为无色的水层,下层为紫红色的油层,故答案为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;溶液分层,上层为无色的水层,下层为紫红色的油层;Cl2+2KI=2KCl+I2;
MnCl2+Cl2↑+2H2O;溶液分层,上层为无色的水层,下层为紫红色的油层;Cl2+2KI=2KCl+I2;
(3)氯碱工业的原理是电解饱和的食盐水,反应的化学方程式为2NaCl+2H2O ![]() Cl2↑+ H2↑+2NaOH,故答案为:2NaCl+2H2O
Cl2↑+ H2↑+2NaOH,故答案为:2NaCl+2H2O ![]() Cl2↑+ H2↑+2NaOH;
Cl2↑+ H2↑+2NaOH;
(4)氯水含有盐酸和次氯酸,次氯酸容易分解,2HClO ![]() 2HCl+O2↑,因此久置氯水的漂白作用会失效,故答案为:2HClO
2HCl+O2↑,因此久置氯水的漂白作用会失效,故答案为:2HClO ![]() 2HCl+O2↑;
2HCl+O2↑;
(5)工业上用氯气与石灰乳反应生产漂白粉,反应的化学反应方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,故答案为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O。


 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:
【题目】含硫单质的水可治皮肤病,而硫难溶于水,微溶于酒精,易溶于![]() ,要增大硫在水中的分散程度,可将硫先放入溶剂X中,再将所得液体分散在水中,则X可以是
,要增大硫在水中的分散程度,可将硫先放入溶剂X中,再将所得液体分散在水中,则X可以是
A. ![]() B. 氯仿C.
B. 氯仿C. ![]() D. 酒精
D. 酒精
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是某学生自己总结的一些规律,其中正确的是
A.有的无机化学反应不属于化合、分解、置换、复分解中的任何一种反应
B.某物质在固态时能导电,可确认该物质是金属单质
C.一种元素在同一物质中可显示不同价态,但一定是该元素的相邻价态
D.氧化物只可能是氧化产物,不可能是还原产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲测定含少量氯化钠的小苏打固态样品中NaHCO3的质量分数可用以下四种方法。
方法一:
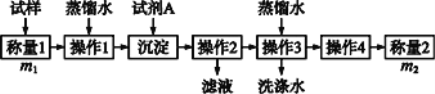
方法二:
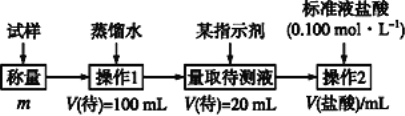
方法三:
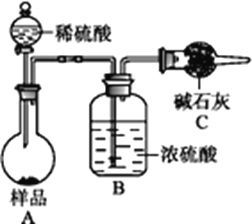
方法四:不使用化学试剂,使用实验室常用仪器。
按要求回答下列问题:
(1)方法一:加入足量的试剂A是___________(填写A的化学式),可将HCO3-转化为沉淀并称重。操作1、2、3、4的名称依次是溶解、____、洗涤和干燥(烘干);
(2)方法二:在操作1中所用到的玻璃仪器中,除了烧杯、玻璃棒、胶头滴管外,还需要用到的是__________,应选择甲基橙作指示剂;
(3)在方法二中计算该样品中NaHCO3的质量分数为_____________;
(4)在方法三中,根据所用的实验装置,除了称量样品质量外,还需测定的实验数据是_____________________;
(5)仔细分析方法三中的实验装置,若由此测得的数据来计算实验结果,则有可能偏高也有可能偏低,偏高的原因可能是_________,偏低的原因可能是__________(均文字简述);
(6)方法四的实验原理是________________(用化学方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某硫酸镁和硫酸铝的混合溶液中,c(Mg2+ )=2 mol·L-1,c(SO42-)=6.5 mol·L-1,若将200 mL此混合液中的Mg2+和Al3+分离,至少应加入1.6 mol·L-1氢氧化钠溶液的体积是
A.0.5 L B.1.625 LC.1.8 LD.2 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有2.8gFe全部溶于一定浓度、200ml的HNO3溶液中,得到标准状况下的气体1.12L,测得反应后溶液的pH为1.若反应前后溶液体积变化忽略不计,则下列有关判断不正确的是
A. 反应后溶液中c(NO3-)=0.85mol/L
B. 反应后的溶液最多还能溶解1.4gFe
C. 反应后溶液中铁元素可能以Fe3+形式存在
D. 1.12L气体只能是NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学实验室使用的浓盐酸的溶质的质量分数通常为36.5%,密度为1.25g/mL。
(1)该盐酸的物质的量浓度为__________mol/L。
(2)现有一种0.2mol/L的稀盐酸的含义是_________(选填字母)。
A.1L水中含有0.2mol HCl
B.1L溶液中含有0.1mol H+
C.将7.1gHCl溶于1L水所配成的溶液
D.从100mL该溶液中取出10mL,剩余溶液的物质的量浓度仍为0.2mol/L
(3)用上述实验室的浓盐酸来配制500mL1 mol/L的稀盐酸,请在下列操作步骤中填写有关的空格:
①用量筒量取________mL的浓盐酸;(精确到小数点后一位)
②向盛有少量蒸馏水的烧杯中,沿_________慢慢注入浓盐酸;
③将已冷却至室温的盐酸溶液沿玻璃棒注入________mL的容量瓶中;
④用少量蒸馏水洗涤烧杯2~3次,并将洗涤液也全部转移到容量瓶中;
⑤继续向容量瓶中加蒸馏水,直至液面接近刻度线1~2cm处;
⑥改用___________________逐滴加蒸馏水,使溶液凹液面恰好与刻度线相切;
⑦盖好容量瓶塞,反复颠倒,摇匀;
⑧将配好的稀硫酸倒入试剂瓶中,贴好标签。
(4)由于操作不当,会引起实验误差。下列情况对所配制的盐酸溶液的物质的量浓度有何影响?(用“偏高”、“偏低”、“无影响”填空)
①容量瓶用蒸馏水洗涤后残留有少量的水_____________;
②定容时,某同学观察液面的情况如图所示_____________;
③摇匀后,发现溶液的液面低于刻度线,又加水至刻度线____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用16mol/L 浓硫酸配制100mL 2.0mol/L 稀硫酸的实验步骤如下:①计算所用浓硫酸的体积 ②量取一定体积的浓硫酸 ③溶解 ④转移、洗涤 ⑤定容 ⑥摇匀。回答下列问题:
(1)该实验所需的玻璃仪器:______、玻璃棒、烧杯、胶头滴管、量筒。
(2)所需浓硫酸的体积是_____,量取浓硫酸所用的量筒的规格是____(规格从下列中选用A.10mL B.20mL C.50mL D.100mL)。
(3)第⑤步定容的具体实验操作是_______。
(4)下列情况对所配制的稀硫酸浓度有何影响?(用偏大、偏小、无影响填写)
A.容量瓶用蒸馏水洗涤后残留有少量的水____。
B.转移溶液前未冷却至室温_____。
C.定容时仰视溶液的凹液面______。
D. 向容量瓶中转移溶液时,不慎有少量溶液洒在容量瓶外面____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于难溶电解质溶解平衡的说法正确的是
A. 可直接根据 Ksp 的数值大小比较难溶电解质在水中的溶解度大小
B. 在 AgCl 的饱和溶液中,加入蒸馏水, Ksp(AgCl)不变
C. 难溶电解质的溶解平衡过程是可逆的,且在平衡状态时 v溶解=v沉淀=0
D. 25℃时, Ksp(AgCl)>Ksp(AgI),向 AgCl 的饱和溶液中加入少量 KI 固体,一定有黄色沉
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com