
����Ŀ������ȼ��ʱ�������仯��ͼ���й�˵����ȷ���ǣ� ��
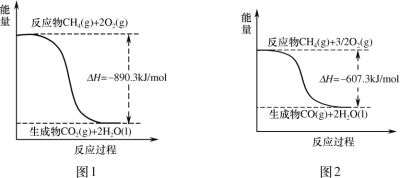
A.ͼ1�з�ӦΪ��CH4(g)+2O2(g)=CO2(g)+2H2O(l) H=+890.3kJ/mol
B.ͼ2�з�ӦΪ��CH4(g)+![]() O2(g)=CO(g)+2H2O(g) H=��607.3kJ/mol
O2(g)=CO(g)+2H2O(g) H=��607.3kJ/mol
C.��ͼ�����Ƶã�CO(g)+![]() O2(g)=CO2(g) H=��283kJ/mol
O2(g)=CO2(g) H=��283kJ/mol
D.��ͼ������֪�������ʵ�����CO2��CO��CO2���е�������
���𰸡�C
��������
A������ͼ���������Ӧ�����������������������������ͼ1�з�ӦΪ��CH4(g)+2O2(g)=CO2(g)+2H2O(l) H=-890.3kJ/mol��A����
B������ͼ�������������ˮ��״̬��Һ̬����ͼ2�з�ӦΪ��CH4(g)+![]() O2(g)=CO(g)+2H2O(l) H=��607.3kJ/mol��B����
O2(g)=CO(g)+2H2O(l) H=��607.3kJ/mol��B����
C��CO(g)+![]() O2(g)=CO2(g) ���ʱ�ɸ���CH4(g)+2O2(g)=CO2(g)+2H2O(l) H=-890.3kJ/mol�ͷ�ӦH=��283kJ/mol��CH4(g)+
O2(g)=CO2(g) ���ʱ�ɸ���CH4(g)+2O2(g)=CO2(g)+2H2O(l) H=-890.3kJ/mol�ͷ�ӦH=��283kJ/mol��CH4(g)+![]() O2(g)=CO(g)+2H2O(l) H=��607.3kJ/mol����ʱ�H=��283kJ/mol��C��ȷ��
O2(g)=CO(g)+2H2O(l) H=��607.3kJ/mol����ʱ�H=��283kJ/mol��C��ȷ��
D��CO(g)+![]() O2(g)=CO2(g) H=��283kJ/mol���÷�Ӧ���ȣ���Ӧ�������������������������������Ե����ʵ�����CO2��CO��CO���е������ߣ�D����
O2(g)=CO2(g) H=��283kJ/mol���÷�Ӧ���ȣ���Ӧ�������������������������������Ե����ʵ�����CO2��CO��CO���е������ߣ�D����
��ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ú�����ܼ�����(2���һ�����)���������������壬H2SO4 �������ᴦ����ͭ��ˮ�� ������������ͬʱ��Cu2����ȡ��[��ȡ�ʣ�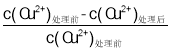 ��100�� ]���ʼ Cu2��Ũ�ȹ�ϵ��ͼ 1 ��ʾ��������������ͬʱ������ǰ��ʼ Cu2��Ũ��Ϊ 200 mg��L��1��Cu2����ȡ�����ˮ pH �Ĺ�ϵ��ͼ 2 ��ʾ������˵���������
��100�� ]���ʼ Cu2��Ũ�ȹ�ϵ��ͼ 1 ��ʾ��������������ͬʱ������ǰ��ʼ Cu2��Ũ��Ϊ 200 mg��L��1��Cu2����ȡ�����ˮ pH �Ĺ�ϵ��ͼ 2 ��ʾ������˵���������
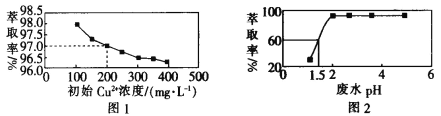
A.����ͼ 1 ��֪����ˮ�г�ʼ Cu2��Ũ��Խ��Cu2������ȡЧ��Խ��
B.����ͼ 2 ��֪����ˮ��ʼ pH��2 ʱ��ȥ�� Cu2����Ч���Ϻ�
C.����ͼ 1 ��֪��Cu2����ʼŨ��Ϊ 200 mg��L��1 ʱ��Cu2������ȡ��Ϊ 97.0��
D.����ͼ 2 ��֪����ȡ 800 mL ��ʼ Cu2��Ũ��Ϊ 200 mg��L��1 �ķ�ˮ���� pH��1.5 ʱ������ˮ��������ķ�ˮ��ʣ�� Cu2�������ʵ���Ϊ 1.5��10��3mol(�����������)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����л����˵��������ǣ�������
A.ʯ�ͺ���Ȼ������Ҫ�ɷֶ���̼�⻯����
B.�����������������������������Һ��Ӧ
C.���ࡢ��֬�͵����ʶ���������Ҫ��Ӫ������
D.һ�������£����ܷ����ӳɷ�Ӧ��ȡ����Ӧ��������Ӧ���Ӿ۷�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£����и���������ָ����Һ���ܴ���������ǣ� ��
A.��ɫ������Һ�У�Fe3+��NH4+��I-��CO32-
B.0.1molL-1KNO3��Һ�У�Na+��Fe2+��Cl-��SO42-
C.ʹ��̪������Һ�У�Na+��Mg2+��SO32-��NH4+
D.![]() =1��10-12����Һ��K+��Na+��CO32-��HCO3-
=1��10-12����Һ��K+��Na+��CO32-��HCO3-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������±��еļ��ܣ��ɼ���������ȼ����Ϊ�� ��
![]()
A.379kJ/molB.808kJ/molC.1656kJ/molD.2532kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ͭ�ڳ������ܱ�ϡ�����ܽ�,�䷴Ӧ�Ļ�ѧ����ʽ����:3Cu+8HNO3(ϡ) =3Cu(NO3)2+2NO��+4H2O
(1)��������_______,����������Ӧ��������__________,��������Ԫ����_______,��ԭ������___________.
(2)����1molNOת�Ƶ���_____mol
(3)�õ����ŷ���ʾ��Ӧ���ӵ�ʧ�ķ������Ŀ:_____________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E���ֻ�����,�����г���Ԫ�أ����ǵ�ת����ϵ��ͼ��ʾ,����AΪ������Һ,CΪ���ܵİ�ɫ����,E��������ˮ,��ȡA��Һ����,��ɫ��ӦΪdz��ɫ(����ɫ�ܲ���)��
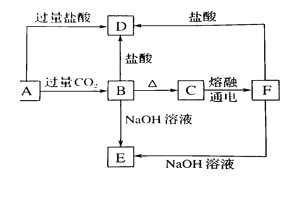
(1)д����ѧʽ;
A______ ,C______ ,D______ ,E______
(2)д�����з�Ӧ�����ӷ���ʽ:
��A��B: _____________________________________________
��B��E: _____________________________________________
��C��E: _____________________________________________
��F��E: _____________________________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ƾ���(Na2SnO33H2O2)��Ⱦ�Ϲ�ҵ����ýȾ�������������ϣ���Ҫ�ɷ���SnO������������Fe��Te��Sb��Pb��As��Ԫ�ص������Ϊԭ�ϣ��Ʊ������ƾ���Ĺ�������ͼ��ͼ��
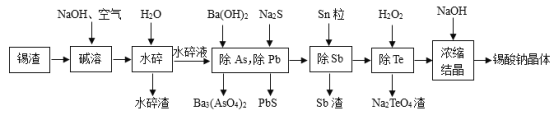
��֪��ˮ��Һ�����ʵ���Ҫ�ɷ�ΪNa2SnO3��Na3AsO4��Na3SbO4��Na2PbO2��Na2TeO3��
(1)��������ʱ��SnO������Ӧ�Ļ�ѧ����ʽΪ___��
(2)��ҵ���Ʊ������ƾ���(Na2SnO33H2O)ʱ���Ὣ��ˮ�������ٴ�ˮϴ����Ŀ����___��
(3) ����Sb��ʱ������Ӧ�����ӷ���ʽΪ___��
(4) ����Te���������������뻹ԭ�������ʵ���֮��Ϊ___���ù����з�Ӧʱ�䡢��Ӧ�¶ȶ�Te���ѳ��ʵ�Ӱ���ϵ��ͼ����70������¶�����Te���ѳ����½���ԭ�������___������Te�������ŷ�Ӧʱ��ͷ�Ӧ�¶ȷֱ�Ϊ___��___��
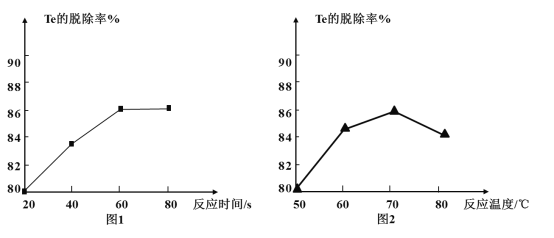
(5)��֪�����Ƶ��ܽ��һ�������¶ȵ����߶����ߣ�������Ũ�����ᾧ��ʱ������NaOH��ԭ����___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ���л������У��е���ͬ���칹�壬�е�û��ͬ���칹�壬����һ��������ͬ���칹��ķ�Ӧ��
A.�����ϩ(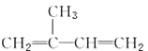 )������ʵ�����Br2�����ӳɷ�Ӧ
)������ʵ�����Br2�����ӳɷ�Ӧ
B.2���ȶ�����NaOH�Ҵ���Һ���ȷ�����ȥHCl���ӵķ�Ӧ
C.�ױ���һ�������·���������Ӧ����һ�����ױ��ķ�Ӧ
D.������Na2CO3��Һ��Ӧ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com