
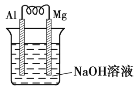
【题目】镁条、铝条平行插入一定浓度的NaOH溶液中,用导线连接构成原电池(如图所示),此电池工作时,下列叙述中正确的是( )
A.Mg比Al活泼,Mg失去电子被氧化成Mg2+
B.负极反应为Al-3e-+4OH-=![]() +2H2O
+2H2O
C.外电路中电子由Mg电极经导线流向Al电极
D.Al是正极,开始工作时溶液中会有白色沉淀析出
【答案】B
【解析】
该原电池中,铝易失电子作负极,电极反应式为Al+4OH--3e-=AlO2-+2H2O,正极上水得电子发生还原反应,电极反应式为2H2O+2e-=H2↑+2OH-,电池反应式为2Al+2OH-+2H2O=3H2↑+2AlO2-,据此分析解答。
A.在NaOH溶液中,铝能与NaOH溶液发生氧化还原反应,在该反应中,铝失电子作原电池的负极,而镁和氢氧化钠溶液不能发生氧化还原反应,故A错误;
B.Al为负极,负极电极反应式为Al+4OH--3e-=AlO2-+2H2O,故B正确;
C.原电池工作时,外电路中电子的流向是由负极Al向正极Mg移动,故C错误;
D.铝作负极,开始工作时氢氧化钠过量,电极反应为Al+4OH--3e-=AlO2-+2H2O,所以没有白色沉淀生成,故D错误;
故答案为B。


科目:高中化学 来源: 题型:
【题目】某小组为研究电化学原理,设计如图装置.下列叙述不正确的是

A. a和b不连接时,铁片上会有金属铜析出
B. a和b用导线连接时,铜片上发生的反应为:Cu2++2e-=Cu
C. 无论a和b是否连接,铁片均会溶解
D. a和b用导线连接后,Fe片上发生还原反应,溶液中的Cu2+向铜电极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组测定不同温度下、不同初始浓度的某溶液中R的水解速率,c(R)随时间的变化曲线如图。下列说法不正确的是

A.在0-6min之间,25℃时R的水解速率为0.05 mol·L—1·min—1
B.在0-24min之间,曲线3对应水解速率最小
C.由曲线1可以得出结论:其它条件不变,水解速率随浓度增大而增大
D.由曲线2、3可以得出结论:其它条件不变,水解速率随温度升高而增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等物质的量的铁和铜的混合物24g与600mL稀硝酸恰好完全反应,生成NO6.72L(标准状况)。向反应后的溶液中加入1molL-1NaOH溶液使金属离子恰好沉淀。下列有关说法错误的是( )
A.混合物溶解后的溶液中c(Fe3+):c(Fe2+)=1:1
B.稀硝酸的物质的量浓度度是2molL-1
C.需要加入NaOH溶液1000mL
D.最后所得沉淀在空气中充分加热可得固体32g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿魏酸在食品、医药等方面有着广泛用途。一种合成阿魏酸的反应可表示为:
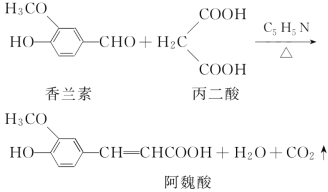
则下列说法不正确的是( )
A.丙二酸与乙二酸互为同系物
B.由题中信息可知阿魏酸甲酯的分子式为C11H12O4
C.香兰素、阿魏酸都是芳香族化合物
D.可用溴水检测上述反应中香兰素是否完全转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语对事实的表述正确的是
A.常温下,0.1mol·L-1 氨水的 pH=11: NH3·H2O NH4+ + OH-
B.Mg 和 Cl 形成离子键的过程: 
C.电解 CuCl2 溶液: CuCl2 == Cu2+ + 2Cl-
D.乙酸与乙醇发生酯化反应: CH3COOH + C2H518OH![]() CH3COOC2H5 + H218O
CH3COOC2H5 + H218O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃料电池是利用燃料(如H2、CO、CH4、CH3OH、NH3等)与O2反应从而将化学能转化为电能的装置。
(1)燃料电池(NaOH作电解质溶液)的正极电极反应式为__。
瑞典ASES公司设计的曾用于驱动潜艇的液氨液氧燃料电池示意图如图所示,有关说法不正确的是(________)

A.电池工作时,Na+向正极移动
B.电子由电2经外电路流向电极1
C.电极总应为4NH3+3O2=2N2+6H2O
D.电极2发生的电极反应为O2+4H++4e-=2H2O
(2)葡萄糖为燃料的微生物燃料电池结构示意图如图所示。

葡萄糖作为微生物燃料电池的___(填“正”或“负”)极。
微生物燃料电池___(填“能”或“不能”在高温下工作。
(3)CO无色无味有毒,世界各国每年均有不少人因CO中毒而失去生命。一种CO分析仪的工作原理所示,该装置中电解质为氧化钇一氧化钠,其中O2可以在固体介质NASICON中自由移动。传感器中通过电极反应测定尾气中CO的含量越高,请回答:

电极反应式为___。
(4)PbO溶解在HCl和NaCl的混合溶液中,得到含电解质Na2PbCl4溶液,电解Na2PbCl4溶液生成Pb的装置如图所示。

电解时阴的电极反应式___。
其过程中通过阳离子交换膜的离子主要为___。
过程中,Na2 PbCl4电解液浓度不断减小,为了恢复其浓度向阴极室加___(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种有机物有如下转化关系(部分产物和转化条件已略去);

已知烯烃A可以作为水果的催熟剂,D是食醋的成分之一。
请回答下列问题:
(1)写出B物质中官能团的名称_________。
(2)A在一定条件下与水反应能得到物质B,则该化学反应的反应类型是_____________。
(3)写出在浓硫酸作用下B与D反应的化学方程式_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com