
【题目】在同温同压下,分别用如图所示的气体吹出体积相等的甲、乙两个气球,则这两个气球中气体的有关量之比(甲:乙)正确的是

A.质量之比为![]() B.原子总数之比为
B.原子总数之比为![]()
C.分子总数之比为![]() D.碳原子数之比为
D.碳原子数之比为![]()
【答案】B
【解析】
同温同压下,体积相等的气体具有相同的分子数,即物质的量相同,乙烯和一氧化碳的摩尔质量均为28g/mol,据此根据公式进行解答。
同温同压下,体积相等的气体具有相同的分子数,即物质的量相同,乙烯和一氧化碳的摩尔质量均为28g/mol;
A.根据m=nM得乙烯和一氧化碳质量相同,质量比为1:1,故A错误;
B.原子物质的量等于分子物质的量乘以一个分子中的原子数,所以二者原子总数之比为(1![]() 6):(1
6):(1![]() 2)=3:1,故B正确;
2)=3:1,故B正确;
C.分子数之比等于物质的量之比,为1:1,故C错误;
D.碳原子数之比等于分子物质的量乘以一个分子中的碳原子数,所以二者碳原子数之比为(1![]() 2):1=2:1,故D错误;
2):1=2:1,故D错误;
故答案选B。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】电化学腐蚀及防护的研究装置如图所示,下列有关说法不正确的是

A.若a、b用导线相连,石墨电极上有气泡产生
B.若a、b不用导线相连,c处比d处更易产生铁锈
C.若a、b用导线相连,铁片主要发生吸氧腐蚀
D.若a、b分别连接电源的正、负极,将加快铁片的腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煅烧黄铁矿(主要成分为FeS2)所得的矿渣中含Fe2O3、SiO2、Al2O3、MgO等.用该矿渣可制备铁红(Fe2O3).完成下列填空:
(1)煅烧黄铁矿的化学方程式____,反应过程中被氧化的元素____.
(2)矿渣中属于两性氧化物的是___,写出Fe2O3与稀硫酸反应的离子方程式__.
(3)Al(OH)3的碱性比Mg(OH)2的碱性___(选填“强”或“弱”);铝原子最外层电子排布式为____.
(4)SiO2的熔点___ Fe2O3的熔点(填“大于”或“小于”),原因是__.
(5)已知矿渣质量为w kg,若铁红制备过程中,铁元素损耗25%,最终得到铁红的质量为m kg,则原来矿渣中铁元素质量分数为______(用表达式表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纯碱(Na2CO3)在生产生活中具有广泛的用途.如图1是实验室模拟制碱原理制取Na2CO3的流程图.
完成下列填空:
已知:粗盐中含有Ca2+、Mg2+、SO42﹣等杂质离子.
(1)精制除杂的步骤顺序是____→___→____→____→____ (填字母编号).
a 粗盐溶解 b 加入盐酸调pH c 加入Ba(OH)2溶液 d 加入Na2CO3溶液 e 过滤
(2)向饱和食盐水中先通入NH3,后通入CO2,理由是______.在滤液a中通入NH3和加入精盐的目的是______.
(3)请在图1流程图中添加两条物料循环的路线.____
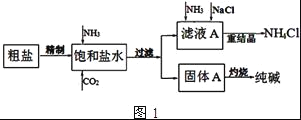
(4)图2装置中常用于实验室制备CO2的是__(填字母编号);用c装置制备NH3,烧瓶内可加入的试剂是___(填试剂名称).
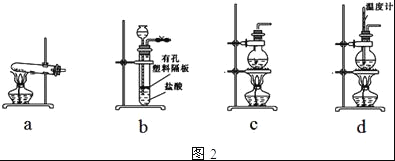
(5)一种天然碱晶体成分是aNa2CO3bNa2SO4cH2O,利用下列提供的试剂,设计测定Na2CO3质量分数的实验方案.请把实验方案补充完整:
供选择的试剂:稀H2SO4、BaCl2溶液、稀氨水、碱石灰、Ba(OH)2溶液
①______.
②______.
③______.
④计算天然碱晶体中含Na2CO3的质量分数.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】坚决反对运动员服用兴奋剂,是我国支持“人文奥运”的重要体现。某种兴奋剂的结构简式如图所示,有关该物质及其溶液的说法错误的是
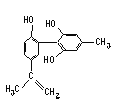
A.该分子中所有氢原子不可能在同一个平面上
B.1 mol该物质与H2反应时,最多消耗7 molH2
C.加入FeCl3溶液呈紫色,因为该物质属于酚类物质
D.滴入酸性高锰酸钾溶液,紫色褪去,可证明其结构中存在碳碳双键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】蒽(![]() )与苯炔(
)与苯炔(![]() )反应生成化合物X(X结构中三个苯环呈立体对称结构),如下图:
)反应生成化合物X(X结构中三个苯环呈立体对称结构),如下图:
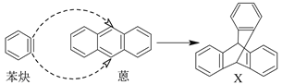
(1)蒽与X都属于_________________(填编号)。
a.环烃 b.不饱和烃 c.烷烃 d.芳香烃
(2)苯炔的分子式为_____________,苯炔不具有的性质______________(填编号)。
a.能溶于水 b.能发生氧化反应 c.能发生加成反应 d.常温常压下为气体
(3)X的一个氢原子被甲基取代的所有同分异构体数为__________(填编号)。
a.2种 b.3种 c.4种 d.5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A.![]() 和CO的混合物共
和CO的混合物共![]() ,其中碳原子的数目为NA
,其中碳原子的数目为NA
B.![]() 重水
重水![]() 分子中含有的中子数为0.8NA
分子中含有的中子数为0.8NA
C.![]() 放入过量的98%浓
放入过量的98%浓![]() 中,转移电子数为3NA
中,转移电子数为3NA
D.![]()
![]() 的NaCl溶液中微粒数大于0.5NA
的NaCl溶液中微粒数大于0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学通过实验研究FeCl3溶液与Cu粉发生的氧化还原反应。实验记录如下:
序号 | I | II | III |
实验 步骤 |
充分振荡,加2mL蒸馏水 |
充分振荡,加入2mL蒸馏水 |
充分振荡,加入2mL蒸馏水 |
实验 现象 | 铜粉消失,溶液黄色变浅,加入蒸馏水后无明显现象 | 铜粉有剩余,溶液黄色褪去,加入蒸馏水后生成白色沉淀 | 铜粉有剩余,溶液黄色褪去,变成蓝色,加入蒸馏水后无白色沉淀 |
下列说法不正确的是( )
A.实验I、II、III中均发生了反应2Fe3++Cu===2Fe2++Cu2+
B.对比实验I、II、III说明白色沉淀的产生可能与铜粉的量及溶液的阴离子种类有关
C.实验II、III中加入蒸馏水后c(Cu2+)相同
D.向实验III反应后的溶液中加入饱和NaCl溶液可能出现白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自来水生产过程中,可用氯气等物质作消毒剂,明矾等物质作絮凝剂。出厂的自来水中含少量可溶性矿物质。完成下列填空:
(1)自来水中含硫量约70 mg/L,它只能以______(填微粒符号)形态存在,不能以其它形态存在的原因是________________________。
(2)已知在碱性条件下,氯气会发生自身氧化还原反应,某反应体系中的物质为:KClO3、Cl2、KCl、KOH、H2O。
①写出该反应的化学方程式。____________________________。
②该反应中氧化剂与还原剂的质量比为_________。
(3)实验室利用反应6HCl+KClO3 → KCl+3H2O+3Cl2↑制取Cl2,当产生标准状况下的气体3.36 L时,转移电子_____mol。
(4)不同环境中,物质的性质可能会有所不同。根据上述两题的反应中KClO3和Cl2的氧化性强弱比较,你能得出的结论是________________________。
(5)铝铵矾[NH4Al(SO4)212H2O]也是常用的工业净水剂,其净水的化学原理是________________(用离子方程式表示)。
(6)在向铝铵矾溶液中逐滴滴加氢氧化钡溶液的过程中,下列关系可能正确的是_________。(选填编号)
a.n(SO42-)>n(NH4+)>n(A13+)>n(OH-)
b.n(A13+)>n(NH4+)>n(SO42-)>n(H+)
c.n(BaSO4)>n[A1(OH)3]>n(NH3·H2O)>n(A1O2-)
d.n(NH3·H2O)>n(BaSO4)>n[A1(OH)3]>n(A1O2-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com