
(12分)根据已学知识,回答下列问题:
(1)具有(n-1)d10n s2电子构型的元素位于周期表中 区和族。
(2)写出3P轨道上有2个未成对电子的元素名称:。
(3)日常生活中广泛应用的不锈钢,在其生产过程中添加了某种元素X,该元素的价电子排布式为3d54s1,该元素可与氧元素形成离子X2O72-,K2X2O7氧化浓盐酸生成氯气的同时还生成了X3+,写出该反应的离子方程式 。
(4)键能是指气态基态原子形成1 mol化学键释放的最低能量。某些化学键的键能如下表
格所示(单位:kJ·mol-1):
键 | H—H | N | O=O | F—F | H—Cl |
键能 | 436 | 946 | 498 | 157 | 431 |
键 | N—N | P—P | P—O | Cl—Cl | Br—Br |
键能 | 193 | 198 | 360 | 242.7 | 193 |
①由表中所列化学键形成的单质分子中,最不稳定的是。
②通过表中键能数据,计算说明N2分子中的键比键稳定(填“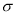 ”或“
”或“ ”)。
”)。
③化学反应的实质是旧化学键断裂和新化学键形成的过程。现有化学反应方程式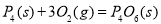 ,通过计算可以确定,1molP4(s)参加该反应, (填“吸收”或“放出”)的热量为kJ。
,通过计算可以确定,1molP4(s)参加该反应, (填“吸收”或“放出”)的热量为kJ。
(12分)
(1)ds ⅡB
(2)硅、硫(2分)
(3) Cr2O72-+14H++6Cl-=3Cl2↑+2 Cr3++7H2O;(2分)
(4) ①F2②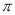
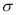 ③放出 1638 (2分)
③放出 1638 (2分)
【解析】
试题分析:(1)根据外围电子排布可知具有(n-1)d10n s2电子构型的元素位于周期表中ds区IIB;
(2)3p轨道上有2个未成对电子,则3p能级上可能是2个电子或4个电子,若是2个电子,则该元素是硅元素,若是4个电子则是硫元素;
(3)X元素的价电子排布式为3d54s1,则X是Cr元素,K2Cr2O7与浓盐酸反应生成氯气、水、Cr3+,所以离子方程式为Cr2O72-+14H++6Cl-=3Cl2↑+2 Cr3++7H2O;
(4)①由表中所给键能数据可知F-F键的键能最小,所以F-F键最易断裂,所以最不稳定的物质是F2;
②N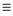 N的键能是946kJ/mol,N-N的键能是193 kJ/mol,则这个π键的键能是946-193=753kJ/mol,一个π键的键能是753/2=376.5kJ/mol>193 kJ/mol,所以π键比
N的键能是946kJ/mol,N-N的键能是193 kJ/mol,则这个π键的键能是946-193=753kJ/mol,一个π键的键能是753/2=376.5kJ/mol>193 kJ/mol,所以π键比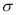 键稳定;
键稳定;
③1molP4中含有6molP-P键,该反应的热效应=反应物的总键能-生成物的总键能=6×198+3×498-12×360=-1638kJ/mol,所以1molP4(s)参加该反应,放出1638kJ的热量。
考点:考查元素的原子结构,元素的分区,反应热的计算,化学键的判断


科目:高中化学 来源:2014-2015学年四川省邛崃市高二上学期半期考试化学试卷(解析版) 题型:选择题
下列说法正确的是
①具有规则几何外形的固体不一定是晶体;②含有阳离子的晶体一定是离子晶体;③非极性分子中一定含有非极性键;④s-s σ键与s-p σ键的电子云形状相同;⑤含有共价键的晶体一定具有高的熔、沸点及硬度;⑥因为H—F的键能大于H—Cl的键能,所以HF的沸点高于HCl;⑦含有π键的化合物与只含σ键的化合物的化学性质不同;⑧中心原子采取sp3杂化的分子,其立体构形不一定是正四面体
A.①②⑤⑥ B.③⑦⑧ C.①⑦⑧ D.③④⑤⑧
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省成都外国语学校高二上学期期中化学试卷(解析版) 题型:选择题
向一定量的FeO、Fe、Fe2O3的混合物中加入100ml1mol/L的盐酸,恰好使混合物完全溶解,放出224ml标况下的气体,在所得溶液中滴入硫氰化钾溶液无血红色出现(即无3价铁)。若用足量CO在高温下还原同质量的此混合物,能得到铁的质量是
A、11.2g B、5.6g C、2.8g D、无法计算
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省成都外国语学校高二上学期期中化学试卷(解析版) 题型:选择题
下列现象与氢键有关的是
①HF的熔、沸点比ⅦA族其他元素氢化物的高
②乙醇可以和水以任意比互溶
③冰的密度比液态水的密度小
④水分子高温下也很稳定
⑤邻羟基苯甲酸的熔、沸点比对羟基苯甲酸的低
A.②③④⑤ B.①②③⑤ C.①②③④ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省成都外国语学校高二上学期期中化学试卷(解析版) 题型:选择题
下列对σ键的认识不正确的是
A.σ键不属于共价键,是另一种化学键
B.s—s σ键与s—p σ键的对称性相同
C.分子中含有共价键,则至少含有一个σ键
D.含有π键的化合物与只含σ键的化合物的化学性质不同
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川成都树德协进中学高二10月阶段性考试化学试卷(解析版) 题型:选择题
“神七”火箭使用的燃料仍是偏二甲肼,其结构可以看作是两个甲基和一个氨基(—NH2)替代了氨气分子中的三个氢原子,下列关于偏二甲肼的说法不正确的是
A.由碳、氢、氮三种元素组成 B.所有N、C原子都在同一平面上
C.分子中所有的N原子均是sp3杂化 D.分子式为C2H8N2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川成都树德协进中学高二10月阶段性考试化学试卷(解析版) 题型:选择题
x 、y为两种元素的原子,x的阴离子与y的阳离子具有相同的电子层结构,由此可知
A.x的原子半径大于y的原子半径
B.x的电负性大于y的电负性
C.x阴离子的半径小于y阳离子的半径
D.x的第一电离能小于y 的第一电离能
查看答案和解析>>
科目:高中化学 来源:2014-2015学年吉林省长春市新高三起点调研考试化学试卷(解析版) 题型:填空题
(16分)A、B、C、D、E均是短周期元素,其原子序数依次增大,A和B同周期,A和D同族,A原子最外层电子数是内层电子数的二倍,B元素族序数是周期数的三倍,B的阴离子与C的阳离子电子层结构相同,C的单质与 B 的单质在不同条件下反应,可生成C2B或C2B2,E是所在周期中原子半径最小的元素,请回答。
(1)D在元素周期表中的位置是 。
(2)C2B的电子式是 ;AB2的结构式是 。
(3)B、C、E离子半径的由大到小的顺序为 ;(用离子符号回答)A、D、E最高价氧化物对应水化物的酸性由强到弱的顺序为 。(用化学式回答)
(4)A、B气态氢化物沸点高的是 ;(用化学式回答)原因 。
(5)水中锰含量超标,容易使洁具和衣物染色,使水产生异味,EB2可以用来出去水中超标的Mn2+,生成黑色沉淀,当消耗13.50 g EB2时,共转移了1 mol电子,则反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年吉林省长春外国语学校高一上学期期中化学试卷(解析版) 题型:填空题
在Cu+4HNO3 = Cu(NO3)2 + 2NO2↑+2H2O反应中,________是氧化剂;______氧化产物;当6.4gCu参加反应时,电子转移的总数为______mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com