
【题目】一种镁氧电池电极材料为金属镁和吸附氧气的活性炭,电解液为KOH浓溶液,如图所示。下列说法不正确的是( )
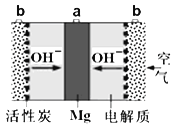
A.正极反应式为:O2+4e-+2H2O=4OH-
B.负极反应式为:Mg-2e-+2OH-=Mg(OH)2
C.电子的移动方向是由a经外电路到b
D.该电池在工作过程中,电解液KOH的浓度保持不变
【答案】D
【解析】
该镁氧电池中,镁电极为负极,通入空气的一极为正极,电解质显碱性,所以负极反应式为:Mg-2e-+2OH-=Mg(OH)2,负极镁被氧化,正极反应式为O2+4e-+2H2O=4OH-,正极上O2被还原,由此解题。
A.镁电极为负极,以负极反应式为:Mg-2e-+2OH-=Mg(OH)2,正极反应式为O2+4e-+2H2O=4OH-,总反应式为:2Mg+O2+2H2O=2Mg(OH)2,故A正确;
B.镁电极为负极,以负极反应式为:Mg-2e-+2OH-=Mg(OH)2,故B正确;
C.电子的移动方向是沿外电路由负极到正极,即a到b,故C正确;
D.反应中KOH被消耗,所以该电池在工作过程中,电解液KOH的浓度减小,故D错误;答案选D。


科目:高中化学 来源: 题型:
【题目】(1)火箭使用的推进剂燃料由N、H两种元素组成,且原子个数N:H=1:2,其水溶液显碱性,则该物质中N原子的杂化方式为______________________。
(2)笑气(N2O)曾被用作麻醉剂,但过度吸食会导致身体机能紊乱。预测N2O的结构式为________________________。
(3)元素的基态气态原子得到一个电子形成气态-1价离子时所放出的能量称作第一电子亲和能(E),-1价阴离子再获得一个电子的能量变化叫做第二电子亲和能,部分元素或离子的电子亲和能数据如下表所示。
元素 | C1 | Br | I | O | O- |
电子亲和能(kJ/mol) | 349 | 343 | 295 | 141 | -780 |
下列说法正确的是___________。
A.电子亲和能越大,说明越难得到电子
B.一个基态的气态氧原子得到一个电子成为O2-时放出141kJ的能量
C.氧元素的第二电子亲和能是-780kJ/mol
D.基态的气态氧原子得到两个电子成为O2-需要吸收能量
(4)在电解炼铝过程中加入冰晶石(用“A”代替),可起到降低Al2O3熔点的作用。冰晶石的生产原理为:2Al(OH)3+12HF+3Na2CO3=2A+3CO2↑+9H2O。根据题意完成下列填空:
①冰晶石的化学式为____________________________。
②冰晶石由两种微粒构成,冰晶石的晶胞结构如图甲所示,●位于大立方体的顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,那么大立方体的体心处所代表的微粒是___________(填微粒符号)。
③冰晶石溶液中不存在的微粒间作用力有________________(填选项字母)。
A 离子键 B 共价键 C 配位键 D 金属键 E 范德华力 F 氢键
④Al单质的晶体中原子的堆积方式如图乙所示,其晶胞特征如图丙所示,原子之间相互位置关系的平面图如图丁所示:

若已知A1的原子半径为d cm,NA代表阿伏加德罗常数,Al的相对原子质量为M,则晶胞中Al原子的配位数为________;Al晶体的密度为__________g.cm-3(用字母表示)。
(5)配合物Fe(CO)5的熔点-20℃,沸点103℃,可用于制备纯铁。Fe(CO)5的结构如图所示。

①Fe(CO)5晶体类型属于__________晶体。
②关于Fe(CO)5,下列说法正确的是_____。
A.Fe(CO)5是非极性分子,CO是极性分子
B.Fe(CO)5中Fe原子以sp3杂化方式与CO成键
C.1mol Fe(CO)5含有10mol配位键
D.反应Fe(CO)5=Fe+5CO没有新化学键生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化中,属于吸热反应的是( )
①液态水汽化②将胆矾加热变为白色粉末③浓H2SO4稀释 ④KClO3分解制O2⑤生石灰跟水反应生成熟石灰⑥石灰石高温分解⑦铝热反应⑧Ba(OH)2·8H2O与固体NH4Cl混合⑨C+H2O=CO+H2 ⑩Al与盐酸反应
A. ②③④⑥⑦⑧⑨ B. ②④⑥⑧⑨ C. ①②④⑥⑧ D. ②③④⑧⑨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列溶液中各组离子一定能够大量共存的是( )
A.使紫色石蕊试液变红的溶液:Fe2+、Mg2+、![]() 、Cl-
、Cl-
B.0.1mol·L-1NaAlO2溶液:K+、![]() 、
、![]() 、
、![]()
C.![]() =0.lmol·L-1的溶液:Na+、K+、
=0.lmol·L-1的溶液:Na+、K+、![]() 、
、![]()
D.通入足量SO2后的溶液:Na+、Ba2+、ClO-、CH3COO-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知由短周期元素构成的三种粒子:甲a(单核带一个单位正电荷)、乙I(四核不带电荷)、丙e(双核带一个单位负电荷),它们都有10个电子。物质A由甲、丙构成,B、C、D、K都是单质,反应①~⑤都是用于工业生产的反应,各有关物质之间的相互反应转化关系如下图所示:
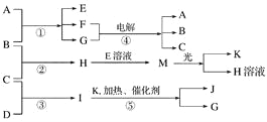
请填写下列空白:
(1)写出下列物质的化学式:B________,I________,J________。
(2) A的化学式是__________________。
(3)写出下列反应的离子方程式:
①H+E(溶液)→M_________________________________________________________。
②I溶于G________________________________________________________________。
(4)写出反应①的化学方程式_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸H2C2O4为二元弱酸,Kal(H2C2O4)=5.4×10-2,Ka2(H2C2O4)=5.4×10-5)。室温下向0.lmol·L-l的Na2C2O4溶液中缓慢通入HCl气体直至过量(忽略溶液体积变化和HCl的挥发)。该过程中得到的下列溶液中微粒的物质的量浓度关系一定正确的是( )
A.0.lmol·L-lNa2C2O4溶液:c(Na+)>c(C2O![]() )>c(HC2O
)>c(HC2O![]() )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
B.pH=7的溶液:c(Na+)=2c(C2O![]() )+c(HC2O
)+c(HC2O![]() )
)
C.c(C2O![]() )=c(HC2O
)=c(HC2O![]() )的溶液:c(Cl-)>c(C2O
)的溶液:c(Cl-)>c(C2O![]() )+2c(H2C2O4)
)+2c(H2C2O4)
D.c(Na)=2c(Cl-)的溶液:c(Na+)+c(H+)>c(Cl-)+c(HC2O![]() )+c(C2O
)+c(C2O![]() )+c(H2C2O4)+c(OH-)
)+c(H2C2O4)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物G是合成鬼臼脂的中间体,可通过以下方法合成:
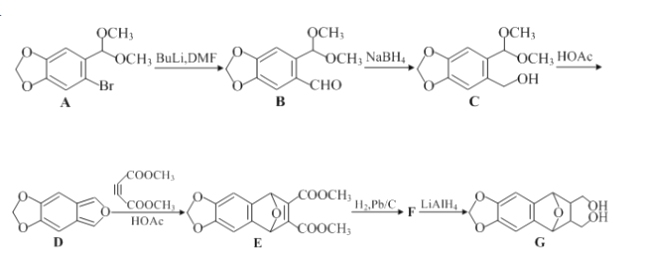
(1)E中的含氧官能团的名称为________、________。
(2)B→C的反应类型为________。
(3)F的分子式为C15H14O7,写出F的结构简式:________。
(4)B的同分异构体X同时满足下列条件。写出符合条件的X的一种结构简式:________。
①属于芳香族化合物;
②在酸性条件下水解后可得三种产物,且每种产物均只含有两种化学环境不同的氢。
(5)已知: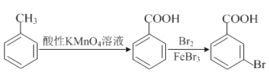 。请以甲苯、BuLi和DMF为原料制备
。请以甲苯、BuLi和DMF为原料制备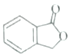 ,写出相应的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。____________
,写出相应的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】大气中的部分碘源于O3对海水中I-的氧化。某科学小组进行O3与含I-溶液反应相关研究。
(1)O3将I-氧化生成I2的过程由3步反应组成:
①I-(aq)+O3(g)![]() IO-(aq)+O2(g) ΔH1
IO-(aq)+O2(g) ΔH1
②IO-(aq)+H+(aq)![]() HIO(aq) ΔH2
HIO(aq) ΔH2
③HIO(aq)+I-(aq)+H+(aq)![]() I2(aq)+H2O(l) ΔH3
I2(aq)+H2O(l) ΔH3
用热化学方程式表示O3氧化I-生成I2的反应___。
(2)O3在水中易分解,在一定条件下,O3的浓度减少一半时所需的时间(t)如下表所示。已知:O3的起始浓度为0.0216mol·L-1。
pH t/min T/℃ | 3.0 | 4.0 | 5.0 | 6.0 |
20 | 301 | 231 | 169 | 58 |
30 | 158 | 108 | 48 | 15 |
50 | 31 | 35 | 15 | 7 |
①在30℃、pH=4.0条件下,O3的分解速率为___mol·L-1·min-1。
②pH增大能加速O3分解,表明对O3分解起催化作用的是____。
③根据表中数据,推测O3在下列条件下分解速率依次增大的顺序为___(填字母)。
a.40℃、pH=3.0 b.10℃、pH=4.0 c.30℃、pH=7.0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X是一种有机合成中间体,某研究小组采用如下路线合成X和一种常见的高分子化合物D。首先合成D和乙醇,线路如下:
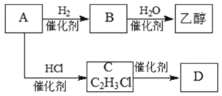
(1)已知A是一种常见的气态烃。写出A分子的结构式________________。
![]() 的化学方程式________________,该反应的类型是:________________。
的化学方程式________________,该反应的类型是:________________。
(2)写出化合物B的结构简式________________,实验室制取B反应的化学方程式:________________。乙醇中官能团的名称是:________。
进一步合成X线路如下:
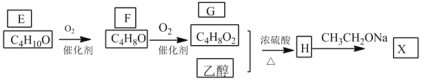
已知:①化合物E的结构中有2个甲基
②![]()

(3)若G中混有F,可以用来检验的试剂是________________,反应的化学方程式为________________。
(4)写出![]() 的化学方程式是________________;反应类型是________。
的化学方程式是________________;反应类型是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com