
【题目】化合物F是合成吲哚-2-酮类药物的一种中间体,其合成路线如下:
![]() (
(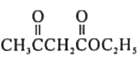 )
)![]()
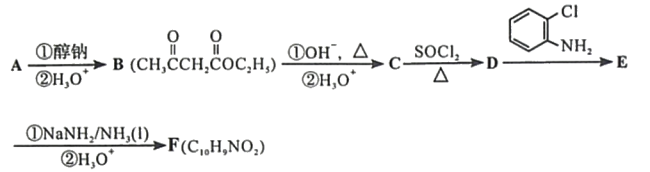
知:Ⅰ.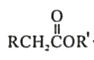
![]()
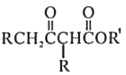
Ⅱ. 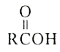
![]()
![]()
![]()
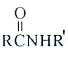
Ⅲ. 
![]()
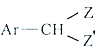
Ar为芳基;X=Cl,Br;Z或Z′=COR, CONHR,COOR等。
回答下列问题:
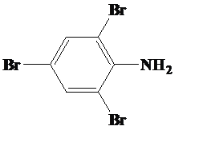
(1)实验室制备A的化学方程式为___________,提高A产率的方法是______________;A的某同分异构体只有一种化学环境的碳原子,其结构简式为_______________。
(2)C→D的反应类型为____________;E中含氧官能团的名称为____________。
(3)C的结构简式为____________,F的结构简式为____________。
(4)Br2和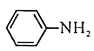 的反应与Br2和苯酚的反应类似,以
的反应与Br2和苯酚的反应类似,以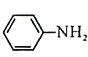 和
和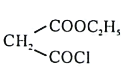 为原料合成
为原料合成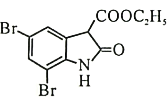 ,写出能获得更多目标产物的较优合成路线(其它试剂任选)________。
,写出能获得更多目标产物的较优合成路线(其它试剂任选)________。
【答案】![]() 及时蒸出产物(或增大乙酸或乙醇的用量)
及时蒸出产物(或增大乙酸或乙醇的用量) 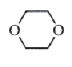 取代反应 羰基、酰胺基 CH3COCH2COOH
取代反应 羰基、酰胺基 CH3COCH2COOH 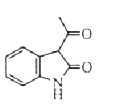

【解析】
根据B的结构和已知条件Ⅰ可知R=H、R’=CH2H5,故A为CH3COOC2H5(乙酸乙酯),有机物B经过碱性条件下水解再酸化形成有机物C(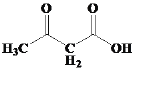 ),有机物C与SOCl2作用通过已知条件Ⅱ生成有机物D(
),有机物C与SOCl2作用通过已知条件Ⅱ生成有机物D(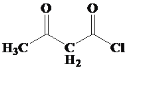 ),有机物D与邻氯苯胺反应生成有机物E(
),有机物D与邻氯苯胺反应生成有机物E(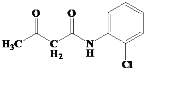 ),有机物E经已知条件Ⅲ发生成环反应生成有机物F(
),有机物E经已知条件Ⅲ发生成环反应生成有机物F(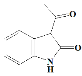 ),据此分析。
),据此分析。
(1)根据分析,有机物A为乙酸乙酯,在实验室中用乙醇和乙酸在浓硫酸的催化下制备,反应方程式为CH3COOH+CH3CH2OH![]() CH3COOC2H5+H2O;该反应为可逆反应,若想提高乙酸乙酯的产率需要及时的将生成物蒸出或增大反应的用量;A的某种同分异构体只有1种化学环境的C原子,说明该同分异构体是一个对称结构,含有两条对称轴,则该有机物的结构为
CH3COOC2H5+H2O;该反应为可逆反应,若想提高乙酸乙酯的产率需要及时的将生成物蒸出或增大反应的用量;A的某种同分异构体只有1种化学环境的C原子,说明该同分异构体是一个对称结构,含有两条对称轴,则该有机物的结构为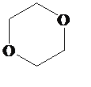 ;
;
(2)根据分析,C→D为 和SOCl2的反应,反应类型为取代反应;E的结构为
和SOCl2的反应,反应类型为取代反应;E的结构为 ,其结构中含氧官能团为羰基、酰胺基;
,其结构中含氧官能团为羰基、酰胺基;
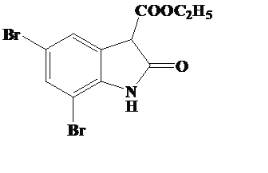
(3)根据分析,C的结构简式为CH3COCH2COOH;F的结构简式为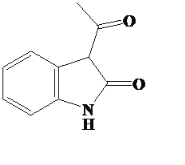 ;
;
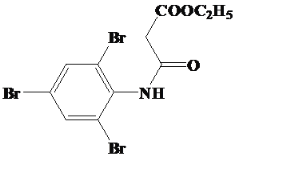
(4)以苯胺和H5C2OOCCH2COCl为原料制得目标产物,可将苯胺与溴反应生成2,4,6—三溴苯胺,再将2,4,6—三溴苯胺与H5C2OOCCH2COCl反应发生已知条件Ⅱ的取代反应,再发生已知条件Ⅲ的成环反应即可得到目标产物,反应的流程为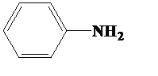
![]()
![]()
![]()


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
【题目】![]() 为阿伏加德罗常数的值。下列说法正确的是( )
为阿伏加德罗常数的值。下列说法正确的是( )
A. ![]() ,
,![]() 完全反应转移的电子数为
完全反应转移的电子数为![]()
B. 用电解粗铜的方法精炼铜,当电路中通过的电子数为![]() 时,阳极应有
时,阳极应有![]() 转化为
转化为![]()
C. 常温下,![]() 的
的![]() 溶液中,水电离出的
溶液中,水电离出的![]() 数为
数为![]()
D. ![]() 浓度为
浓度为![]() 的
的![]() 溶液中,阴离子数为
溶液中,阴离子数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电子排布的表述正确的是( )
A.![]() 可表示单核8电子粒子基态时电子排布
可表示单核8电子粒子基态时电子排布
B.![]() 此图错误,违背了洪特规则
此图错误,违背了洪特规则
C.2p3表示基态氮原子的外围电子排布式
D.![]() 表示处于激发态的硼原子的电子排布图
表示处于激发态的硼原子的电子排布图
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微生物脱盐电池是一种高效、经济的能源装置,利用微生物处理有机废水获得电能,同时可实现海水淡化。现以NaCl溶液模拟海水,采用惰性电极,用下图装置处理有机废水(以含 CH3COO-的溶液为例)。下列说法错误的是
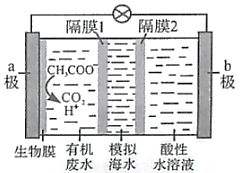
A.负极反应为 ![]()
B.隔膜1为阳离子交换膜,隔膜2为阴离子交换膜
C.当电路中转移1mol电子时,模拟海水理论上除盐58.5g
D.电池工作一段时间后,正、负极产生气体的物质的量之比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】探究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下:
Ⅰ. ![]()
![]()
Ⅱ. ![]()
![]()
Ⅲ. ![]()
![]()
回答下列问题:
(1)![]() _________
_________![]() 。
。
(2)一定条件下,向体积为VL的恒容密闭容器中通入1 mol CO2和3 mol H2发生上述反应,达到平衡时,容器中CH3OH(g)为ɑ mol,CO为b mol,此时H2O(g)的浓度为__________mol﹒L-1(用含a、b、V的代数式表示,下同),反应Ⅲ的平衡常数为___________。
(3)不同压强下,按照n(CO2):n(H2)=1:3投料,实验测定CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如下图所示。
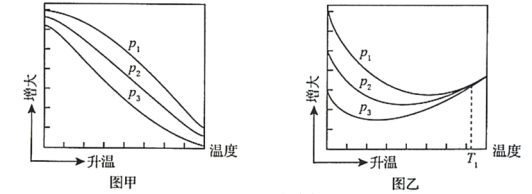
已知:CO2的平衡转化率=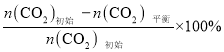
CH3OH的平衡产率=![]()
其中纵坐标表示CO2平衡转化率的是图___________(填“甲”或“乙”);压强p1、p2、p3由大到小的顺序为___________;图乙中T1温度时,三条曲线几乎交于一点的原因是___________。
(4)为同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择的反应条件为_________(填标号)。
A.低温、高压 B.高温、低压 C.低温、低压 D.高温、高压
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解物质的量浓度相同、体积比为2∶3的CuSO4和NaCl的混合溶液,可能发生的反应有( )
①2Cu2++2H2O![]() 2Cu+4H++O2↑
2Cu+4H++O2↑
②Cu2++2Cl-![]() Cu+Cl2↑
Cu+Cl2↑
③2Cl-+2H+![]() H2↑+Cl2↑
H2↑+Cl2↑
④2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
A.①②③B.①②④C.②③④D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究原电池和电解池的工作原理,某研究性小组分别用如图所示装置进行实验。
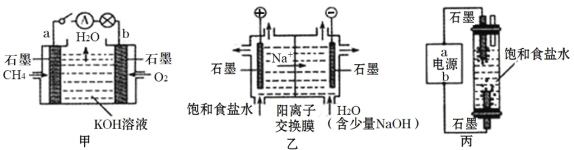
(1)甲装置中,a电极的反应式为_____。
(2)乙装置中,阴极区产物为_____。
(3)丙装置是一种家用84消毒液(NaClO)发生器。外接电源a为_____ (填“正”或“负”)极,该装置内发生反应的化学方程式为_____、_____。
(4)若甲装置作为乙装置的电源,一段时间后,甲中消耗气体与乙中产生气体的物质的量之比为_____ (不考虑气体的溶解)。
(5)某工厂采用电解法处理含Cr2O72-的废水,耐酸电解槽用铁板作阴、阳极,槽内盛放含铬废水,Cr2O72-被还原成为Cr3+,Cr3在阴极区生成Cr(OH)3沉淀除去,工作原理如图。
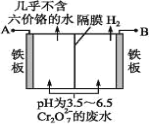
①写出电解时阴极的电极反应式____。
②写出Cr2O72-被还原为Cr3+的离子方程式____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用太阳能光解水,制备的H2用于还原CO2合成有机物,可实现资源的再利用。回答下列问题:
Ⅰ.半导体光催化剂浸入水或电解质溶液中,光照时可在其表面得到产物
(1)下图为该催化剂在水中发生光催化反应的原理示意图。光解水能量转化形式为___________。
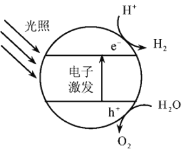
(2)若将该催化剂置于Na2SO3溶液中,产物之一为![]() ,另一产物为__________。若将该催化剂置于AgNO3溶液中,产物之一为O2,写出生成另一产物的离子反应式__________。
,另一产物为__________。若将该催化剂置于AgNO3溶液中,产物之一为O2,写出生成另一产物的离子反应式__________。
Ⅱ.用H2还原CO2可以在一定条下合成CH3OH(不考虑副反应):![]()
(3)某温度下,恒容密闭容器中,CO2和H2的起始浓度分别为 a molL-1和3 a molL-1,反应平衡时,CH3OH的产率为b,该温度下反应平衡常数的值为___________。
(4)恒压下,CO2和H2的起始物质的量比为1:3时,该反应在无分子筛膜时甲醇的平衡产率和有分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出H2O。
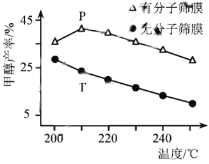
①甲醇平衡产率随温度升高而降低的原因为____________。
②P点甲醇产率高于T点的原因为___________。
③根据上图,在此条件下采用该分子筛膜时的最佳反应温度为___________°C。
Ⅲ.调节溶液pH可实现工业废气CO2的捕获和释放
(5) ![]() 的空间构型为__________。已知25℃碳酸电离常数为Ka1、Ka2,当溶液pH=12时,
的空间构型为__________。已知25℃碳酸电离常数为Ka1、Ka2,当溶液pH=12时,![]() =1:_______:__________。
=1:_______:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中进行反应:2SO2(g)+O2(g) ![]() 2SO3(g) ΔH<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是
2SO3(g) ΔH<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是

A. 图Ⅰ表示温度对化学平衡的影响,且甲的温度较高
B. 图Ⅱ表示t0时刻使用催化剂对反应速率的影响
C. 图Ⅲ表示t0时刻增大O2的浓度对反应速率的影响
D. 图Ⅳ表示t0时升温对反应速率的影响
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com