
【题目】硫酸的工业制备是一个重要的化工生产过程,但同时在生产过程中会产生大量SO2等污染物。以硫酸工业的尾气、氨水、石灰石、焦炭及氯化钾为原料可以合成有重要用途的硫化钙、硫酸钾、氯化铵、亚硫酸铵等物质。合成路线如下:

完成下列填空:
(1)某电厂每月用煤300t(煤中含硫的质量分数为2.5%),若燃烧时煤中的硫全部转化为二氧化硫,现用反应Ⅰ的原理将尾气中的SO2转化为石膏,且反应过程中96%的硫转化为石膏,则可生产石膏______ t。
(2)操作a中,必须的操作步骤有蒸发、___________、___________等;
(3)反应Ⅲ中氧化剂与还原剂的物质的量之比为__________;
(4)写出反应Ⅳ的方程式______________ ;操作b所得滤液中阳离子的检验方法是________________。
(5)反应Ⅴ在25℃,40%乙二醇溶液中进行,该复分解反应能顺利进行的原因是___________;
(6)该生产过程中可以循环使用的物质是_______________。
【答案】38.7 冷却结晶 过滤 1:4 CaSO4+2NH3+CO2+H2O=(NH4)2SO4+CaCO3↓ 取溶液少许加入NaOH并加热,生成有刺激性气味的气体能使湿润的红色石蕊试纸变蓝 由于K2SO4在乙二醇溶液中的溶解度小,能够形成晶体而析出,因此符合复分解反应发生的条件 CaCO3,CO2
【解析】
由流程可知,I中发生的反应为2CaCO3+O2+2SO2=2CaSO4+2CO2,反应Ⅳ为CaSO4、NH3和CO2反应生成碳酸钙和硫酸铵,发生CO2+2NH3+CaSO4+H2O =CaCO3↓+(NH4)2SO4,可知CaCO3、CO2可循环使用,反应Ⅴ为硫酸铵溶液中加入氯化钾生成硫酸钾晶体,所以操作b为过滤,滤液中含有的阳离子为铵根离子,Ⅱ中发生SO2+2NH3·H2O=(NH4)2SO3+H2O,Ⅲ中发生CaSO4+4C=CaS+4CO↑,据此分析解答。
(1)二氧化硫与碳酸钙反应生成亚硫酸钙与二氧化碳,反应方程式为:SO2+CaCO3=CaSO3+CO2,亚硫酸钙在水存在的条件下被氧气氧化生成CaSO42H2O,反应方程式为:2CaSO3+O2+4H2O=2(CaSO42H2O),总反应为:2CaCO3+2SO2+O2+4H2O═2(CaSO42H2O)+2CO2,因此有
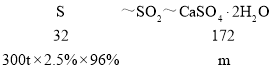
![]() =
=![]() ,解得:m=38.7t,故答案为:38.7;
,解得:m=38.7t,故答案为:38.7;
(2)操作a是从亚硫酸铵溶液中获得亚硫酸铵晶体,亚硫酸铵晶体受热易分解,所以操作a为冷却结晶、过滤,故答案为:冷却结晶;过滤;
(3)反应Ⅲ的化学方程式为:CaSO4+4C=CaS+4CO↑,其中氧化剂为CaSO4,还原剂为C,反应中氧化剂与还原剂的物质的量之比为1∶4,故答案为:1∶4;
(4)反应Ⅳ的化学方程式为CaSO4+2NH3+CO2+H2O=(NH4)2SO4+CaCO3↓,操作b过滤,所得滤液中阳离子为铵根离子,具有铵根离子的方法为:取溶液少许加入NaOH并加热,生成有刺激性气味的气体,并能使湿润的红色石蕊试纸变蓝,故答案为:CaSO4+2NH3+CO2+H2O=(NH4)2SO4+CaCO3↓;取溶液少许加入NaOH并加热,生成有刺激性气味的气体,并能使湿润的红色石蕊试纸变蓝;
(5)反应V中选用了40%的乙二醇溶液,温度控制在25℃,是因为乙二醇能够降低硫酸钾的溶解度,有利于硫酸钾析出,故答案为:由于K2SO4在乙二醇溶液中的溶解度小,能够形成晶体而析出,因此符合复分解反应发生的条件;
(6)根据上面的分析可知,该生产过程中可以循环使用的物质为CaCO3,CO2,故答案为:CaCO3,CO2.


 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:
【题目】40℃硝酸钾饱和溶液先升温至80℃,在恒温下蒸发部分溶剂至析出少量溶质,然后将溶液逐渐冷却至60℃.下列示意图中能正确表示整个过程中溶液浓度a%与时间t关系的是( )
A.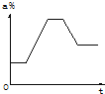 B.
B. C.
C. D.
D.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.95℃纯水显中性,故pH=7
B.稀释弱电解质溶液时,溶液中所有粒子浓度都减小
C.pH试纸在使用之前应用蒸馏水润湿
D.室温下,向10 mL pH=3的醋酸溶液中加水稀释后,溶液中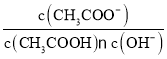 的值不变
的值不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W、Q原子序数依次增大,Y元素最外层电子数是其电子层数的3倍,Q与Y同主族,X与Y构成的化合物可引起光化学烟雾,Z、W、Q的最高价氧化物的水化物两两之间均能发生反应。下列说法正确的是( )
A.简单氢化物的沸点:Y<QB.W的氧化物可作耐高温材料
C.简单离子半径最大的为ZD.气态氢化物的稳定性:Y<X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸铵[(NH4)2C2O4]为无色柱状晶体,不稳定,受热易分解,可用于测定Ca2+、Mg2+的含量。
I.某同学利用如图所示实验装置检验草酸铵的分解产物。
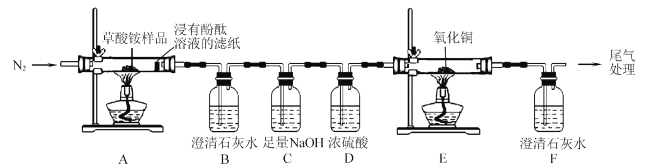
(l)实验过程中,观察到浸有酚酞溶液的滤纸变红,装置B中澄清石灰水变浑浊,说明分解产物中含有____(填化学式);若观察到____, 说明分解产物中含有CO2草酸铵分解的化学方程式为____。
(2)反应开始前,通人氮气的目的是____。
(3)装置C的作用是 ____。
(4)还有一种分解产物在一定条件下也能还原CuO,该反应的化学方程式为 _____。
Ⅱ.该同学利用草酸铵测定血液中钙元素的含量。
(5)取20. 00mL血液样品,定容至l00mL,分别取三份体积均为25. 00mL稀释后的血液样品,加入草酸铵,生成草酸钙沉淀,过滤,将该沉淀溶于过量稀硫酸中,然后用0. 0l00mol/LKMnO4溶液进行滴定。滴定至终点时的实验现象为____。三次滴定实验消耗KMnO4溶液的体积分别为0.43mL,0.4lmL,0.52mL,则该血液样品中钙元素的含量为__________ mmol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,有关物质的电离平衡常数如下:

(1)电解质由强至弱顺序为___(用化学式表示,下同)。
(2)常温下,0.02mol·L-1的CH3COOH溶液的电离度约为___,体积为10 mL pH=2的醋酸溶液与亚硫酸溶液分别加蒸馏水稀释至1000mL,稀释后溶液的pH,前者___后者(填“>”、“<”或“=”)。
(3)下列离子CH3COO-、CO32-、HSO3-、SO32-在溶液中结合H+的能力由大到小的顺序为_____。
(4)NaHSO3溶液显酸性的原因_____(离子方程式配适当文字叙述),其溶液中离子浓度由大到小的关系是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积一定的密闭容器中,置入一定量的一氧化氮和足量碳发生化学反应:C(s)+2NO(g)CO2(g)+N2(g)+Q,平衡时c (NO)与温度T的关系如图所示,则下列说法正确的是
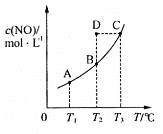
A.该反应的Q >0
B.若该反应在T1、T2时的平衡常数分别为K1、K2,则K1<K2
C.在T2时,若反应体系处于状态D,则此时V正>V逆
D.若状态B、C、D的压强分别为PB、PC 、PD ,则 PC=PD>PB
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属镓是由门捷列夫第一个预言成真的元素,有“电子工业脊梁”的美誉,它与铝同主族,其氧化物和氢氧化物均为两性化合物,镓及其化合物应用广泛。粉煤灰中可以提取镓,粉煤灰中的主要成分为Ga2O3,含CaO、SiO2、Al2O3等杂质。镓的熔点较低(29.8℃).沸点很高(2403℃)。
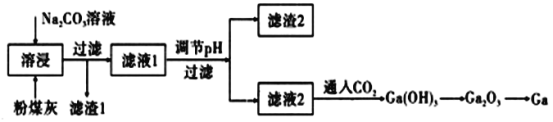
(1)滤渣1的主要成分为:___________。
(2)为了提高溶浸效率可以采用的措施有(写两种):____________。
(3)写出镓单质与氢氧化钠溶液反应的离子方程式:___________。
(4)其他镓的化合物在生活和前沿科技上有广泛应用,根据已学知识回答下列问题:
①GaCl3溶液制备GaCl3固体,应如何操作:_________。
②当代工业上固态氮化镓(GaN)的制备方法是利用镓与NH3在1000℃高温下合成,同时生成氢气,每消耗1 mol Ga时放出15.135 kJ热量。该可逆反应的热化学方程式是______。
(5)下表是两种两性氢氧化物的电离常数。

将一块镓铝合金完全溶于烧碱溶液,再往反应后的溶液中缓缓通入CO2,最先析出的氢氧化物是____。
(6)电解法可以提纯粗镓(内含Zn、Fe、Cu等杂质),以NaOH水溶液为电解质,在阴极析出高纯度的镓,请写出阴极电极反应:_____(离子氧化顺序为:Zn2+<Ga3+<Fe2+)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:25℃时,0.1000mol·L-lCH3COOH溶液中CH3COOH的电离度(×100%)约为1%。该温度下,用0.1000mol·L-l氨水滴定10.00mL0.1000mol·L-lCH3COOH溶液,溶液的pH与溶液的导电能力(I)的关系如图所示。下列说法中正确的是( )
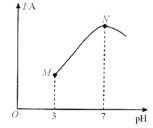
A.M点→N点,水的电离程度逐渐增大
B.25℃时,CH3COOH 的电离常数约为1.0×10-2
C.N点溶液中,c(CH3COO-)>c(NH4+)
D.当滴入20 mL氨水时,溶液中c(CH3COO-)>c(NH4+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com