
| A、pH=3的HX酸与pH=11的YOH碱等体积混合,所得溶液的pH一定为7 |
| B、在0.1 mol/L (NH4)2Fe(SO4)2溶液中c(H+)+c(NH4+)+c(Fe2+)=c(OH-)+c(SO42-) |
| C、在醋酸钠溶液中加入适量醋酸,所得酸性溶液中c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| D、0.2 mol/L HCl与0.1 mol/L NaAlO2等体积混合,所得溶液中c(Cl-)>c(Na+)>c(Al3+)>c(H+)>c(OH-) |
| 1 |
| 3 |
| 2 |
| 3 |
| 1 |
| 3 |
| 2 |
| 3 |


 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案科目:高中化学 来源: 题型:
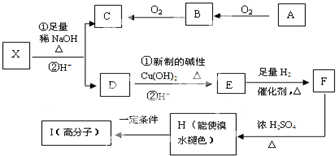
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 10 |
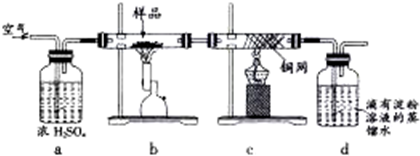
查看答案和解析>>
科目:高中化学 来源: 题型:
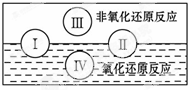 已知元素X、Y、Z质子数都小于18,并且质子数X+Y=Z.X原子的电子层数与核外电子总数相同,Z原子有两个电子层,最外层电子数是内层电子数的三倍,则:
已知元素X、Y、Z质子数都小于18,并且质子数X+Y=Z.X原子的电子层数与核外电子总数相同,Z原子有两个电子层,最外层电子数是内层电子数的三倍,则:查看答案和解析>>
科目:高中化学 来源: 题型:
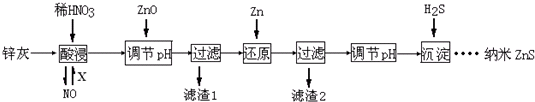
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1 mol/L |
| B、0.5 mol/L |
| C、4 mol/L |
| D、1 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、SO42-、Cu2+、NO3- |
| B、Ag+、Fe3+、Cl-、SO42- |
| C、H+、I-、NO3-、SiO32- |
| D、NH4+、OH-、Cl-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、浓硝酸存放在带橡皮塞的棕色玻璃瓶中 |
| B、汽油或煤油存放在带橡皮塞的棕色玻璃瓶中 |
| C、碳酸钠溶液存放在配有磨口塞的棕色玻璃瓶中 |
| D、氯水或硝酸银溶液存放在配有磨口塞的棕色玻璃瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com