
 )是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如图
)是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如图
 ,甲苯和氯气在光照条件下发生取代反应生成C,C发生水解(取代)反应得D,则C为
,甲苯和氯气在光照条件下发生取代反应生成C,C发生水解(取代)反应得D,则C为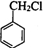 ,结合有机物的结构和性质解答该题.
,结合有机物的结构和性质解答该题. ,甲苯和氯气在光照条件下发生取代反应生成C,C发生水解(取代)反应得D,则C为
,甲苯和氯气在光照条件下发生取代反应生成C,C发生水解(取代)反应得D,则C为 ,
,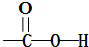 ,
,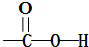 ;
; ,D的含苯环的同分异构体中,能使FeCI3溶液显紫色即有酚羟基的为苯环上连有甲基和羟基的结构,有邻间对三种,
,D的含苯环的同分异构体中,能使FeCI3溶液显紫色即有酚羟基的为苯环上连有甲基和羟基的结构,有邻间对三种, ,根据反应⑤的方程式
,根据反应⑤的方程式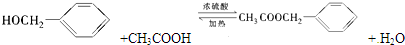 可知,120克B即2mol,与足量的D反应,若B的转化率为60%,则生成乙酸苯甲酯的质量为2×60%×150g=180g,
可知,120克B即2mol,与足量的D反应,若B的转化率为60%,则生成乙酸苯甲酯的质量为2×60%×150g=180g, 等,
等, .
.


科目:高中化学 来源: 题型:
 在试管A中加入3mL 乙醇,然后边振荡试管边慢慢加入2mL 浓硫酸和2mL 乙酸,按如图所示连接好装置进行实验,以制取乙酸乙酯.
在试管A中加入3mL 乙醇,然后边振荡试管边慢慢加入2mL 浓硫酸和2mL 乙酸,按如图所示连接好装置进行实验,以制取乙酸乙酯.查看答案和解析>>
科目:高中化学 来源: 题型:

| A、从①口进气,用排水法集气 |
| B、从①口进气,用排气法集气 |
| C、从②口进气,用排水法集气 |
| D、从②口进气,用排气法集气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 在元素周期表前四周期中原子序数依次增大的六种元素A、B、C、D、E、F中,A与其余五种元素既不同周期也不同主族,第二周期元素B原子的核外成对电子数是未成对电子数的2倍,C原子的最外层p轨道的电子为半充满结构,D原子核外电子有8种不同的运动状态,E的基态原子在前四周期元素的基态原子中单电子数最多,F元素的基态原子最外能层只有一个电子,其它能层均已充满电子.
在元素周期表前四周期中原子序数依次增大的六种元素A、B、C、D、E、F中,A与其余五种元素既不同周期也不同主族,第二周期元素B原子的核外成对电子数是未成对电子数的2倍,C原子的最外层p轨道的电子为半充满结构,D原子核外电子有8种不同的运动状态,E的基态原子在前四周期元素的基态原子中单电子数最多,F元素的基态原子最外能层只有一个电子,其它能层均已充满电子.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
+ 4 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、各取少许溶液分别放入铜片 |
| B、分别与石蕊试液作用 |
| C、用玻璃棒各蘸少许液涂在纸上 |
| D、各取少许溶液分别放入铝片 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、锌是负极,其质量逐渐减小 |
| B、氢离子在铜表面被氧化,产生气泡 |
| C、该装置可将化学能转化为电能 |
| D、电子从锌片经导线流向铜片 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com