
【题目】已知A为常见的金属单质,根据如图所示的关系:
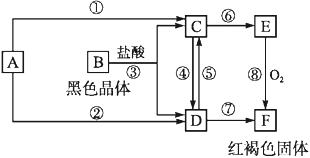
(1)确定C、E的化学式,C为_____,E为_____
(2)写出④的离子方程式,⑧的化学方程式:
④_________________________,
⑧________________________。
【答案】FeCl2 Fe(OH)2 2Fe2++Cl2=2Fe3++2Cl- 4Fe(OH)2+O2+2H2O=4Fe(OH)3
【解析】
A为常见的金属单质,F为红褐色固体,且E和O2反应得到F,则F为Fe(OH)3,E为Fe(OH)2,A为Fe;再根据图中的转化关系,可以推出B为Fe3O4,C为FeCl2,D为FeCl3。
经分析,A为Fe,B为Fe3O4,C为FeCl2,D为FeCl3,E为Fe(OH)2,F为Fe(OH)3,则:
(1)C为FeCl2,E为Fe(OH)2;
(2)反应④的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-;反应⑧的化学方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3。


科目:高中化学 来源: 题型:
【题目】25℃时,pH=2的盐酸和醋酸各1mL分别加水稀释,pH随溶液体积变化的曲线如下图所示。下列说法不正确的是( )

A. 曲线Ⅰ代表盐酸的稀释过程 B. a溶液的导电性比c溶液的导电性强
C. a溶液中和氢氧化钠的能力强于b溶液 D. 将a、b两溶液加热至30℃, 变小
变小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活、社会密切相关.下列有关说法中不正确的是
A.2008年北京奥运会开幕式上的“脚印”等焰火让全世界为之欢呼、倾倒,这主要是利用了化学中“焰色反应”的有关知识
B.神七宇航员所穿航天服是由我国自行研制的新型“连续纤维增韧”航空材料做成,其主要成分是由碳化硅、陶瓷和碳纤维复合而成的,它是一种新型无机非金属材料
C.腌制食品中应严格控制![]() 的用量
的用量
D.从海水中可提取Mg,用惰性电极电解熔融的![]() 或其水溶液都可制得Mg
或其水溶液都可制得Mg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下用H2还原CuCl制备活性铜,反应原理如下:
2Cu(s)+Cl2(g) ![]() 2CuCl(s) ΔH1=-36 kJ·mol-1①
2CuCl(s) ΔH1=-36 kJ·mol-1①
H2(g)+2CuCl(s) ![]() 2Cu(s)+2HCl(g) ΔH2②
2Cu(s)+2HCl(g) ΔH2②
有关物质的键能数据如下表:
物质 | H2 | Cl2 | HCl |
键能/kJ·mol-1 | 436 | 243 | 432 |
(1)ΔH2=________kJ·mol-1。
(2)经测定反应②制备活性铜的反应趋势大,原因是__________。
(3)在某温度下,反应①达到平衡状态,在tl时,增加压强到原来的2倍(Cu的量足够),在图中画出Cl2浓度的变化趋势线。________________________

(4)白色不溶于水的CuCl可以由电解法制得,如图所示:

①装置中用的交换膜为________。
A.阳离子交换膜 B.阴离子交换膜
C.质子交换膜 D.氢氧根离子交换膜
②阳极的电极反应式为______________________________________________。
(5)已知CuCl可溶解于稀硝酸,写出该反应的化学方程式:
________________________________________________________________________。
(6)根据已学知识写出制取CuCl的一种方法,用化学方程式表示:____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X是某金属单质,X、A、B、C含同一种元素,可发生如下转化:
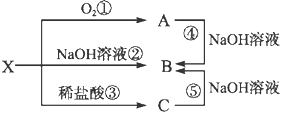
(1)写出以下反应的离子方程式:
②___________________________;
④___________________________。
(2)确定化学式B_______ X_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学电源在日常生活和高科技领域中都有广泛应用。下列说法不正确的是
A.  Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度增加
Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度增加
B.  正极的电极反应式为Ag2O+2e+H2O2Ag+2OH
正极的电极反应式为Ag2O+2e+H2O2Ag+2OH
C.  锌筒作负极,发生氧化反应,锌筒会变薄
锌筒作负极,发生氧化反应,锌筒会变薄
D.  使用一段时间后,电解质溶液的酸性减弱,导电能力下降
使用一段时间后,电解质溶液的酸性减弱,导电能力下降
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,H2SO3的电离常数:Ka1=1.54×102,Ka2=1×107。向mmL0.1mol/LH2SO3溶液中滴加0.1mol·L1KOH溶液,混合溶液中水电离的c水(H+)与KOH溶液体积V的关系如图所示,下列说法不正确的是
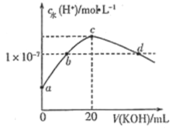
A.m=10
B.c点对应的溶液中存在c(K+)>c(HSO3-)+2c(SO32)
C.b、d两点溶液的pH=7
D.SO32-+H2OHSO3-+OH的K=1×107
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知pOH= -lg c(OH-)。25℃时,向20.00mL 0.10mol/L弱碱MOH溶液中滴加0.10 mol/L盐酸,溶液pH、pOH随滴入盐酸体积的变化如图所示,下列说法正确的是
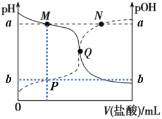
A.Q点消耗盐酸的体积大于20.00mL
B.V(HCl)=40.00mL时,溶液中存在:c(H+) - c(OH-) = c(M+) + 2c(MOH)
C.a+b的值可能大于14
D.水的电离程度:M>Q
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据列于下表:
元素 | Mn | Fe | |
电离能/( | I1 | 717 | 759 |
I2 | 1509 | 1561 | |
I3 | 3248 | 2957 | |
锰元素位于第四周期第ⅦB族。请写出基态Mn2+的价电子轨道排布图:_________________,比较两元素的I2、I3可知,气态Mn2+再失去1个电子比气态Fe2+再失去1个电子难,对此你的解释是________________________________________________________
(2)下表是第三周期部分元素的电离能[单位:[![]() (电子伏特)]数据。
(电子伏特)]数据。
元素 |
|
|
|
甲 | 5.7 | 47.4 | 71.8 |
乙 | 7.7 | 15.1 | 80.3 |
丙 | 13.0 | 23.9 | 40.0 |
丁 | 15.7 | 27.6 | 40.7 |
下列说法正确的是___________(填序号)。
A.甲的金属性比乙强 B.乙有![]() 价
价
C.丙不可能为非金属元素 D.丁一定为金属元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com