
| A、分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| B、氢气还原氧化铜实验中先通氢气再加热实验结束时应先停止加热,继续通氢气至固体冷却 |
| C、配制浓硫酸与蒸馏水的混合液时,应将浓硫酸慢慢加到蒸馏水中并及时搅拌和冷却 |
| D、用胶头滴管向试管中加入液体时,为防止滴在试管外面,应将滴管尖嘴处伸入试管口中 |


科目:高中化学 来源: 题型:
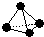 ,已知断裂1mol B-B键吸收167kJ的热量,生成1mol B≡B键放出942kJ热量.试判断相同条件下B4与B2的稳定性顺序是:
,已知断裂1mol B-B键吸收167kJ的热量,生成1mol B≡B键放出942kJ热量.试判断相同条件下B4与B2的稳定性顺序是:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用分液漏斗分离醋酸和水的混合物 |
| B、用酒精萃取碘水中的碘 |
| C、用10mL量筒量取7.5mL稀盐酸 |
| D、用容量瓶配置溶液过程中定容时发现蒸馏水稍微过量,可用胶头滴管吸出少许 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
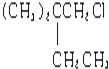 ,B和D分别与强碱的醇溶液共热,都只能得到有机化合物E.以上反应及B的进一步反应如图所示:
,B和D分别与强碱的醇溶液共热,都只能得到有机化合物E.以上反应及B的进一步反应如图所示:
查看答案和解析>>
科目:高中化学 来源: 题型:
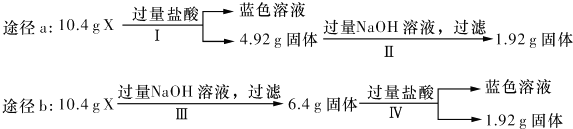
| A、由工可知X中一定存在Fe2 O3、Cu |
| B、无法判断混合物中是否含有Al2O3 |
| C、1.92 g固体成分为Cu |
| D、原混合物中m( Fe2O3):m(Cu)=1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
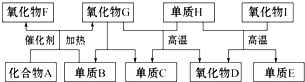
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向0.1 mol?L-1NH4 Cl溶液中通入一定量氨气:c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| B、将醋酸钠、盐酸两溶液混合后,溶液呈中性,则混合后的溶液中:c(Na+)<c(Cl-) |
| C、已知Ka(HF)=7.2×10-4,Ka(HCN)=4.9×10-10,等体积等浓度的NaF、NaCN溶液中,前者离子总数小于后者 |
| D、浓度均为0.1mol?L-l的三种溶液中:①(NH4)2CO3、②(NH4)2 SO4、③(NH4)2Fe(SO4)2,c(NH4+)的大小顺序为:③>②>① |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、③⑤ | B、③④ | C、②④ | D、①③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com