
【题目】运用元素周期律研究元素及其化合物的性质具有重要的意义。
I.部分短周期主族元素的最高价氧化物对应的水化物(浓度均为0.01mol.L-1)溶液的PH和原子序数的关系如下图所示。

(1)元素R在周期表中的位置是 。
(2)元素Y和W形成的Y2W2型化合物中含有化学键的类型为 。
(3)测定Z元素最高价氧化物对应水化物溶液物质的量浓度的方法为 。
II.短周期元素C、O、S能形成多种化合物,如CO2、CS2、COS等
(1)下列能说明碳、硫两种元素非金属性相对强弱的是 (填序号)
A.相同条件下水溶液的PH:Na2CO3>Na2SO4
B.酸性:H2SO3 >H2CO3
C.CS2中碳元素为+4价,硫元素为-2价
(2)羰基硫(COS)可作为一种熏蒸剂,能防止某些昆虫、线虫的危害,其分子结构和CO2相似
①羰基硫(COS)的电子式为: 。
②羰基硫(COS)用氢氧化钠溶液处理及利用的过程如下:

已知A是一种正盐,则A的化学式为 ;若气体a为单质,反应 II的离子方程式为 。
【答案】I.(1)第三周期第ⅦA族
(2)离子键、非极性共价键
(3)酸碱中和滴定
II.(1)ac (2)①![]() ②Na2CO32S2-+5H2O
②Na2CO32S2-+5H2O![]() S2O32-+4H2↑+2OH-
S2O32-+4H2↑+2OH-
【解析】试题分析:I.据题意X、Y、Z、W、R是短周期主族元素且原子序数依次增大,最高价氧化物对应的水化物(浓度均为0.01mol.L-1)溶液的PH,Y对应PH=12,说明Y是钠,X对应PH=2,X是氮,Z对应PH>2,所以 Z 是磷,W对应PH<2,所以W是S;R对应PH=2原子序数最大,所以R是Cl。
(1)元素R在周期表中的位置是:第三周期第ⅦA族。
(2)元素Y和W形成的Y2W2型化合物是Na2S2中含有化学键的类型为:离子键、非极性共价键。
(3)测定Z元素最高价氧化物对应水化物溶液磷酸物质的量浓度的方法为:酸碱中和滴定。
II.(1)A.Na2CO3水解呈碱性,说明H2CO3是弱酸,Na2SO4不水解,H2SO4是强酸,所以H2SO4的酸性强于H2CO3的,则能说明碳与硫两元素非金属性相对强弱关系为:S>C,a正确;B.酸性:H2SO3 >H2CO3,亚硫酸不是最高价含氧酸,不能说明碳与硫两元素非金属性相对强弱,b错误;c、直接说明S的非金属性强于C,所以S才显负价,碳元素显示正价,c正确。
(2)①羰基硫(COS)的电子式为:![]() ;②COS与氢氧化钠反应,根据原子守恒,A溶液应该是含C的正盐,所以是Na2CO3;②据原子守恒,气体a应该是氢气,所以反应为:2S2-+5H2O=S2O32-+4H2+2OH-。
;②COS与氢氧化钠反应,根据原子守恒,A溶液应该是含C的正盐,所以是Na2CO3;②据原子守恒,气体a应该是氢气,所以反应为:2S2-+5H2O=S2O32-+4H2+2OH-。


科目:高中化学 来源: 题型:
【题目】下列条件下,两瓶气体所含原子数一定相等的是( )
A. 同质量、不同密度的N2和CO2 B. 同温度、同体积的H2和N2
C. 同体积、同密度的C2H4和C3H6 D. 同压强、同体积的N2O和CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将铝粉与Fe3O4粉末配制成铝热剂,分成三等份。
①一份直接放入足量的烧碱溶液中,充分反应后放出气体在标准状况下的体积为V1;
②一份在高温下恰好反应完全,反应后的混合物与足量的盐酸反应后,放出的气体在标准状况下的体积为V2;
③一份直接放入足量的盐酸中,充分反应后放出气体在标准状况下的体积为V3。
下列说法正确的是( )
A. V1=V3>V2 B. V2>V1=V3 C. V1=V2>V3 D. V1>V3>V2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学一选修2:化学与技术] 化学是人类进步的关键,化学为人类的生产、生活提供了物质保证。
(1)纯碱是一种重要的化工原料。目前制碱工业主要有“氨碱法”和“联合制碱法”两种工艺。
①“氨碱法”产生大量CaCI2副产品,该工艺中生成CaCI2的化学反应方程式为__
②“联合制碱法”中相关的化学反应方程式为
③CO2是制碱工业的重要原料,请阐述“联合制碱法”与“氨碱法”中C02的来源有何不同 。
(2)铀(U)是核反应最重要的燃料,在核反应中有重要的应用。目前已经研制成功一种螫合型离子交换树脂,它专门吸附海水中的U4+,而不吸附其他元素,其反应原理为___ _(用离子方程式表示,树脂用HR代替,下同),发生离子交换后的离子交换膜用酸处理还可再生,并得到含铀的溶液,其反应原理为 。
(3)钢铁工业对促进经济和社会发展起了重要作用。
①不锈钢中含有的铬元素是在炼钢过程的氧吹 (填“前”或“后”)加入。
②炼钢时,加入硅、锰和铝的目的是____ 。
③炼铁和炼钢生产中,尾气均含有的主要污染物是____ ;从环保和经济角度考虑,上述尾气经处理可用作____ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】孔雀石的主要成分为Cu2(OH)2CO3,还含少量二价铁和三价铁的氧化物及硅的氧化物。以下是实验室以孔雀石为原料制备CuSO4·5H2O晶体的流程图:
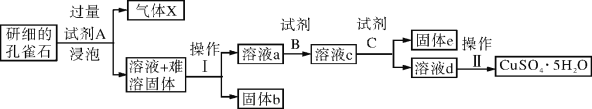
(1)试剂A的化学式是_____________;操作Ⅰ的名称是______________;
(2)生成气体X的化学方程式为:_________________________________。
(3)使用试剂B的目的是将溶液中的Fe2+转化为Fe3+,试剂B最好选用_________
A.酸性KMnO4溶液 B.双氧水 C.浓硝酸 D.氯水
(4)已知:
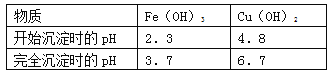
①试剂C的使用是为了调节溶液的pH,使Fe3+转化为沉淀予以分离。试剂C宜选用__________:
A.稀硫酸 B.NaOH溶液 C.氨水 D.CuO
②为完全除去溶液c中的Fe3+而又不使Cu2+沉淀,则应调节溶液pH的范围为__________。
(5)请设计一种实验方案检验溶液中Fe3+是否完全除去(写出操作步骤、现象和结论) ______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中HNO3既表现出酸性又表现出强氧化性的是
A.稀硝酸与CuO反应
B.稀硝酸与NaOH 溶液反应
C.浓硝酸与灼热的碳反应
D.浓硝酸与铜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硫酸钠在印染、造纸等众多行业中有着广泛的应用。研究小组用Na2CO3溶液吸收SO2制备Na2SO3。其实验流程如下:


查阅资料可知,向碳酸钠溶液通入二氧化硫的过程中,溶液中有关组分的质量分数变化如右图是所示。
(1)右图中的线2表示的组分为 (填化学式)。
(2)实验时,“反应II”中加入NaOH溶液的目的是 (用化学方程式表示)。
(3)国家标准规定产品中Na2SO3的质量分数≥97.0%为优等品,≥93.0%为一等品。为了确定实验所得产品的等级,研究小组采用了两种方法进行测定。
①方法I:称取2.570g产品,用蒸馏水溶解,加入足量的双氧水使Na2SO3完全氧化生成Na2SO4,再加入过量的BaCl2溶液,所得沉淀经过过滤、洗涤、干燥后称量,质量为4.660g,通过计算确定产品中Na2SO3的质量分数(写出计算过程)
②方法II:称取1.326g产品,配成100mL溶液,取25.00mL该溶液,滴加0.1250mol/L I2溶液,恰好使Na2SO3完全氧化生成Na2SO4时,消耗I2溶液20.00mL。通过计算确定产品中Na2SO3的质量分数(写出计算过程)
③判断Na2SO3产品的等级,并说明理由。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分。表中所列字母分别代表某一化学元素。

(1)下列 (填写编号)组元素的单质具有良好导电性。
①a、c、m ②b、g、k ③c、h、1 ④d、e、f
(2)电离能主要取决于原子核对核外电子的吸引力和形成稳定结构的倾向。下表是一些气态原子各级电离能的数据(kJ·mol-1):
锂 | X | Y | |
失去一个电子 | 519 | 502 | 580 |
失去二个电子 | 7296 | 4570 | 1820 |
失去三个电子 | 11799 | 6920 | 2750 |
失去四个电子 | 9550 | 11600 |
①为什么锂原子的第二电离能远远大于第一电离能 。
②用电子式表示X和j以原子个数1比1形成的一种化合物 。
③Y在周期表中是 族元素。
④e元素的电子排布式为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用化学知识解决生活中的问题,下列家庭小实验或说法不合理的是
A. 用米汤检验食盐中是否含碘酸钾(KIO3)
B. 用食醋除去暖水瓶中的薄层水垢
C. 医用酒精的浓度通常为75%,可用于杀菌消毒
D. 用灼烧并闻气味的方法区别纯棉织物和纯羊毛织物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com