
【题目】K3[Fe(C2O4)3]· 3H2O(三草酸合铁酸钾晶体)为翠绿色晶体, 溶于水, 难溶于乙醇, 110℃下失去结晶水,230℃分解;是制备负载型活性铁催化剂的主要原料。 实验室利用(NH4)2Fe(SO4)2· 6H2O (硫酸亚铁铵)、H2C2O4(草酸)、K2C2O4(草酸钾)、30%双氧水等为原料制备三草酸合铁酸钾晶体的部分实验过程如下:
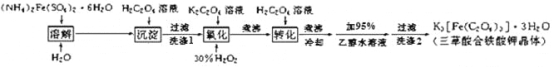
已知:沉淀FeC2O4 · 2H2O 既难溶于水又难溶于强酸
6FeC2O4 + 3H2O2 + 6K2C2O4 = 4K3[Fe(C2O4)3] + 2Fe(OH)3↓
2Fe(OH)3 + 3H2C2O4 + 3K2C2O4 = 2K3[Fe(C2O4)3] + 6H2O
(1)检验硫酸亚铁铵是否变质的试剂是_____;溶解时加几滴稀硫酸的目的是______。
(2)硫酸亚铁铵溶液与 H2C2O4溶液反应生成 FeC2O4 · 2H2O 沉淀,写出该反应方程式_______________;沉淀过滤后,洗涤 1 的操作方法是_______________________________。
(3)在沉淀中加入饱和 K2C2O4 溶液,并用 40 ℃ 左右水浴加热,再向其中慢慢滴加足量的 30% H2O2溶液,不断搅拌。此过程需保持温度在 40 ℃ 左右,可能的原因是_______。加入30%过氧化氢溶液完全反应后,煮沸的目的是______________。
(4)洗涤 2 中所用洗涤试剂最合适的是_______(填选项字母)。
A.草酸钠溶液 B.蒸馏水 C.乙醇 D.KCl溶液
(5)为了不浪费药品,95%乙醇水溶液进行回收的方法是________,所用的主要玻璃仪器有__________(任写两种)等。
【答案】KSCN(或其它合理答案) 抑制Fe2+水解 (NH4)2Fe(SO4)2·6H2O+H2C2O4=FeC2O4·2H2O↓+(NH4)2SO4+H2SO4+4H2O
或(NH4)2Fe(SO4)2·6H2O+H2C2O4=FeC2O4·2H2O↓+2NH4HSO4+4H2O 向过滤器中加入蒸馏水至浸没沉淀,待水自然流下后,重复操作数次 温度太高双氧水容易分解;温度太低反应速率太慢等 除去过量的双氧水 C 蒸馏 蒸馏烧瓶、温度计、冷凝管、牛角管、锥形瓶任写两种
【解析】
(1)引起硫酸亚铁铵变质的原因是Fe2+易被空气中的氧气氧化为Fe3+,所以检验硫酸亚铁铵是否变质只要检验硫酸亚铁铵溶液中是否存在Fe3+,故所用的试剂是KSCN,若加入KSCN溶液后,溶液变为血红色,就证明含有Fe3+,硫酸亚铁铵变质(或亚铁氰化铁K4[Fe(CN)6],Fe3+与K4[Fe(CN)6]反应生成蓝色沉淀,即普鲁士蓝);硫酸亚铁铵是强酸弱碱盐,Fe2+、NH4+容易水解产生Fe(OH)2、NH3·H2O,使溶液变浑浊,溶解时加几滴稀硫酸的目的是为了抑制Fe2+水解。
(2)硫酸亚铁铵溶液与 H2C2O4溶液反应生成 FeC2O4 · 2H2O 沉淀,反应的方程式为:(NH4)2Fe(SO4)2·6H2O +H2C2O4=FeC2O4·2H2O↓+(NH4)2SO4+H2SO4+4H2O或 (NH4)2Fe(SO4)2·6H2O+H2C2O4=FeC2O4·2H2O↓+2NH4HSO4+4H2O;沉淀过滤后,洗涤 1 的操作方法是,向过滤器中加入蒸馏水至浸没沉淀,待水自然流下后,重复操作数次。
(3)在沉淀中加入饱和 K2C2O4 溶液,并用 40 ℃ 左右水浴加热,再向其中慢慢滴加足量的 30% H2O2溶液,不断搅拌,此过程需保持温度在 40 ℃ 左右,可能的原因是:温度过高双氧水容易分解,温度太低反应速率较慢;加入30%过氧化氢溶液完全反应后,煮沸的目的是除去过量的双氧水。
(4)为了减少在洗涤过程中的损失,结合“K3[Fe(C2O4)3]· 3H2O溶于水,难溶于乙醇”,洗涤 2 中所用洗涤试剂最合适的是乙醇,答案选C。
(5)从95%乙醇水溶液中进行回收乙醇的方法是采用蒸馏方法;蒸馏所用的主要玻璃仪器有蒸馏烧瓶、温度计、冷凝管、牛角管、锥形瓶等。


 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化学 来源: 题型:
【题目】某研究小组为了探究一种无机矿物盐![]() 仅含四种元素
仅含四种元素![]() 的组成和性质,设计并完成了如下实验:
的组成和性质,设计并完成了如下实验: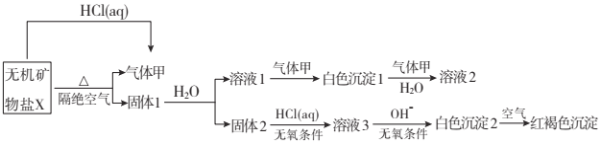
另取![]() 在惰性气流中加热至完全分解,得到
在惰性气流中加热至完全分解,得到![]() 固体1。请回答如下问题:
固体1。请回答如下问题:
(1)画出白色沉淀1中金属元素的原子结构示意图__________,写出气体甲的电子式 __________。
(2)![]() 的化学式是__________,在惰性气流中加热X至完全分解的化学反应方程式为__________.
的化学式是__________,在惰性气流中加热X至完全分解的化学反应方程式为__________.
(3)白色沉淀2在空气中变成红褐色沉淀的原因是__________![]() 用化学反应方程式表示
用化学反应方程式表示![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气是一种重要的工业原料,液氯储存区贴有的说明卡如下:
包装 | 钢瓶 |
储运要求 | 远离金属粉末、氨、烃类、醇类物质;设置氯气检测仪 |
泄漏处理 | NaOH、NaHSO3溶液吸收 |
下列解释事实的方程式不正确的是
A. 氯气用于自来水消毒:Cl2 + H2O![]() 2H+ + Cl-+ ClO-
2H+ + Cl-+ ClO-
B. 电解饱和食盐水制取Cl2:2Cl- +2H2O![]() 2OH-+ H2↑+Cl2↑
2OH-+ H2↑+Cl2↑
C. 浓氨水检验泄露的氯气,产生白烟:8NH3 + 3Cl2 === 6 NH4Cl + N2
D. 氯气“泄漏处理”中NaHSO3溶液的作用:HSO3-+ Cl2 + H2O === SO42-+ 3H+ + 2Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Aminolevulinic acid是一种新型小分子药物,其结构为![]() ,下列说法错误的是( )
,下列说法错误的是( )
A. Aminolevulinic acid 的分子式是C5H7NO3
B. lmol该分子最多只能与lmol氢气发生加成反应
C. Aminolevulinic acid能发生氧化反应、还原反应和取代反应
D. Aminolevulinic acid分子中含有四种官能团
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列短周期元素的数据(已知Be的原子半径为0.089nm):
① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
原子半径 (nm) | 0.074 | 0.160 | 0.152 | 0.110 | 0.099 | 0.186 | 0.075 | 0.082 |
最高正化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
最低负化合价 | 2 | 3 | 1 | 3 |
(1)⑧号元素的在周期表中的位置是________________;上述元素处于同一主族的有_________________。(用元素符号表示)
(2)上表中某两种元素形成的共价化合物中,每个原子都满足最外层为8电子的稳定结构,写出其电子式:_________________________(任写一种)。
(3)元素①和⑥能形成两种化合物,写出其中较稳定的化合物与水反应的离子方程式_____________________________________________________。
(4)含锂材料在社会中广泛应用,如各种储氢材料(Li2NH等)、便携式电源材料(LiCoO2等)。根据下列要求回答问题:
![]() 和
和![]() 作核反应堆最佳热载体,
作核反应堆最佳热载体,![]() 和
和![]() 用作高温堆减速剂。下列说法正确的是________。
用作高温堆减速剂。下列说法正确的是________。
A.![]() 和
和![]() 互为同位素B.
互为同位素B.![]() 和
和![]() 属于同种核素
属于同种核素
C.![]() 和
和![]() 的化学性质不同D.
的化学性质不同D.![]() 和
和![]() 是同种物质
是同种物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用多孔石墨电极完成下列实验:
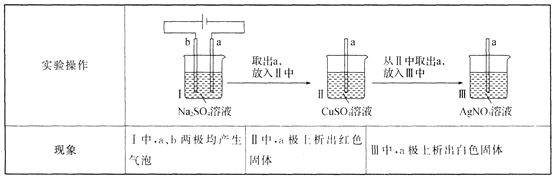
下列对实验现象的解释或推测不合理的是 ( )
A.I中,b极反应:2H2O-4e-=== O2↑+4 H+
B.Ⅱ中,析出红色固体:Cu2++H2 === Cu+2H+
C.Ⅲ中,只可能发生反应:2Ag++Cu === Cu2++2Ag
D.I中,a极上既发生了化学过程,也发生了物理过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表中,除了22种非金属元素外,其余的都是金属,请根据元素周期表回答下列问题:
I.(1)基态氮原子核外共有_______种运动状态不相同的电子,该原子核外电子排布中电子在能量最低的轨道呈_______形,用n表示能层,氟元素所在族的外围电子排布式为______________。
(2)在元素周期表中,某些主族元素与下方的主族元素的性质有些相似,被称为“对角线规则”,如下表:

根据“对角线规则”写出Be(OH)2与NaOH反应的离子方程式______________,硼酸(H3BO3)是一种具有片层结构的白色晶体,层内的H3BO3分子间通过氢键相连(如图)。含1mol H3BO3的晶体中有__________mol氢键,H3BO3中B原子的杂化类型为_____________。

(3)以第二周期为例,除Be、N外,其它元素的第一电离能从左到右逐渐增大的原因是____________________________________________________。
II.近年来铁及其化合物在工农业中有广阔的应用前景。
(4)铁的一种络离子[Fe(CN)6]4-中Fe2+的配位数为6,该络离子中不存在______(填序号)。
A.共价键 B.非极性键 C.配位键 D.δ键 E.π键
(5)AlCl3的熔点比NaCl熔点低的原因是____________________________________。
(6)一种Al-Fe合金的立体晶胞如图所示。若晶体的密度为ρ gcm-3,则此合金中最近的两个Fe原子之间的距离为__________cm(用含ρ的代数式表示)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】连二次硝酸(H2N2O2)是一种二元酸,可用于制N2O气体。
(1)常温下,用0.01mol/L的NaOH溶液滴定10mL0.01mol/L的H2N2O2溶液,测得溶液pH与NaOH溶液体积的关系如图所示。
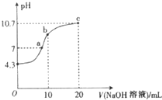
c点时溶液中各离子浓度由大到小的顺序为___;
②b点时溶液中c(N2O22-)___c(H2N2O2)(填“>”“<”或“=”);
(2)硝酸银溶液和连二次硝酸钠溶液混合,可以得到黄色的连二次硝酸银沉淀,向该分散系中滴加硫酸钠溶液,当白色沉淀和黄色沉淀共存时,分散系中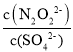 =___。
=___。
[已知KSP(Ag2SO4)=1.4×10-5、KSP(Ag2N2O2)=5.6×10-9 ]。
(3)常温下,向b mol/L醋酸钠溶液中滴加等体积的amol/L的盐酸,使溶液恰好呈中性,则醋酸的电离平衡常数=___(用含a、b的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法正确的是( )
A.苯佐卡因(![]() )是局部麻醉药,分子中含有2种官能团,分子式为C9H10NO2
)是局部麻醉药,分子中含有2种官能团,分子式为C9H10NO2
B.香叶醇(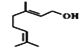 )能发生加成反应不能发生取代反应
)能发生加成反应不能发生取代反应
C.某有机物的分子式为C4H8,能使溴的CCl4溶液褪色,则它在一定条件下与水反应时最多可生成的有机物(不考虑立体异构)有4种
D.青蒿素(![]() )的一氯代物有5种(不含立体异构)
)的一氯代物有5种(不含立体异构)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com