
【题目】连二次硝酸(H2N2O2)是一种二元酸,可用于制N2O气体。
(1)常温下,用0.01mol/L的NaOH溶液滴定10mL0.01mol/L的H2N2O2溶液,测得溶液pH与NaOH溶液体积的关系如图所示。
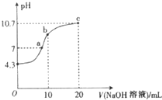
c点时溶液中各离子浓度由大到小的顺序为___;
②b点时溶液中c(N2O22-)___c(H2N2O2)(填“>”“<”或“=”);
(2)硝酸银溶液和连二次硝酸钠溶液混合,可以得到黄色的连二次硝酸银沉淀,向该分散系中滴加硫酸钠溶液,当白色沉淀和黄色沉淀共存时,分散系中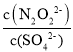 =___。
=___。
[已知KSP(Ag2SO4)=1.4×10-5、KSP(Ag2N2O2)=5.6×10-9 ]。
(3)常温下,向b mol/L醋酸钠溶液中滴加等体积的amol/L的盐酸,使溶液恰好呈中性,则醋酸的电离平衡常数=___(用含a、b的代数式表示)
【答案】c(Na+)>c(N2O22-)>c(OH-)>c(HN2O2-)>c(H+) < 4×10-4 ![]()
【解析】
硝酸银溶液和连二次硝酸钠溶液混合,可以得到黄色的连二次硝酸银沉淀,向该分散系中滴加硫酸钠溶液,当白色沉淀和黄色沉淀共存时, Ag2SO4![]() 2Ag++SO42- ,Ag2N2O2
2Ag++SO42- ,Ag2N2O2![]() 2Ag++N2O22-同时达到平衡,溶液中的Ag+浓度相等,分散系中
2Ag++N2O22-同时达到平衡,溶液中的Ag+浓度相等,分散系中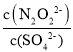 也就是Ag2SO4、Ag2N2O2的溶度积常数之比。
也就是Ag2SO4、Ag2N2O2的溶度积常数之比。
(1)c点时,NaOH与H2N2O2恰好完全反应,生成Na2N2O2和H2O,
在溶液中存在下列转化:
Na2N2O2=2Na++ N2O22-,
N2O22-+H2O![]() HN2O2-+OH-,
HN2O2-+OH-,
HN2O2-+H2O![]() H2N2O2+OH-,
H2N2O2+OH-,
H2O![]() H++OH-
H++OH-
并且转化的趋势依次减小,从而得出各离子浓度由大到小的顺序为
c(Na+)>c(N2O22-)>c(OH-)>c(HN2O2-)>c(H+),
答案为:c(Na+)>c(N2O22-)>c(OH-)>c(HN2O2-)>c(H+);
②b点时,刚好等摩反应,生成HN2O2-和水,从图中可以看出,此时溶液呈碱性,说明HN2O2-水解趋势大于电离趋势,从而得出溶液中c(N2O22-)<c(H2N2O2),
答案为:<。
(2)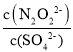 =
=![]() ,
,
答案为:4×10-4。
(3)常温下,向b mol/L醋酸钠溶液中滴加等体积的amol/L的盐酸,使溶液恰好呈中性,溶质为醋酸钠和醋酸,所以醋酸钠和盐酸的反应中,醋酸钠是过量的,生成的醋酸的物质的量和HCl的物质的量相等。假设醋酸钠溶液和盐酸的体积均为1L,则生成的醋酸的物质的量为amol,剩余的醋酸钠的物质的量为(b-a)mol,溶液呈中性,所以c(H+)=10-7mol/L,根据电离平衡常数表达式K=![]() ,
,
答案为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G七种短周期元素的原子序数依次增大,其中仅有一种稀有气体元素。A和E最外层电子数相同,短周期主族元素的原子中,A 原子的半径最小,E元素焰色反应颜色为黄色;B、C、F和G在周期表中相邻,B、C同周期,F、G同周期C、F同主族, C元素是地壳中含量最多的元素;A和C可形成两种常见的液态化合物X和Y(相对分子质量X<Y),D形成的分子为单原子分子。回答问题:
(1)G元素为______(填元素符号), Y的电子式为_______________。
(2)液态化合物Y与稀H2SO4酸化的K2Cr2O7溶液作用可产生一种无色助燃性气体及可溶性的Cr2(SO4)3,则该反应的离子方程式为______________________________________。
(3)用某种金属易拉罐与A、C、E组成的化合物的水溶液反应,产生的气体可充填气球,请写出该反应的离子方程式____________,使用这种气球存在的隐患是________________。
(4)P和Q两种物质都是由A、C、E、F四种元素组成的盐,其水溶液都显酸性,等物质的量的P和Q恰好完全反应。写出该反应的离子方程式:_________________________,这两种盐均含有的化学键类型为________________________。
(5)由A、B两元素形成的化合物W可作为火箭推进器中的强还原剂,已知一个W分子和一个Y分子中都含有18个电子,0.5mol液态W和足量液态Y反应,生成一种无色无味无毒的气体B2和液态X。写出该反应的化学方程式为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】K3[Fe(C2O4)3]· 3H2O(三草酸合铁酸钾晶体)为翠绿色晶体, 溶于水, 难溶于乙醇, 110℃下失去结晶水,230℃分解;是制备负载型活性铁催化剂的主要原料。 实验室利用(NH4)2Fe(SO4)2· 6H2O (硫酸亚铁铵)、H2C2O4(草酸)、K2C2O4(草酸钾)、30%双氧水等为原料制备三草酸合铁酸钾晶体的部分实验过程如下:
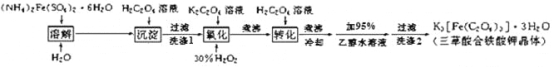
已知:沉淀FeC2O4 · 2H2O 既难溶于水又难溶于强酸
6FeC2O4 + 3H2O2 + 6K2C2O4 = 4K3[Fe(C2O4)3] + 2Fe(OH)3↓
2Fe(OH)3 + 3H2C2O4 + 3K2C2O4 = 2K3[Fe(C2O4)3] + 6H2O
(1)检验硫酸亚铁铵是否变质的试剂是_____;溶解时加几滴稀硫酸的目的是______。
(2)硫酸亚铁铵溶液与 H2C2O4溶液反应生成 FeC2O4 · 2H2O 沉淀,写出该反应方程式_______________;沉淀过滤后,洗涤 1 的操作方法是_______________________________。
(3)在沉淀中加入饱和 K2C2O4 溶液,并用 40 ℃ 左右水浴加热,再向其中慢慢滴加足量的 30% H2O2溶液,不断搅拌。此过程需保持温度在 40 ℃ 左右,可能的原因是_______。加入30%过氧化氢溶液完全反应后,煮沸的目的是______________。
(4)洗涤 2 中所用洗涤试剂最合适的是_______(填选项字母)。
A.草酸钠溶液 B.蒸馏水 C.乙醇 D.KCl溶液
(5)为了不浪费药品,95%乙醇水溶液进行回收的方法是________,所用的主要玻璃仪器有__________(任写两种)等。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用食用油进行实验,以下是实验操作和现象:
实验操作 | 将食用油滴入水中 | 向食用油中滴加溴水 | 将少量食用油与纯碱(主要成分是 |
实验现象 | 食用油浮在水面上 | 溴水褪色 | 分层现象消失 |
下列关于食用油的实验结论不正确的是( )
A.食用油的密度比水小
B.食用油中含碳碳不饱和键
C.食用油在碱性条件下会水解生成可溶于水的物质
D.食用油是一种有机酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法不正确的是
A.一定条件下,合成氨反应中有0.5molN2发生反应,则反应中转移电子数为3NA
B.10克环己烷与2-丙醇的混合液中,碳元素的质量分数为72%,则其中所含的氧原子数目为![]() NA
NA
C.12g石墨中含有3NA个C-C共价键
D.常温常压下有28g单晶硅晶体,则其中所含的Si﹣Si键数目为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳族元素及其化合物广泛存在于自然界中,请回答下列问题:
Ⅰ![]() 锗
锗![]() 是典型的半导体元素,在电子、材料等领域应用广泛。
是典型的半导体元素,在电子、材料等领域应用广泛。
![]() 基态Ge原子的核外电子排布式为
基态Ge原子的核外电子排布式为![]() ______。
______。
![]() 与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。从原子结构角度分析,原因可能是______。
与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。从原子结构角度分析,原因可能是______。
![]() 比较下表中锗卤化物的熔点和沸点,分析其变化规律及原因
比较下表中锗卤化物的熔点和沸点,分析其变化规律及原因
|
|
| |
熔点 |
| 26 | 146 |
沸点 |
| 186 | 约400 |
![]() 光催化还原
光催化还原![]() 制备
制备![]() 的反应中,带状纳米
的反应中,带状纳米![]() 是该反应的良好催化剂。Zn、Ge、O的电负性由大至小的顺序是______。Ⅱ
是该反应的良好催化剂。Zn、Ge、O的电负性由大至小的顺序是______。Ⅱ![]() 碳元素的単质有多种形式,其化合物在电子、材料等领域亦应用广泛。
碳元素的単质有多种形式,其化合物在电子、材料等领域亦应用广泛。
![]() 下图所示依次是
下图所示依次是![]() 、石墨和金刚石的结构图。金刚石、石墨烯
、石墨和金刚石的结构图。金刚石、石墨烯![]() 指单层石墨
指单层石墨![]() 中碳原子的杂化形式分别为______、______。
中碳原子的杂化形式分别为______、______。
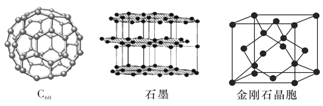
![]() 属于______晶体,石墨属于______晶体。
属于______晶体,石墨属于______晶体。
![]() 一种含碳磁性材料的单晶胞结构如图所示。
一种含碳磁性材料的单晶胞结构如图所示。
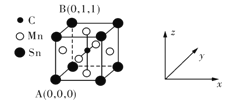
![]() 原子坐标参数表示晶胞内部各原子的相对位置。上图所示晶胞结构中A的原子坐标参数为
原子坐标参数表示晶胞内部各原子的相对位置。上图所示晶胞结构中A的原子坐标参数为![]() 0,
0,![]() ,B为
,B为![]() 1,
1,![]() ,则该晶胞中碳原子的原子坐标为______。
,则该晶胞中碳原子的原子坐标为______。
![]() 在晶体中的堆积方式为______
在晶体中的堆积方式为______![]() 填“简单立方”“体心立方”“面心立方最密”或”六方最密”
填“简单立方”“体心立方”“面心立方最密”或”六方最密”![]() 堆积。
堆积。
![]() 若该晶胞的边长为apm,
若该晶胞的边长为apm,![]() 表示阿伏加德罗常数的值,则该晶体密度的表达式为______。
表示阿伏加德罗常数的值,则该晶体密度的表达式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图是一种检验某气体化学性质的实验装置,图中B为开关。 如先打开B,在A处通入干燥氯气,C中红色布条颜色无变化;当关闭B时,C处红色布条颜色褪去。则D瓶中盛有的溶液是( )
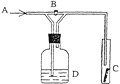
A.浓H2SO4 B.饱和食盐水C.浓NaOH溶液D.KI溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳、氧、氮、镁、铬、铁、锌是几种重要的元素,请回答下列问题:
![]() 铝的基态原子的价电子排布式是_________________。
铝的基态原子的价电子排布式是_________________。
![]() 用水解法制备一种磁性材料铁氧体时常加入尿素
用水解法制备一种磁性材料铁氧体时常加入尿素![]() 、醋酸钠等碱性物质。尿素分子中所含非金属元素的电负性由大到小的顺序是_________,分子中
、醋酸钠等碱性物质。尿素分子中所含非金属元素的电负性由大到小的顺序是_________,分子中![]() 键和
键和![]() 键的数目之比为__________。醋酸钠中碳原子的杂化类型为____________。
键的数目之比为__________。醋酸钠中碳原子的杂化类型为____________。
![]() 、
、![]() 等金属离子与
等金属离子与![]() 、
、![]() 能形成稳定金属配离子,其中形成的化合物稳定性相对较高的是__________
能形成稳定金属配离子,其中形成的化合物稳定性相对较高的是__________![]() 填“
填“![]() ”或“
”或“![]() ”
”![]() ,其原因是__________;已知氨
,其原因是__________;已知氨![]() 熔点:
熔点:![]() 、沸点:
、沸点:![]() ,联氨
,联氨![]() 熔点:
熔点:![]() 、沸点:
、沸点:![]() ,解释其熔沸点高低的主要原因:______________。
,解释其熔沸点高低的主要原因:______________。
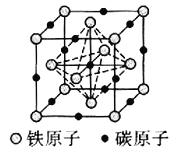
![]() 碳溶解在
碳溶解在![]() 中形成的一种间隙固溶体,无磁性,其晶胞为面心立方结构,如图所示,则该物质的化学式为__________。若晶体密度为
中形成的一种间隙固溶体,无磁性,其晶胞为面心立方结构,如图所示,则该物质的化学式为__________。若晶体密度为![]() ,则晶胞中最近的两个碳原子的距离为__________
,则晶胞中最近的两个碳原子的距离为__________![]() 阿伏加德罗常数的值用
阿伏加德罗常数的值用![]() 表示,写出简化后的计算式即可
表示,写出简化后的计算式即可![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置符合实验目的是( )
目的 | 粗铜的精炼 | 验证NaCl溶液(含酚酞)的产物 | 在铁制品上镀铜 | 构成原电池 |
装置 |
|
|
|
|
选项 | A | B | C | D |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com