
【题目】用下列实验装置进行相应的实验,能达到实验目的的是
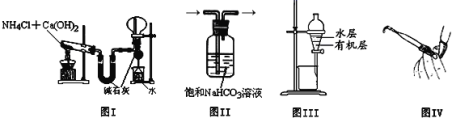
A.图I用于实验室制氨气并收集干燥的氨气
B.图II用于除去Cl2中含有的少量HCl
C.图III用于提取I2的CCl4溶液中的I2
D.图IV用于检查碱式滴定管是否漏液
【答案】A
【解析】
A.固体氢氧化钙和氯化铵共热反应生成氯化钙和水和氨气,氨气为碱性气体,用碱石灰干燥,氨气的密度比空气小,用向下排空气法收集,多余的氨气用水吸收,以防污染空气,吸收氨气时,用碱石灰防水蒸气进入烧瓶,为防止倒吸,在干燥管下端接一个倒扣漏斗, A正确;
B.氯气能和碳酸氢钠溶液反应,应用饱和NaCl溶液,B错误;
C.碘和四氯化碳溶液互溶,不能用分液的方法分离,提取I2的CCl4溶液中的I2应用蒸馏,C错误;
D.“碱式滴定管检查是否漏液的方法:向滴定管内注满清水,观察是否有液体从滴定管的尖嘴出漏出,如有则滴定管漏液,若无则滴定管没有漏液,图IV为排碱式滴定管气泡,D错误。
答案选A。


科目:高中化学 来源: 题型:
【题目】现使用酸碱中和滴定法测定市售白醋的总酸量 (g/100mL )。
I.实验步骤:
(1)用_____ (填仪器名称 )量取10.00mL 食用白醋,在_____ (填仪器名称 )中用水稀释后转移到100mL_____ (填仪器名称 )中定容,摇匀即得待测白醋溶液。
(2)用_____色手柄滴定管取待测白醋溶液 20.00mL 于锥形瓶中,向其中滴加2滴_____作为指示剂。
(3)读取盛装0.1000mol/L NaOH 溶液的滴定管的初始读数。如果液面位置如图所示 则此时的读数为_____mL。
![]()
(4)滴定。当_____时,停止滴定,并记录 NaOH溶液的终读数,重复滴定 3 次。
II.实验记录
滴定次数 实验数据 (mL ) | 1 | 2 | 3 | 4 |
V (样品 ) | 20.00 | 20.00 | 20.00 | 20.00 |
V (NaOH ) (消耗 ) | 15.95 | 15.00 | 15.05 | 14.95 |
(5)甲同学在处理数据时计算得平均消耗的NaOH溶液的体积为:V= (15.95+15.00+15.05+14.95 )/4=15.24(mL)。指出他的计算的不合理之处:_____。 按正确数据处理,可得c (市售白醋)=_____mol/L。
(6)在本实验的滴定过程中,下列操作会使实验结果偏大的是_____ (填写序号)
a.盛装NaOH的滴定管在滴定时未用标准NaOH溶液润洗
b.盛装待测白醋的滴定管的尖嘴在滴定前有气泡,滴定后气泡消失
c.锥形瓶中加入待测白醋溶液后,再加少量水
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中,实验操作、装置、现象及结论都正确的是
选项 | 实验操作或装置 | 实验现象 | 相关解释及结论 |
A. | 用两支试管各取5 mL 0.1 mol·L-1酸性KMnO4溶液,分别加入2 mL 0.1 mol·L-1和0.2 mol·L-1 H2C2O4溶液 | 两试管溶液均褪色,且加0.2 mol·L-1H2C2O4的试管中褪色更快 | 其他条件不变,H2C2O4浓度越大,化学反应速率越大 |
B. |
| 左球气体颜色加深,右球气体颜色变浅 | 勒夏特列原理 |
C. | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 熔化后的液态铝滴落下来 | 金属铝的熔点较低 |
D. |
| 饱和Na2CO3溶液上有透明的不溶于水的油状液体产生 | 乙酸乙酯难溶于水 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制造太阳能电池需要高纯度的硅,工业上制取高纯度硅常用以下反应实现:
①Si(s)+3HCl(g)![]() SiHCl3(g)+H2(g)
SiHCl3(g)+H2(g)
②SiHCl3(g)+H2(g)![]() Si(s)+3HCl(g)
Si(s)+3HCl(g)
对以上两个反应的下列叙述错误的是( )
A.两个反应都是置换反应
B.反应①所需粗硅可通过反应:SiO2+2C![]() Si+2CO↑来制备
Si+2CO↑来制备
C.两个反应都是氧化还原反应
D.两个反应互为可逆反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别按下图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中A为电流表。请回答下列问题:
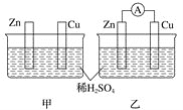
(1)以下叙述中,正确的是_______________(填字母)。
A.甲中锌片是负极,乙中铜片是正极
B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液pH均增大
D.产生气泡的速度甲中比乙中慢
E.乙的外电路中电流方向Zn→Cu
F.乙溶液中![]() 向铜片方向移动
向铜片方向移动
(2)变化过程中能量转化的主要形式:甲为___________;乙为______。
(3)在乙实验中,某同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是___。
(4)在乙实验中,如果把硫酸换成硫酸铜溶液,请写出铜电极的电极反应方程式及总反应离子方程式:铜电极:____,总反应:___。当电路中转移0.25 mol电子时,消耗负极材料的质量为_____g(Zn的相对原子质量65)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将气体A、B置于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g)2C(g)+2D(g),反应进行到10 s末,达到平衡,测得A的物质的量为1.8 mol,B的物质的量为0.6 mol,C的物质的量为0.8 mol。
(1)用C表示10 s内反应的平均反应速率为________。
(2)反应前A的物质的量浓度是________。
(3)10 s末,生成物D的浓度为________。
(4)A与B的平衡转化率之比为________。
(5)反应过程中容器内气体的平均相对分子质量变化是________(填“增大”、“减小”或“不变”,下同),气体的密度变化是________。
(6)平衡后,若改变下列条件,生成D的速率如何变化(填“增大”、“减小”或“不变”):①降低温度______;②增大A的浓度________;③恒容下充入氖气_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活、生产、科技关系密切,下列说法中正确的是( )
A.“碳海绵”吸收泄漏的原油时发生了化学变化
B.“玉兔二号”月球车首次实现在月球背面着陆,其帆板太阳能电池的材料是二氧化硅
C.“嫘祖栽桑蚕吐丝,抽丝织作绣神奇”中的“丝”不耐酸碱
D.氢燃料电池中使用的储氢材料,如稀土类![]() 等合金材料是纯净物
等合金材料是纯净物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢铁占世界钢铁年产量的四分之一。
请回答钢铁在腐蚀、防护过程中的有关问题。
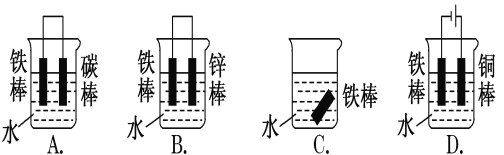
(1)下列哪些装置不能防止铁棒被腐蚀________________;
(2)实际生产可在铁件的表面镀铜防止铁被腐蚀.装置示意图如图.请回答:
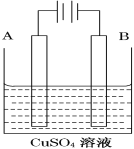
①B电极对应的金属是________(写元素名称),
A电极的电极反应式是___________________。
②镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中,一定条件下发生反应:2A(?) ![]() B(g)+2C(g),且达到平衡。当升高温度时气体的密度增大,则下列叙述中正确的是 ( )
B(g)+2C(g),且达到平衡。当升高温度时气体的密度增大,则下列叙述中正确的是 ( )
A.升高温度,正反应速率增大,逆反应速率减小B.若正反应是放热反应,则A为气态
C.物质A一定为非气态,且正反应是吸热反应D.若向容器中充入惰性气体,则平衡向左移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com