
科目: 来源: 题型:
【题目】“飘尘”是物质燃烧时产生的粒状漂浮物,颗粒很小(直径小于10-7m),不易沉降(可漂浮数小时甚至数年),它与空气中的SO2、O2接触时,SO2会转化为SO3,使空气酸度增加。飘尘所起的主要作用与下列变化中硫酸的作用相同的是( )
A. 氯气除杂过程中通入浓硫酸中 B. 浓硫酸与木炭共热
C. 乙酸乙酯与稀硫酸共热 D. 浓硫酸可以用铝槽车运输
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关物质的性质与用途具有对应关系的是 ( )
A.SO2具有还原性,可用于漂白纸浆
B.NH4HCO3受热易分解,可用作氮肥
C.氢氧化铝具有弱碱性,可用作净水剂
D.常温下铁能被浓硝酸钝化,可用铁质容器贮运浓硝酸
查看答案和解析>>
科目: 来源: 题型:
【题目】[化学—选修3:物质结构与性质]四川含有丰富的矿产资源,钒矿、钛矿、黄铁矿等七种矿产储量位居全国第1位。回答下列问题:
(1)V2O5常用作SO2 转化为SO3的催化剂。SO2 分子中键角 120°(填“>”、“<”或“=”);SO3分子中S原子的杂化轨道类型为 ;V2O5 溶解在NaOH溶液中,可得到钒酸钠(Na3VO4),该盐阴离子的立体构型为 。
(2)VO2+在酸性条件下可被草酸(H2C2O4)还原为VO2+,草酸被氧化为CO2,该反应用于钒含量的测定。写出反应的离子方程式 。
(3)钛在元素周期表中的位置为 ,其电子排布式为 。用乙醚从TiCl3的饱和溶液中萃取可得TiCl3·6H2O绿色晶体,其配位数为6,将1mol该晶体加入到足量硝酸银溶液中可得2mol白色沉淀,则该配合物的化学式是 。
(4)科学家通过X射线探明,黄铁矿(FeS2)的晶体结构与NaCl的晶体结构相似,若在FeS2晶体中阴阳离子间最近距离为a cm,阿伏伽德罗常数为NA。则晶体密度表达式为 g/cm3。
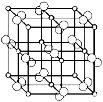
查看答案和解析>>
科目: 来源: 题型:
【题目】电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛。
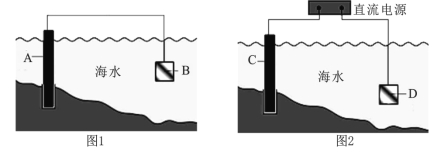
(1)图1中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择 (填字母序号)。
a.碳棒 b.锌板 c.铜板
该电化学保护方法的名称是 。
(2)图2中,钢闸门C为 极,用氯化钠溶液模拟海水进行实验,D为石墨块,总反应的离子方程式为 。
(3)有关上述实验,下列说法正确的是 。
A.溶液中Na+向D极移动
B.从D极处逸出的气体能使湿润的KI淀粉试纸变蓝
C.反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
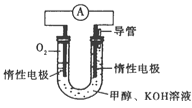
(4)模拟工业上离子交换膜法制烧碱的方法,可用如图装置电解硫酸钾溶液来制取H2、O2、H2SO4和KOH。
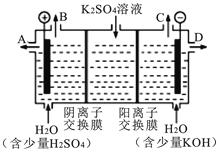
①该电解槽的阳极反应方程式为 。 此时通过阴离子交换膜的离子数 (填“大于”“小于”或“等于”)通过阳离子交换膜的离子数。
②制得的氢氧化钾溶液从出口(填“A”、“B”、“C”或 “D”) 导出。
③若采用CH4燃料电池(石墨为电极,KOH为电解质溶液)为电源,则该电池的负极电极方程式为 ,若B极产生标准状况下22.4 L气体,则理论上需要通入 mol CH4。
④电解过程中阴极区碱性明显增强,用平衡移动原理解释原因 。
查看答案和解析>>
科目: 来源: 题型:
【题目】低碳经济是以低能耗、低污染、低排放为基础的经济模式,低碳循环正成为科学家研究 的主要课题。最近有科学家提出构想:把空气吹 入饱和碳酸钾溶液,然后再把CO2从溶液中提取 出来,经化学反应后使之变为可再生燃料甲醇。 该构想技术流程如下:
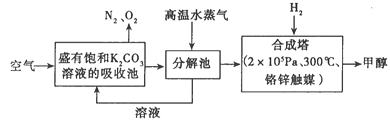
(1)向分解池中通入高温水蒸气的作用是________________。
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) △H=-1275.6 kJ·mol-1
②2CO(g)+O2(g)=2CO2(g) △H=-566.0 kJ·mol-1
③H2O(g)=H2O(l) △H=-44.0 kJ·mol-1
则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为______________。
(3)依据甲醇燃烧的反应原理。设计如右图所示的电池装置。该装置负极的电极反应式为____________。
(4)已知Ksp(CaCO3)=2.8×10-9mol2·L-2.现将CaCl2溶液与0.02 mol·L-1Na2CO3溶液等体积混合,生成CaCO3沉淀时,所需CaCl2溶液的最小物质的量浓度为_____________。
(5)CO(g)和H2O(g)在一定条件下反应可得到清洁燃料H2。将不同量的CO(g)和H2O(g)分别通入到体积为2 L的恒容密闭容器中发生反应:CO(g)+H2O(g)=CO2(g)+H2(g),不同温度下得到三组数据:
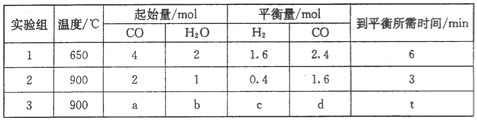
①实验1前6 min的反应速率v(CO2)=___________(保留小数点后两位,下同)。
②实验2条件下平衡常数K=_____________。
③该反应的△H____________0 (填“<”或“>”=。)
④实验3中,若平衡时的转化率α(CO)>α(H2O),则a/b的取值范围是_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组离子在溶液中能够大量共存的是
A.NH4+、Ca2+、OH-、HCO3- B.NH4+、Br-、Na+、SO42-
C.Ag+、H+、SO32-、ClO- D.H+、Cl-、Fe2+、NO3-
查看答案和解析>>
科目: 来源: 题型:
【题目】【化学—选修5:有机化学基础】
有机化合物X、Y、A、B、C、D、E、F、G之间的转化关系如下图。
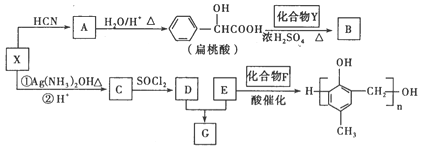
已知以下信息:
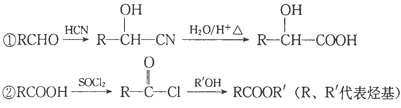
③X在催化剂作用下可与H2反应生成化合物Y。
④化合物F的核磁共振氢谱图中只有一个吸收峰。
回答下列问题:
(1)X的含氧官能团的名称是________,X与HCN反应生成A的反应类型是_________。
(2)酯类化合物B的分子式是C15H14O3,其结构简式是_____________。
(3)X发生银镜反应的化学方程式是______________________。
(4)G在NaOH溶液中发生水解反应的化学方程式是__________________。
(5)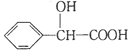 的同分异构体中:①能发生水解反应;②能发生银镜反应;
的同分异构体中:①能发生水解反应;②能发生银镜反应;
③能与氯化铁溶液发生显色反应;④含氧官能团处在对位。满足上述条件的同分异构体共有________种(不考虑立体异构),写出核磁共振氢谱图中有五个吸收峰的同分异构体的结构简式__________________。
(6)写出以C2H5OH为原料合成乳酸(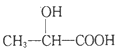 )的路线(其它试剂任选)。(合成路线常用的表示方式为:A
)的路线(其它试剂任选)。(合成路线常用的表示方式为:A![]() B……
B……![]() 目标产物)
目标产物)
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃时,有c(CH3COOH)+c(CH3COO-)=0.1 mol·L-1的一组醋酸、醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-)与pH的关系如图所示。下列有关溶液中离子浓度关系的叙述不正确的是

A.由题给图示可求出25℃时醋酸的电离平衡常 数Ka=10-4.75
B.W点所表示的溶液中:c(Na+)+c(H+) =c(CH3COOH)+c(OH-)
C.pH=3.5的溶液中:c(Na+)+c(H+)-c(OH-)+c(CH3COOH)=0.1 mol·L-1
D.向W点所表示的1.0L溶液中通入0.05mol HCl气体(溶液体积变化可忽略):c(H+) = c(CH3COOH) + c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com