
科目: 来源: 题型:
【题目】下列与有机物的结构、性质有关的叙述正确的是( )
A.苯、油脂均不能使酸性KMnO4溶液褪色
B.甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应
C.葡萄糖、果糖的分子式均为C6 H12O6,二者互为同分异构体
D.乙醇、乙酸均能与Na反应放出H2,二者分子中官能团相同
查看答案和解析>>
科目: 来源: 题型:
【题目】已知4NH3+5O2=4NO+6H2O ,若反应速率分别用V(NH3)、 V(O2)、V(NO)、V(H2O)表示,则正确的关系是
A. ![]() V(NH3)=V(O2) B.
V(NH3)=V(O2) B. ![]() V(O2)=V(H2O)
V(O2)=V(H2O)
C. ![]() V(NH3)=V(H2O) D.
V(NH3)=V(H2O) D. ![]() V(O2)=V(NO)
V(O2)=V(NO)
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学设计如下方案,以分离KCl和BaCl2两种固体混合物,试回答问题:
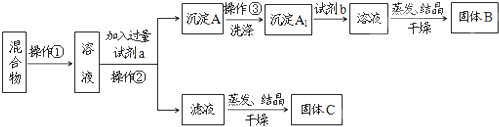
(1)操作①的名称是 ,操作②的名称是 。
(2)试剂a是 ,试剂b是 ,固体B是 。(填化学式)
(3)加入试剂b所发生的化学反应方程式为: 。
(4)该方案是否达到实验目的: (填“是”或“否”)。若不能,应如何改进(若能,此问不用回答 。
(5)若要测定原混合物中KCl和BaCl2的质量分数,除了要准确称量混合物的质量外,至少还要获得的数据是 (填“A”、“A1”、“B”、“C”)的质量。
查看答案和解析>>
科目: 来源: 题型:
【题目】在恒温恒压下,向密闭容器中充入4 mol SO2和2 mol O2,发生反应2SO2(g)+O2(g) ![]() 2SO3(g) ΔH<0。2 min后,反应达到平衡,生成SO3为1.4 mol,同时放出热量Q kJ。则下列分析正确的是( )
2SO3(g) ΔH<0。2 min后,反应达到平衡,生成SO3为1.4 mol,同时放出热量Q kJ。则下列分析正确的是( )
A.在该条件下,反应前后的压强之比为6∶5.3
B.若反应开始时容器体积为2 L,则v(SO3)=0.35 mol·L-1·min-1
C.若把“恒温恒压下”改为“恒压绝热条件下”反应,平衡后n(SO3)<1.4 mol
D.若把“恒温恒压下”改为“恒温恒容下”反应,达平衡时放出热量大于Q kJ
查看答案和解析>>
科目: 来源: 题型:
【题目】硫—碘循环分解水制氢主要涉及下列反应:
Ⅰ SO2+2H2O+I2===H2SO4+2HI
Ⅱ 2HI![]() H2+I2
H2+I2
Ⅲ 2H2SO4===2SO2+O2+2H2O
(1)分析上述反应,下列判断正确的是____________。
a.反应Ⅲ易在常温下进行 b.反应Ⅰ中SO2氧化性比HI强
c.循环过程中需补充H2O d.循环过程产生1 mol O2的同时产生1 mol H2
(2)一定温度下,向1 L密闭容器中加入1 mol HI(g),发生反应Ⅱ,H2物质的量随时间的变化如图所示。

0~2 min内的平均反应速率v(HI)=____________。该温度下,H2(g)+I2(g)![]() 2HI(g)的平衡常数K=____________。
2HI(g)的平衡常数K=____________。
(3)实验室用Zn和稀硫酸制取H2,反应时溶液中水的电离平衡____________移动(填“向左”、“向右”或“不”);若加入少量下列试剂中的____________,产生H2的速率将增大。
a.NaNO3 b.CuSO4 c.Na2SO4 d.NaHSO3
(4)以H2为燃料可制作氢氧燃料电池。
已知2H2(g)+O2(g)===2H2O(l) ΔH=-572 kJ·mol-1
某氢氧燃料电池释放228.8 kJ电能时,生成1 mol液态水,该电池的能量转化率为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】NA为阿伏加德罗常数,下列说法正确的是
A.标准状况下,22.4 L水中含有的水分子数为NA
B.常温常压下,46 g NO2和N2O4的混合气体中含有的氧原子数为2NA
C.1mol/L的Ba(NO3)2溶液中含NO3-离子数为2NA
D.分子数为NA的CO和N2的混合气体的体积约为22.4 L,质量为28 g
查看答案和解析>>
科目: 来源: 题型:
【题目】氯碱工业是以电解饱和食盐水为基础的基本化学工业。下图是某氯碱工业生产原理示意图:
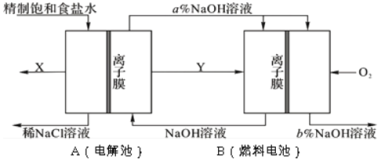
(1)写出装置A在通电条件下反应的化学方程式______________。
(2)A装置所用食盐水由粗盐水精制而成。精制时,为除去食盐水中的Mg2+和Ca2+,要加入的试剂分别为___________、___________。
(3)氯碱工业是高耗能产业,按上图将电解池与燃料电池相组合的新工艺可以节(电)能30%以上,且相关物料的传输与转化关系如图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
①图中Y是______________(填化学式);X与稀NaOH溶液反应的离子方程式是:______________。
②分析比较图示中氢氧化钠质量分数a%与b%的大小___________。
③若用B装置作为A装置的辅助电源,每当消耗标准状况下氧气的体积为11.2 L时,则B装置可向A装置提供的电量约为______________(一个e-的电量为1.60×10-19C;计算结果精确到0.01)。
查看答案和解析>>
科目: 来源: 题型:
【题目】 蚂蚁分泌的蚁酸主要成分是甲酸(结构式为![]() ,Ka=1.8×10-4),通常情况下是一种无色易挥发的液体。甲酸在浓硫酸作用下容易分解产生CO。某化学兴趣小组的同学对HCOOH的性质进行了以下探究:
,Ka=1.8×10-4),通常情况下是一种无色易挥发的液体。甲酸在浓硫酸作用下容易分解产生CO。某化学兴趣小组的同学对HCOOH的性质进行了以下探究:
I、该组同学选择如图1所示的装置探究HCOOH在浓硫酸作用下分解产生了CO,请完成下列各小题。
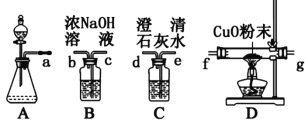

图1 图2
⑴写出甲酸分解的化学方程式 ;
⑵装置的连接顺序a ;
⑶HCOOH的分解产物中有CO的现象 ;
⑷该实验设计有一处明显的缺陷是 ;
II、该组同学分析了甲酸分子结构后,认为甲酸能发生银镜反应,并设计了如图2所示的实验。
⑸依图所示的实验,加热20分钟后并没有出现光亮的银镜。请解释实验中没有产生银镜的原因 ;
⑹请设计实验来验证你的解释 。
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上常采用煅烧黄铁矿来制备SO2,同时产生烧渣。烧渣的主要成分是含铁的氧化物和二氧化硅等,利用烧渣制备高效净水剂聚合硫酸铁可以达到资源综合利用的目的。其工艺流程如下:
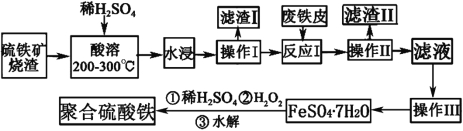
⑴检验“反应I”后的溶液中是否含有Fe3+的试剂是 。
⑵滤渣I的主要成分是 。
⑶“操作III”中具体的方法依次为 、 、过滤和洗涤。
⑷加入适量H2O2的目的是将Fe2+氧化为Fe3+,氧化时需控制反应温度为50~60℃的原因是 。
⑸生成聚合硫酸铁的过程是先水解再聚合,聚合的化学方程式为
mFe2(OH)n(SO4)( 3-![]() )
)![]() [Fe2(OH)n(SO4)( 3-
[Fe2(OH)n(SO4)( 3-![]() )]m
)]m
请写出水解的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com