
科目: 来源: 题型:
【题目】25℃时,在10 mL浓度均为0.1 mol/LNaOH和NH3·H2O混合溶液中滴加0.1 mol/L盐酸,下列有关溶液中粒子浓度关系正确的是( )
A.未加盐酸时:c(OH-)>c(Na+)=c(NH3·H2O)
B.加入盐酸至溶液pH=7时:c(Cl-)=c(Na+)
C.加入10 mL盐酸时:c(NH![]() )+c(H+)=c(OH-)
)+c(H+)=c(OH-)
D.加入20 mL盐酸时:c(Cl-)=c(NH![]() )+c(Na+)
)+c(Na+)
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.高纯度氢氧化镁广泛应用于医药、电力等领域。镁硅酸盐矿石可用于生产氢氧化镁,简要工艺流程如图所示:
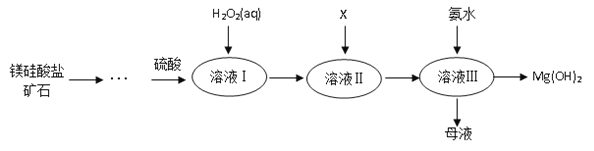
已知:
①溶液Ⅰ中除含Mg2+、SO42外,还含有少量Fe3+、Al3+、Fe2+等离子;
②常温下,几种金属离子开始沉淀和沉淀完全时的pH如下表所示:
金属离子 | Fe3+ | Al3+ | Fe2+ | Mg2+ |
开始沉淀时的pH | 1.5 | 3.3 | 6.5 | 9.4 |
沉淀完全时的pH | 3.7 | 5.2 | 9.7 | 12.4 |
请回答下列问题:
(1)镁在元素周期表中的位置_______________;
(2)向溶液Ⅱ中加入试剂X是_____________,作用是_________________________;
(3)流程中不加H2O2引起的后果是___________________________________;
(4)说出母液的一种用途___________________;
(5)加入H2O2溶液发生反应的离子方程式是___________________;
Ⅱ.海水中含有丰富的镁资源。某同学设计了从模拟海水中制备MgO的实验方案:
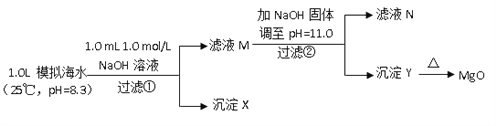
模拟海水中的离子浓度/ (mol/L) | Na+ | Mg2+ | Ca2+ | Cl- | HCO3- |
0.439 | 0.050 | 0.011 | 0.560 | 0.001 |
注:溶液中某种离子的浓度小于1.0×10-5mol/L,可认为该离子不存在;实验过程中,假设溶液体积不变。
已知:Ksp(CaCO3)=4.96×10-9;Ksp(MgCO3)=6.82×10-6;Ksp [Ca(OH)2]=4.68×10-6;Ksp [Mg(OH)2]=5.61×10-12。请回答下列问题:
(6)沉淀物X为_____________;
(7)滤液N中Ca2+浓度为_______________;
(8)加NaOH固体调整pH=12.5是否可行______(填“是”“否”);原因是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】将化合物A的蒸气2 mol充入0.5 L容器中加热,发生分解反应2A(g) ![]() B(g)+nC(g),反应到3 min时,容器中A的浓度为1.6 mol·L-1,测得这段时间内,用C的浓度变化表示的平均反应速率v(C)=1.2 mol·L-1·min-1。
B(g)+nC(g),反应到3 min时,容器中A的浓度为1.6 mol·L-1,测得这段时间内,用C的浓度变化表示的平均反应速率v(C)=1.2 mol·L-1·min-1。
(1)化学方程式中的化学计量数n的值是__________。
(2)以B的浓度变化表示的该反应的平均速率为______。
查看答案和解析>>
科目: 来源: 题型:
【题目】工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法是还原沉淀法。该法的工艺流程为:![]()
其中第①步存在平衡:2 CrO42-(黄色)+2H+![]() Cr2O72- (橙色)+H2O
Cr2O72- (橙色)+H2O
(1) 若平衡体系的pH=12,则溶液显_______色。
(2) 能说明第①步反应达平衡状态的是______________。
a.Cr2O72-和CrO42-的浓度不变
B.2v(Cr2O72-) =v(CrO42-)
C.溶液的颜色不变
(3)第②步中,还原lmol Cr2O72-离子,需要_______mol的FeSO47H2O。
(4)第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr (OH)3 (s)![]() Cr3+ (aq) +3OH- (aq)
Cr3+ (aq) +3OH- (aq)
常温下,Cr(OH)3的溶度积Ksp=c(Cr3+)·c3(OH-) = 10-32,要使0.01mol/Lc(Cr3+)开始沉淀,溶液的pH应调至__________,若使c(Cr3+)降至10-5mol/L,溶液的pH应调至___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在元素周期表第三周期中,置换酸中氢能力最强的元素的元素符号为_____,最高价氧化物对应水化物的酸性最强的化合物的化学式是__________,碱性最强的化合物的化学式是__________,显两性的氢氧化物的化学式是__________,该两性氢氧化物与盐酸、氢氧化钠溶液分别反应的离子方程式为__________________、_________________,原子半径最大的金属元素的名称是________,离子半径最小的离子结构示意图是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】T℃时在2L密闭容器中使X(g)与Y(g)发生反应生成Z(g),反应过程中X、Y、Z的物质的量变化如图1所示;若保持其他条件不变,温度分别为T1和T2,Y的百分含量与时间的关系如图2所示。下列分析不正确的是( )

A.容器中发生的反应可表示为:3X(g)+Y(g)2Z(g)
B. 0~3min内,v(X)=0.1 mol/(Lmin)
C.若改变条件,使反应进程如图3所示,则改变的条件可能是增大压强
D.达平衡后,升高温度,v正、v逆都增大,且再次平衡前v正>v逆
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,0.1molL-1某一元酸(HA)溶液![]() 中= 1×10-8,相同物质的量浓度的某一元碱(BOH)溶液中
中= 1×10-8,相同物质的量浓度的某一元碱(BOH)溶液中![]() = 1×1012,下列叙述正确的是( )
= 1×1012,下列叙述正确的是( )
A.PH=a的HA溶液,稀释10倍,其pH=a+1
B.等体积的HA和BOH恰好完全反应,溶液的pH=7
C.HA的pH=3;BOH的pH=13
D.相同体积相同pH的HA和盐酸分别与足量Zn反应,生成氢气的物质的量相同
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周
期序数与族序数相等,请回答下列问题:
Q | R | ||
T | W |
(1)T的原子结构示意图为____________
(2)元素原子的得电子能力为Q____W(填“>”或“<”)。
(3)W的单质与其最高价氧化物对应的水化物浓溶液共热能发生反应,生成两种物质,其中一种是具有漂白性的气体,反应的化学方程式为
________________________________________________________________________
(4)原子序数比R多1的元素的一种氢化物在二氧化锰催化作用下易分解为它的另一种氢化物,此分解反应的化学方程式是
________________________________________________________________________
(5)将12 g Q单质在足量的氧气中燃烧,所得气体通入1 L 1.5 mol·L-1NaOH溶液中,完全吸收后,溶液中大量存在的离子有______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知以下信息:①1 mol N2的共价键断裂吸收946 kJ的能量;1 mol H2的共价键断裂吸收436 kJ的能量;形成1 mol NH3中的化学键释放1 173 kJ的能量。②将一定量的N2和H2投入一密闭容器中,在一定条件下进行反应,测得有关数据如下:
N2(mol·L-1) | H2(mol·L-1) | NH3(mol·L-1) | |
起始时 | 3 | 3 | 0 |
2s末 | 2.6 | 1.8 | 0.8 |
根据以上相关数据回答问题:
(1)用H2表示该反应2 s内的平均反应速率为________
(2)______(填“能”或“不能”)确认该反应2 s末已达化学平衡状态。
(3)写出该反应的化学方程式:
________________________________________________________________________。
(4)氮气和氢气生成氨气的过程______(填“释放”或“吸收”)能量。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com