
科目: 来源: 题型:
【题目】碘及其化合物在科研、生活等方面有广泛用途。回答下列问题:
(1)海带中富含碘,按如下实验流程可对海带中碘的含量进行测定。

取0.0100 mol/L的AgNO3标准溶液装入棕色滴定管,取100.00 mL海带浸取原液至滴定池,用电势滴定法测定碘含量。测得的电动势(E) 反映溶液中c(Iˉ)的变化,部分数据如下表:
V(AgNO3)/mL | 15.00 | 19.00 | 19.80 | 19.98 | 20.00 | 20.02 | 21.00 | 23.00 | 25.00 |
E/mV | -225 | -200 | -150 | -100 | 50.0 | 175 | 275 | 300 | 325 |
①灼烧海带时,除需要坩埚外,还需要用到的实验仪器是____________ (填序号)。
a.烧杯 b.三脚架 c.温度计 d.泥三角 e.酒精灯 f.坩埚钳
②使用棕色滴定管的原因是_____________________。
③根据表中数据,计算海带中碘的百分含量为____________。
(2)“大象的牙膏”是著名化学实验之一,其实验方法是将浓缩的过氧化氢溶液与肥皂液混合,再滴加少量碘化钾溶液,即可观察到泡沫状物质像喷泉一样喷涌而出。
已知:2H2O2(l)=2H2O(l)+O2(g) △H=-196kJ/mol,活化能Ea=76kJ/mol,若用I-催化时活化能Ea’=57kJ/mol。
①在H2O2溶液中加入KI溶液作催化剂,反应过程中发生I-与IO-之间的转化,请依次写出发生反应的离子方程式:
反应甲:______________________;
反应乙:______________________。
②反应甲为吸热反应,且甲的反应速率小于乙的反应速率,在下图中画出在H2O2溶液中加入KI后,反应过程的能量变化图。_______

(3)HI不稳定,其水溶液具有强酸性。现用0.lmol/LKI溶液、NH4I固体、pH试纸设计实验验证上述性质。简述实验方案。
①强酸性:__________________________。
②不稳定性:___________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】现有短周期主族元素X、Y、Z、R、T五种,R原子的最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Y与T同主族。五种元素原子半径与原子序数之间的关系如图所示。下列推断正确的是

A. 离子半径:Y<Z
B. 氢化物的稳定性:Y<T
C. 最高价氧化物对应水化物的酸性:T<R
D. 由X、Y、Z三种元素组成的常见化合物中含有离子键
查看答案和解析>>
科目: 来源: 题型:
【题目】微量元素硼和镁对植物的叶的生长和人体骨骼的健康有着十分重要的作用。
(1)写出基态B原子的轨道表达式___________________。
(2)三价B易形成配离子,如[B(OH)4]-、[BH4]-等。[B(OH)4]-的结构式为___________________ (标出配位键),其中心原子的杂化方式为式________,写出[BH4]-的两种等电子体________________。
(3)图1表示多硼酸根的一种无限长的链式结构,其化学式可表示为____________(以n表示硼原子的个数)。

(4)硼酸晶体是片层结构,图2表示的是其中一层的结构。层间存在的作用力有_________________;硼酸晶体在冷水中溶解度很小,但在热水中较大,原因是_____________________。
(5)三氯化硼的熔点比氯化镁的熔点低,原因是_________________________________________。
(6)镁属六方最密堆积(图3),其晶胞结构如图4所示,若镁原子半径为apm,则镁晶体的密度为_________________________________g/cm3(用含a的代数式表示)。

查看答案和解析>>
科目: 来源: 题型:
【题目】为测定某烃类物质A的结构,进行如下实验。
(1)将有机物A置于足量氧气中充分燃烧,将生成物通过浓硫酸,浓硫酸增重7. 2克,再将剩余气体通过碱石灰,减石灰增重17.6克;则物质A中各元素的原子个数比是________________;
(2)质谱仪测定有机化合物A的相对分子质量为56,则该物质的分子式是____________;
(3)根据碳原子和氢原子的成键特点,预测能够使酸性高锰酸钾溶液和溴的四氯化碳溶液褪色的A的可能结构并写出结构简式______________。(含顺反异构)
(4)经核磁共振氢谱测定,有机物A分子内有4种氢原子,则用方程式解释A使溴的四氯化碳溶液褪色的原因:______________,反应类型:________________;A也可能合成包装塑料,请写出相关的化学反应方程式:______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】厨房垃圾发酵液可通过电渗析法处理,同时得到乳酸的原理如图所示(图中HA表示乳酸分子,A—表示乳酸根离子)。下列说法正确的是( )

A. 通电后,阳极附近pH增大
B. 电子从负极经电解质溶液回到正极
C. 通电后,A—通过阴离子交换膜从阴极进入浓缩室
D. 当电路中通过2 mol电子的电量时,会有1 mol的O2生成
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,密闭容器中进行反应:2SO2(g)+O2(g)![]() 2SO3(g) △H<0。测得v正(SO2)随反应时间(t)的变化如图所示。下列有关说法正确的是( )
2SO3(g) △H<0。测得v正(SO2)随反应时间(t)的变化如图所示。下列有关说法正确的是( )

A. t2时改变的条件是:只加入一定量的SO2
B. 在t1时平衡常数K1大于t3时平衡常数K2
C. t1时平衡混合气的![]() 大于t3时平衡混合气的
大于t3时平衡混合气的![]()
D. t1时平衡混合气中SO3的体积分数等于t3时平衡混合气中SO3的体积分数
查看答案和解析>>
科目: 来源: 题型:
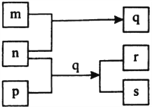
【题目】元素W、X、Y、Z的原子序数依次增加。p、q、r是由这些元素组成的二元化合物。m、n分别是元素Y、Z的单质,n通常为深红棕色液体,0.01 mol/L r溶液的pH为2,p被英国科学家法拉第称为“氢的重碳化合物”,s通常是难溶于水、比水重的油状液体。上述物质的转化关系如图所示。下列说法不正确的是( )
A. 原子半径的大小W<X<Z
B. W的氧化物常温常压下为液态
C. Y的氧化物可能呈黑色或红棕色
D. Z的氧化物的水化物一定为强酸
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下,容器内某反应中M、N的物质的量随反应时间变化的曲线如下图,下列表述中正确的是

A. t3时,正反应速率大于逆反应速率
B. t2时,正逆反应速率相等,反应达到平衡状态
C. 化学方程式为:2M= N
D. t1时,N的浓度是M浓度的2倍
查看答案和解析>>
科目: 来源: 题型:
【题目】对于反应2HI(g) ![]() H2(g) +I2(g),下列叙述能够说明己达平衡状态的是
H2(g) +I2(g),下列叙述能够说明己达平衡状态的是
A. 混合气体的颜色不再变化
B. 温度和体积一定时,容器内压强不再变化
C. lmolH-H键生成的同时有2molH-I键断裂
D. 各物质的物质的量浓度之比为2:1:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com