
科目: 来源: 题型:
【题目】将某些化学知识用数轴表示,可以收到直观、简明、易记的效果。用数轴表示的下列知识正确的是( )
A. 硫及其化合物的化合价与氧化还原反应的关系:
B. 分散系的分类:
C. AlCl3溶液与NaOH溶液反应后铝元素的存在形式:
D. CO2与NaOH溶液反应后的产物
查看答案和解析>>
科目: 来源: 题型:
【题目】今有H2、Cl2混合气100mL(标况),其中一种气体体积为45mL。光照使两种气体发生反应后恢复到标况,气体体积为______mL。为了说明反应后气体中H2或Cl2有剩余,使气体通过10mL水,并使剩余气体干燥后恢复到标况,若(1)剩余________mL,证明有________剩余;理由___________________。
(2)溶液有________性质,证明有________剩余;理由是____________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】室温下,单质A、B、C分别为固体、黄绿色气体、无色气体,在合适反应条件下,它们可按下面框图进行反应。又知E溶液是无色的。
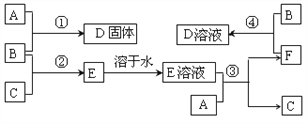
请回答:
(1)A是____________,B是____________,C是_____________。(填化学式)
(2)反应①的化学方程式为________________________________________
(3)反应③的化学方程式为________________________________________
(4)反应④的化学方程式为________________________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】把铁片放入下列溶液中,铁片溶解,溶液质量增加,但没有气体放出的是
A. 稀硫酸 B. CuSO4溶液 C. Fe2(SO4)3溶液 D. AgNO3溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】(l)将Cl2通入水中,Cl2部分与水反应:Cl2+H2O=H++Cl-+HClO。若要减少Cl2的溶解,可在氯水中加入少量________。
a.AgNO3晶体 b. CaCO3粉末 c. NaCl晶体 d.蒸馏水 e.浓盐酸
(2)在一定条件下,同时加入CO、H2O(g)、CO2、H2于一密闭容器中发生如下反应:CO +H2O(g)![]() CO2+H2,反应开始时向右进行。下列说法中不正确的是__________。
CO2+H2,反应开始时向右进行。下列说法中不正确的是__________。
a.反应开始时,正反应速率大于逆反应速率
b.反应开始时,正反应速率最大,逆反应速率为零
c.随着反应的进行,正反应速率逐渐减小,最后为零
d.随着反应的进行,逆反应速率增大,正反应速率减小,最后相等。
(3)一定条件下(温度值定), SO2与O2反应的浓度随时间的变化如下表
时间(min) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
c(SO2)mol/L | 1.0 | |||||||
c(O2)mol/L | 0.5 | 0.35 | 0.25 | 0.18 | 0.1 | 0.05 | 0.05 | 0.05 |
C(SO3)mol/L | 0 | 0.3 | 0.5 | 0.65 | 0.8 | 0.9 | 0.9 | 0.9 |
由上表数据计算:
a.30min-40min 时间段,以SO2表示的反应速率为__________;
b.该温度下,正反应的平衡常数的值为__________________;
c.平衡时,SO2的转化率为_______;
(4)电解尿素[CO(NH3)2]的碱性溶液制氢气的装置示意图见下图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。电解时,阳极的电极反应式为____________。

(5)3.04g铜镁合金完全溶解于100mL密度为1.40g/mL、质量分数为63%的硝酸中,得到NO2气体2688mL(标准状况),向反应后的溶液中加入1.0mol/L NaOH溶液,当金属离子全部沉淀时,得到5.08g沉淀。则加入NaOH溶液的体积是_________mL。
查看答案和解析>>
科目: 来源: 题型:
【题目】镁被称为“国防金属”,镁及其合金用途很广,目前世界上60%的镁从海水中提取。从海水中提取镁的流程如下:
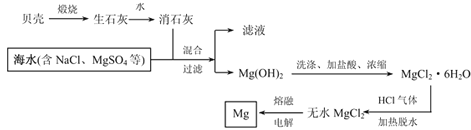
请根据上述流程图和镁及化合物的性质回答下列问题:
(1)用贝壳煅烧生石灰的反应方程式:________________
(2)氢氧化镁溶于盐酸的离子方程式为:_____________。
(3)简述,由MgCl2·6H2O制无水MgCl2,加热时通HCl气体的主要原因是:___________。
(4)金属镁属于(填写下列编号):___________。
a.黑色金属 b.有色金属 c.轻金属 d.重金属 e.贵金属
(5)Mg(OH)2煅烧可得熔点很高的MgO,MgO的电子式为:____________。
(6)MgCl2和AlCl3的熔点均较低,加MgO和Al2O3的熔点都很高。为什么冶炼金属镁是电解MgCl2,而冶炼金属铝则电解Al2O3:_______________。
(7)某MgCl2溶液的浓度为0.01mol/L,在该溶液中滴加NaOH溶液至pH=10,此时溶液中的Mg2+是否沉淀完全?_________(填“是”或“否”),此时c(Mg2+)=_________。
(已知:Ksp[Mg(OH)2]=1.8×10-11)
查看答案和解析>>
科目: 来源: 题型:
【题目】海洋是生命的摇篮,海水不仅是宝贵的水资源,而且蕴藏着丰富的化学资源。从海水中提取一些重要的化工产品的工艺流程如图所示。

根据上述流程图回答下列问题:
(1)海水淡化处理的方法有蒸馏法、冷冻法、_____________。(写出1种即可)
(2)写出反应①化学反应方程式_______________________________________。
(3)标准状况下22.4 L Cl2气体发生反应②,转移的电子数是________NA。
(4)反应③中硫酸酸化可提高Cl2的利用率,理由是____________________________。
(5)过程③到过程⑤的变化为“Br-→Br2→Br-→Br2”,其目的是_______________。
(6)浓缩氯化镁溶液后冷却可以得到MgCl2﹒6H2O,该晶体受热时会发生如下变化:MgCl2﹒6H2O== Mg(OH)Cl + HCl↑+ 5H2O。则,从溶液制备无水晶体的“操作a”可以采取的措施是__________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验证明:Cu不能在常温下与O2反应,也不能与稀硫酸共热发生反应。但工业上却是将废铜屑倒入热的稀硫酸中并通入空气来制CuSO4的,铜屑在此条件下被溶解的化学方程式为______________。利用Cu制备CuSO4的另一种方法可用化学方程式表示为____________________________。
以上两种方法______ (填“前”、“后”) 者好,这样做的好处是①_________________________ ,②_______________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物G可用于治疗哮喘、系统性红斑狼疮等。其合成路线如下图所示。

已知:
①通常在同一碳原子上连有两个烃基不稳定,易脱水形成羰基
②醛能发生羟醛缩合反应,最终脱水生成不饱和醛:

③
请回答:
(1)A生成B的反应类型为_________,B中含有的官能团名称为_________。
(2)写出两个符合下列条件的A的同分异构体结构简式________。
①能与氯化铁溶液发生显色反应
②核磁共振氢谱显示分子中苯环上有两种不同化学环境的氢原子
(3)化合物C的结构简式为_________。
(4)D
![]()
E的化学方程式为__________。
(5)1molG在一定条件下与足量H2充分反应,需要消耗H2__________mol。
(6)![]() 可由
可由![]() 和有机物H分子间脱去一分子水而得,则H的名称为______;通常采用
和有机物H分子间脱去一分子水而得,则H的名称为______;通常采用![]() 为原料合成
为原料合成![]() ,请参照题目路线图设计该合成路线______(无几时机任选)。
,请参照题目路线图设计该合成路线______(无几时机任选)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com