
科目: 来源: 题型:
【题目】五种短周期元素在元素周期表中的位置如图所示,已知:E元素原子的最外层电子数是次外层的2倍。下列说法不正确的是
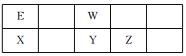
A. X有多种氢化物 B. 简单阴离子的半径:Y>Z
C. 气态氢化物的稳定性:W>Y>Z D. Y的氢化物与Z单质能发生化学反应
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室制备氯气的反应原理为MnO+4HCl( 浓) ![]() MnCl2+Cl2↑+2H2O,然后用制取的气体进行性质实验。请完成下列问题:
MnCl2+Cl2↑+2H2O,然后用制取的气体进行性质实验。请完成下列问题:

(1) 制取氯气的反应中还原剂与氧化剂的物质的量之比为__________;
(2) 氯气不溶于饱和食盐水,装置②的作用:________;浓硫酸的作用: ________;
(3) ④布条上现象: ________;⑤布条上现象: ________;
(4) NaOH 溶液中发生反应的主要离子方程式为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】有一医药中间体的结构简式如下: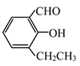
(1)其分子式为______ ,含有的含碳官能团名称为______.
(2)关于其化学性质的描述,下列不正确的是(_____).
A. 能与氯化铁溶液发生化学反应 B. 能发生银镜反应
C. 能使溴水褪色 D. 能发生消去反应
(3)一定条件下,1mol该物质最多可与____ molH2发生加成反应.
(4)同时符合下列条件的同分异构体有____ 种.
①苯环上只有两个取代基; ②能与碳酸氢钠溶液反应
查看答案和解析>>
科目: 来源: 题型:
【题目】碳、钠、氯、铁等元素形成的单质及化合物在社会生活中应用广泛。请完成下列有关问题:
(1)工业用氯气与消石灰生产漂白粉,漂白粉的有效成分在水溶液中的电离方程式为______ 。
(2)氯化亚铁溶液中滴入几滴KSCN溶液无明显变化,再滴加少最氯水溶液变成红色,写出该变化过程中的化学方程式,开标出电子转移的方向与数目:______ 。
(3)实现C2O42-→CO2的转化必须加入______ (选填:氧化剂、还原剂、酸)。
(4)一个钠离子的质量为______ (保留三位有效数宁)。
(5)CO、CO2、O3(臭氧)三种气体,含有的氧原子数相等,则三种气体在同温同压下的体积比为______ 。
查看答案和解析>>
科目: 来源: 题型:
【题目】砷为第4周期第ⅤA族元素,根据它在元素周期表中的位置推测,砷不可能具有的性质是( )
A. 砷在通常情况下是固体
B. 可以存在-3、+3、+5等多种化合价
C. As2O5对应水化物的酸性比H3PO4弱
D. AsH3的稳定性比PH3强
查看答案和解析>>
科目: 来源: 题型:
【题目】某学生将一氯丙烷和NaOH溶液共热煮沸几分钟后,冷却,滴入AgNO3溶液,结果未见到白色沉淀生成,其主要原因是( )
A.加热时间太短B.不应冷却后再滴入AgNO3溶液
C.加AgNO3溶液后未加稀HNO3D.加AgNO3溶液前未用稀HNO3酸化
查看答案和解析>>
科目: 来源: 题型:
【题目】用下图所示装置除去含CN-、Cl-、废水中的CN-时,控制溶液pH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是( )

A. 可以用石墨作阳极,铁作阴极
B. 阳极的电极反应式为:Cl-+2OH--2e-=ClO-+H2O
C. 阴极的电极反应式为:2H2O+2e-=H2↑+2OH-
D. 除去CN-的反应:2CN-+5ClO-+2H+=N2↑+2CO2↑+5Cl-+H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】利用水钴矿(主要成分为Co2O3,含少量Fe2O3、A12O3、MnO、MgO、CaO、SiO2等)可以制取多种化工试剂,以下为草酸钴晶体和氯化钴晶体的制备流程,回答下列问题:

已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+、Mg2+、Ca2+等.
②沉淀I中只含有两种沉淀。
③流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见下表.
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)浸出过程中Co2O3发生反应的离子反应方程式为___________。
(2)NaClO3在浸出液中发生的离子反应方程式为_________________。
(3)加入Na2CO3调PH至5.2,目的是__________________________;萃取剂层含锰元素,则沉淀II的主要成分为_____________。
(4)操作I包括:将水层加入浓盐酸调整PH为2~3,___________、____________、过滤、洗涤、减压烘干等过程。
(5)为测定粗产品中CoCl2·6H2O含量,称取一定质量的粗产品溶于水,加入足量硝酸酸化的硝酸银溶液,过滤、洗涤、干燥,测沉淀质量。通过计算发现粗产品中CoCl2·6H2O质量分数大于100%,其原因可能是____________________(回答一条原因即可)。
(6)将5.49g草酸钴晶体(CoC2O4·2H2O)置于空气中加热,受热过程中不同温度范围内分别得到一种固体物质,其质量如下表.
温度范围/℃ | 固体质量/g |
150~210 | 4.41 |
290~320 | 2.41 |
经测定,整个受热过程,只产生水蒸气和CO2气体,则290~320℃温度范围,剩余的固体物质化学式为__。
[已知: CoC2O4·2H2O的摩尔质量为183g·mol-1]
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A、B、C、D是中学化学的常见物质,且A、B、C均含有同一种元素。在一定条件下它们之间的相互转化关系如图所示(部分反应中的H2O已略去)。

请回答下列问题:
(1)若A可用于自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,加热蒸干B的溶液不能得到B,则B的化学式可能是_____________;工业上制取A的离子方程式为________________。
(2)若A是一种碱性气体,常用作制冷剂,B是汽车尾气之一,遇空气会变色,则反应则C的化学式是_____________ ①的化学方程式为______________________________。
(3)若D是氯碱工业的主要产品之一,B有两性,则反应②的离子方程式是________。
(4)若A、C、D都是常见气体,C是导致酸雨的主要气体,则反应③的化学方程式为________。某同学将搜集到的一定量的酸雨保存在密闭容器中,每隔一定时间测酸雨的pH,发现在起始一段时间内,酸雨的pH呈减小趋势,用离子方程式解释原因:_________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某溶液可能含有K+、NH4+、Mg2+、Fe2+、Fe3+、SO42-、Br-、Cl-、CO32-中的若干种,离子浓度均相等,实验及现象如下:
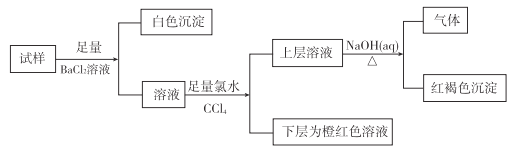
下列判断正确的是
A. 白色沉淀是BaSO4和BaCO3
B. 原溶液存在Fe3+,不存在Fe2+
C. 若原溶液存在Fe3+,必然存在Cl-,无K+
D. 原溶液不存在CO32-、Mg2+、K+、C1-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com