
科目: 来源: 题型:
【题目】T ℃时在2 L的密闭容器中X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,反应温度分别为T1和T2时,Y的体积分数与时间的关系如图2所示。则下列结论正确的是
 A.反应进行的前3 min内,用X表示的反应速率v(X)=0.3 mol·(L·min)-1
A.反应进行的前3 min内,用X表示的反应速率v(X)=0.3 mol·(L·min)-1
B.容器中发生的反应可表示为3X(g)+Y(g) ![]() 2Z(g)
2Z(g)
C.保持其他条件不变,升高温度,反应的化学平衡常数K减小
D.若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强
查看答案和解析>>
科目: 来源: 题型:
【题目】锰酸锂(LiMn2O4)可作为锂离子电池的正极材料。工业上利用软锰矿浆吸收含硫烟气(SO2 和O2)制备锰酸锂,生产流程如下:
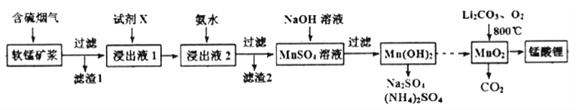
已知:①软锰矿主要成分为MnO2,含少量Fe2O3、FeO、Al2O3、SiO2等杂质。
②软锰矿浆在吸收含硫烟气的过程中酸性逐渐增强。
③部分氢氧化物沉淀相关的溶液pH如下表:
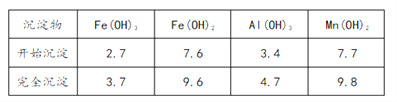
(1)已知:
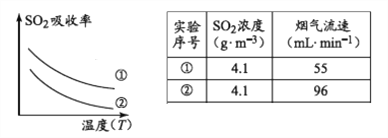
下列措施可提高SO2吸收率的是__________(填序号)
a.降低通入含硫烟气的温度 b.升高通入含硫烟气的温度
c.减少软锰矿浆的进入量 d.减小通入含硫烟气的流速
(2)加入试剂X能提高产品纯度,则X可以是_____________(填化学式)
(3)加氨水调溶液pH在5~6之间,目的是_______________。
(4)锰酸锂可充电电池的总反应式为:Li1-xMnO2+LixC ![]() LiMn2O4+C(x<1)
LiMn2O4+C(x<1)
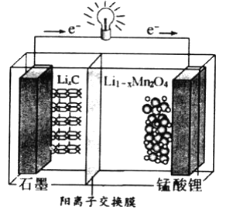
①放电时,电池的正极反应式为__________________
②充电时,若转移1mole-,则石墨电极将增重__________g。
查看答案和解析>>
科目: 来源: 题型:
【题目】卤代烃在生产生活中具有广泛的应用,回答下列问题:
(1)多氯代甲烷常为有机溶剂,其中分子结构为正四面体的是 . 工业上分离这些多氯代物的方法是 .
(2)三氟氯溴乙烷(CF3CHClBr)是一种麻醉剂,写出其所有同分异构体的结构简式(不考虑立体异构).
(3)聚氯乙烯是生活中常用的塑料.工业生产聚氯乙烯的一种工艺路线如下: ![]()
反应①的化学方程式为 , 反应类型为;反应②的反应类型为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物I(C12H14O3)是制备液晶材料的中间体之一,其分子中含有醛基和酯基。
I可以用E和H在一定条件下合成:
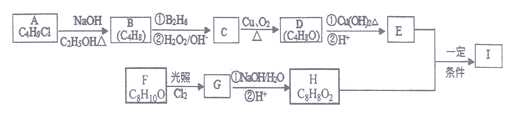
己知以下信息:①A的核磁共振氧谱表明其只有一种化学环境的氢;
②![]() ;
;
③化合物F苯环上的一氯代物只有两种且遇Fe3+不变色;
④通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
请回答下列问题:
(1) A的结构简式为____________,B所含官能团的名称是____________________。
(2)C的名称为______________,E的分子式为__________________。
(3) A→B、C→D的反应类型分别为____________________、______________________。
⑷写出F→G的化学方程式:____________________。
(5)I的结构简式为_____________________。
(6)I的同系物J比I相对分子质量小28,J的同分异构体中能同时满足如下条件:①苯环上只有一个取代基;②既能发生银镜反应,又能与饱和NaHCO3溶液反应放出CO2,共有_______种(不考虑立体异构)。上述同分异构体中有一种发生银镜反应并酸化后核磁共振氢谱为五组峰,且峰面积比为1:2:2:2:3,写出J的这种同分异构体的结构简式___________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】滴液漏斗已知:R﹣OH+HX→R﹣X+H2O
如图是实验室用乙醇与浓硫酸和溴化钠反应制备溴乙烷的装置,图中省去了加热装置.有关数据见表: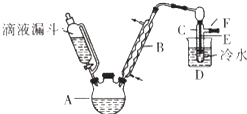
乙醇、溴乙烷、溴有关参数
乙醇 | 溴乙烷 | 溴 | |
状态 | 无色液体 | 无色液体 | 深红棕色液体 |
密度/gcm﹣3 | 0.79 | 1.44 | 3.1 |
沸点/℃ | 78.5 | 38.4 | 59 |
(1)制备操作中,加入的浓硫酸必需进行稀释,其目的是 .
a减少副产物烯和醚的生成 b.减少Br2的生成c减少HBr的挥发 d.水是反应的催化剂
(2)加热的目的是(从速率和限度两方面回答);应采取的加热方式是 .
(3)为除去产品中的一种主要杂质,最好选择下列溶液来洗涤产品.
A.氢氧化钠
B.碘化钠
C.亚硫酸钠
(4)第(3)步的实验所需要的主要玻璃仪器是 .
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室用图示装置制备KC1O溶液,再与KOH、Fe(NO3)3溶液反应制备髙效净水剂K2FeO4。

<査阅资料>O2与KOH溶液在20℃以下反应生成KC1O,在较高温度下则生成KC1O3;K2FeO4易溶于水,微溶于浓KOH溶液,在0℃~5℃的强碱性溶液中较稳定。
(1)仪器a的名称是___________;装置A中反应的离子方程式为___________________。
装置C中三颈烧瓶置于冰水浴中的目的是_______________。
(2)装置B吸收的气体是___________,装置D的作用是____________________。
(3)C中得到足量KC1O后,将三颈烧瓶上的导管取下,依次加入KOH溶液、Fe(NO3)3溶液,水浴控制反应温度为25℃,搅拌1.5 h,溶液变为紫红色(含K2FeO4),该反应的离子方程式为________________。再加入饱和KOH溶液,冷却至0℃~5℃析出紫黑色晶体,过滤,得到K2FeO4粗产品。
(4)K2FeO4粗产品含有Fe(OH)3、KC1等杂质,其提纯步骤为:
①将一定量的K2FeO4粗产品溶于冷的3 mol/LKOH溶液中。
②过滤。
③____________________。
④搅拌、静置、过滤,用乙醇洗涤2~3次,
⑤在真空干燥箱中干燥。
(5)称取提纯后的K2FeO4样品0.2200 g于烧杯中,加入强碱性NaCr(OH)溶液,反应后再加稀H2SO4调节溶液呈强酸性,配成250 mL溶液,取出25.00 mL放入锥形瓶,用0.01000 mol/L的(NH4)2Fe(SO4)2溶液滴定至终点,重复操作2次,平均消耗(NH4)2Fe(SO4)2溶液30.00 mL。涉及主要反应为:
Cr(OH)4-+FeO42- =Fe(OH)3↓+CrO42-+OH-
2CrO42-+2H+![]() Cr2O72-+H2O
Cr2O72-+H2O
Cr2O72-+6Fe2++14H+=6Fe3++2Cr3++7H2O
则该K2FeO4样品的纯度为_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com