
科目: 来源: 题型:
【题目】对于2X(g)![]() Y(g)的体系,在压强一定时,平衡体系中Y的质量分数w(Y)随温度的变化情况如图所示(实线上的任何一点为对应温度下的平衡状态)。
Y(g)的体系,在压强一定时,平衡体系中Y的质量分数w(Y)随温度的变化情况如图所示(实线上的任何一点为对应温度下的平衡状态)。

(1)该反应的正反应方向是一个________反应(“吸热”或“放热”)。
(2)A、B、C、D、E各状态中,v正<v逆的点是____________。
(3)维持t1不变,E→A所需时间为x,维持t2不变,D→C所需时间为y,则x ______ y(填“<”、“>”或“=”)。
(4)欲使E状态从水平方向到C状态后,再沿平衡曲线到达A状态,从理论上来讲,可选用的条件是____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】2SO2(g)+O2(g) ![]() 2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH= -99kJ·mol-1。请回答下列问题:
2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH= -99kJ·mol-1。请回答下列问题:
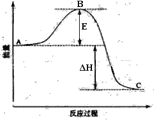
(1)图中E表示__________。E的大小对该反应的反应热_______(填“有”或“无”)影响。
(2)该反应通常用V2O5作催化剂,加V2O5会使图中B点(填“升高”还是“降低”),△H______(填“变大”、“变小”或“不变”)。
(3)图中△H=___________kJ·mol-1;
(4)当反应达到平衡时,升高温度,反应速率_______ (增大”“减小”或“不变”),SO2的转化率_________ (增大”“减小”或“不变”),原因是______________________
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于周期表的说法正确的是
A. 同一周期元素原子的最外层电子数相同
B. 同一主族元素原子的电子层数相同
C. 能生成碱的金属都在第ⅠA族
D. 第ⅦA族元素统称为卤族元素
查看答案和解析>>
科目: 来源: 题型:
【题目】有关AgCl的沉淀溶解平衡说法中正确的是( )
A.AgCl沉淀生成和溶解不断进行,速率相等
B.AgCl难溶于水,溶液中没有Ag+和Cl-
C.AgCl悬浊液中加入NaCl固体,AgCl溶解度不变
D.升温,AgCl沉淀的溶解度减小
查看答案和解析>>
科目: 来源: 题型:
【题目】烧瓶中放入铜片和稀硝酸,来制取较纯净的一氧化氮,反应开始后发现烧瓶中充满红棕色气体,这时的操作应是 ( )。
A. 立即接上收集容器,用向上排空气法收集
B. 待烧瓶中红棕色气体消失后,用向上排空气法收集
C. 待烧瓶中红棕色气体消失后,用排水法收集
D. 立即用排水法收集
查看答案和解析>>
科目: 来源: 题型:
【题目】英国一家公司正在研发全球首款“充一次电,用七天”的碱性氢氧燃料手机电池.如图为碱性氢氧燃料电池结构示意图. 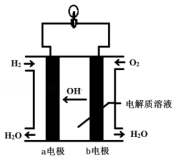
请回答下列问题.
(1)电池是将化学能直接转化为能的装置.
(2)氢氧燃料电池中发生反应的化学方程式是 . 作为碱性氢氧燃料电池,该电池的电解质溶液可以是 .
(3)b 电极上的反应为,则该电极为电池的极.从氧化还原角度分析,该反应属于反应.
(4)氢氧燃料电池与普通电池相比,其优点是(答出一点即可).但作为手机电池,长时间使用时,会感觉手机发烫,这是因为有一部分能量转化为能,所以它还需要解决一些问题,如:手机壳必须多开一个排气孔,可能的原因是 .
查看答案和解析>>
科目: 来源: 题型:
【题目】依据事实,写出下列反应的热化学方程式。
(1)在25℃、101 kPa下,1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ。则表示甲醇燃烧热的热化学方程式为 。
(2)若适量的N2和O2完全反应,每生成23 g NO2需要吸收16.95 kJ热量,则表示该反应的热化学方程式为 。
(3)NA为阿伏加德罗常数,C2H2(g)完全燃烧生成CO2和液态水的反应,有5NA个电子转移时,放出650 kJ的热量,该反应的热化学方程式为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下,将X和Y各0.16 mol加入10 L恒容密闭容器中,发生反应X(s)+2Y(g) ![]() 2Z(g) △H<0,一段时间后达到平衡。反应过程中测定的数据如下表:
2Z(g) △H<0,一段时间后达到平衡。反应过程中测定的数据如下表:
t/min | 2 | 4 | 7 | 9 |
n(Y)mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是( )
A. 其他条件不变,再充入0.2 mol Z,Z的体积分数增大
B. 该温度下此反应的平衡常数K=l.44
C. 当容器内气体的平均摩尔质量不变时,即达到化学平衡状态
D. 反应前 2 min 的平均速率 v(Z)=4.0×10-3mol·L-1·min-1
查看答案和解析>>
科目: 来源: 题型:
【题目】在3种不同条件下,分别向容积为2L的恒容密闭容器中充入2 molA和1 mol B,发生反应:2A(g)+B(g)![]() 2D(g) △H=QkJ·mol-1。相关条件和数据见下表:
2D(g) △H=QkJ·mol-1。相关条件和数据见下表:
实验编号 | 实验Ⅰ | 实验Ⅱ | 实验Ⅲ |
反应温度/1C | 700 | 700 | 750 |
达平衡时间/min | 40 | 5 | 30 |
n(D)平衡/mol | 1.5 | 1.5 | 1 |
化学平衡常数 | K1 | K2 | K3 |
下列说法正确的是( )
A. 实验Ⅲ达平衡后,恒温下再向容器中通入lmolA和1molD,平衡不移动
B. 升高温度能加快反应速率的原理是降低了活化能,使活化分子百分数提高
C. 实验Ⅲ达平衡后容器内的压强是实验Ⅰ的![]() 倍
倍
D. K3>K2>K1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com