
科目: 来源: 题型:
【题目】下列说法不正确的是
A. 能使湿润的淀粉碘化钾试纸变蓝色的气体不一定是氯气
B. 铁丝能在氧气中燃烧,但不能在空气中燃烧
C. 二氧化硫和三氧化硫都是酸性氧化物,它们的水溶液都是强酸
D. 液溴应保存在磨口玻璃塞试剂瓶中,并加少量水进行水封
查看答案和解析>>
科目: 来源: 题型:
【题目】NaHSO4在水溶液中能够完全电离出H+、Na+、和SO42- 。下列对于NaHSO4的分类中不正确的是
A.NaHSO4是盐 B.NaHSO4是酸式盐
C.NaHSO4是钠盐 D.NaHSO4是酸
查看答案和解析>>
科目: 来源: 题型:
【题目】黄铜矿(CuFeS2)是炼铜的最主要矿物。火法冶炼黄铜矿的过程中,其中一步反应是;2Cu2O+ Cu2S![]() 6Cu+SO2。回答下列问题。
6Cu+SO2。回答下列问题。
(1)Cu+的价电子轨道表示式为__________________;Cu2O与Cu2S比较,熔点较高的是_______,原因为_____________________________________。
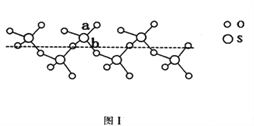
(2)SO2与SO3的键角相比,键角更大的是____________。将纯液态SO3冷却到289.8K时凝固得到一种螺旋状单链结构的固体,其结构如下图1所示。此固态SO3中S原子的杂化轨道类型是_______;该结构中S—O键长有两类,一类键长约140pm,另一类键长约为160pm,较短的键为_________(填图中字母)。
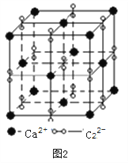
(3)离子化合物CaC2的一种晶体结构如下图2所示。写出该物质的电子式_____。从钙离子看,属于____________堆积;一个晶胞含有的π键平均有______个。

(4)奥氏体是碳溶解在γ—Fe中形成的一种间隙固溶体,无磁性,其晶胞如上图3所示,则该物质的化学式为________,若晶体密度为dg/cm3,则晶胞中最近的两个碳原子的距离为____________________ pm。(阿伏加德罗常数的值用NA表示,写出计算式即可)。
查看答案和解析>>
科目: 来源: 题型:
【题目】现有X,Y,Z,M四种元素均为短周期元素.有关信息如下表:
原子或分子结构、单质或化合物相关信息 | |
X | 含X元素的物质焰颜色反应为黄色 |
Y | 单质为双原子分子.若低温蒸发液态空气,因其沸点较低可先获得Y的单质 |
Z | Z元素原子易失去2个电子形成8电子结构的离子 |
M | M元素原子的最外层电子数是K层电子数的3倍,M与X处于同一周期 |
(1)X元素在周期表的位置是;
(2)1个Y单质分子中含对个共用电子对;
(3)Z能在CO2气体中燃烧,其化学反应方程式为 .
(4)化合物X2M溶液在空气中长期放置,与氧气反应会生成与过氧化钠的结构和化学性质相似的物质X2M2 , 其溶液显黄色.则X2M2的电子式为 , 用化学方程式表示X2M溶液在空气中的变质过程 .
查看答案和解析>>
科目: 来源: 题型:
【题目】元素X,Y,Z,M,N均为短周期主族元素,且原子序数依次增大.已知Y原子最外层电子数与核外电子总数之比为3:4;M原子的最外层电子数与次外电子数之比为3:4;N﹣与Ar原子电子层结构相同;X是短周期主族元素中原子半径最小的;Z是短周期主族元素中原子半径最大的;化合物XN常温下为气体.据此回答:
(1)N的最高价氧化物对应水化物的化学式是 .
(2)Z与M形成的化合物水溶液显碱性,其原因是(用离子方程式表示).
(3)X与Y,X与M均可形成18电子分子,这两种分子在水溶液中反应可观察到的现象是 , 反应的化学方程式是 .
(4)由X,Y,Z,M四种元素组成一种强酸的酸式盐,写出Ba(OH)2溶液中逐滴加入该盐溶液至中性的离子方程式 .
(5)Y,Z,N形成的化合物的水溶液中离子浓度的大小顺序是 .
(6)如图所示: 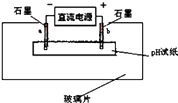
取一张用ZN溶液浸湿的pH试纸平铺在玻璃片上,取两根石墨棒做电极,接通直流电源.一段时间后,a电极处的pH试纸上可观察到的现象是 .
查看答案和解析>>
科目: 来源: 题型:
【题目】在密闭容器中,使1 mol N2和3 mol H2混合发生下列反应:N2 (g) + 3H2 (g)![]() 2NH3 (g) ΔH <0。
2NH3 (g) ΔH <0。
(1)达到平衡时, 充入N2并保持体积不变,平衡将______移动(填“正向”、“逆向”或“不”)。
(2)达到平衡时,充入氩气(Ar)并保持体积不变,平衡将______移动(同上)。
(3)达到平衡时,充入氩气(Ar),并保持压强不变,平衡将______移动(同上)。
(4)达到平衡时,将c(N2)、c(H2)、c(NH3)同时增大1倍,平衡______移动(同上)。
(5)保持体积不变,升高温度时,混和气体的平均相对分子质量______,密度_______(填“变大”、“变小”或“不变”)。
(6)当反应达到平衡时,N2和H2的浓度比是______;N2和H2的转化率比是______。
查看答案和解析>>
科目: 来源: 题型:
【题目】有A,B,C,D,E 5种元素,它们的核电荷数依次增大,且都小于20.其中C,E是金属元素;A和E属同一族,它们原子的最外层电子排布为ns1 . B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,C原子最外层上电子数等于D原子最外层上电子数的一半.请回答下列问题:
(1)A是 , B是 , C是 , D是 , E是 . (写元素符号)
(2)由这五种元素组成的一种化合物是(写化学式) . 写出该物质的一种主要用途. .
(3)用轨道表示式表示D元素原子的价电子构型 .
(4)元素B与D的电负性的大小关系是 , C与E的第一电离能的大小关系是 . (填>、<、﹦)
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:X,Y,Z,W为短周期元素,原子半径X:99pm Y:154pm Z:125pm W:117pm,X,Y,W位置如图所示(副族省略),X,Y,Z的最高价氧化物对应的水化物相互能反应,下列说法正确的是( ) 
A.元素Z处于周期表的阴影位置
B.非金属性:X>W
C.X与W形成化合物熔点很高,为离子化合物
D.Y,W的最高价氧化物对应的水化物能反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com