
科目: 来源: 题型:
【题目】酸雨是含硫氧化物或含氮氧化物随雨写降到地面形成的,主要由化石燃料的大量使用造成,酸雨的治理响应了十九大报告提出的保护环境的基本国策。
(1)煤燃烧烟尘中的锰、铁等可使SO2转化为SO3发生反应2SO2(g)+O2(g)=2SO3(g)。某温度下将2.0molSO2和1.0molO2充入2L密闭容器中,若反应达平衡后,SO2的平衡转化率为0.6,则该反应的平衡常数为______。若升高温度,平衡常数减小,则该反应的ΔH_______0(填“>”、“=”“<”)。
(2)高浓度SO2和NO2在浓雾天气下反应生成了两种物质,其中一种为亚硝酸(HNO2),该过程发生反应的化学方程式为_________。
(3)洗涤含SO2的烟气,可以减少SO2排放,以下物质的溶液可作洗涤剂的是______。
a.氨气 b.苏打 c.氨水 d.明矾
(4)汽车尾气中含有NOx和CO,已知气缸中生成NO的反应为:N2(g)+O2(g) ![]() 2NO(g),则在恒容密闭容器中,下列说法中能说明该反应达到平衡状态的是________。
2NO(g),则在恒容密闭容器中,下列说法中能说明该反应达到平衡状态的是________。
a.混合气体的压强保持不变
b.混合气体的平均相对分子质量保持不变
c.NO质量分数保持不变
d.氧气的浓度保持不变
e.N2和NO正反应速率之比为1:2
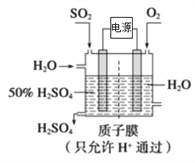
(5)SO2可以变废为宝,利学家研究出了用电化学原理生产硫酸的新工艺(如下图所示),其阳极的电极反应式为__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】SO2的催化氧化是工业制取硫酸的关键步骤之一,该反应的化学方程式为:2SO2+O2![]() 2SO3,
2SO3,
△H<0。请回答下列问题:
(1)判断该反应达到平衡状态的标志是__________(填字母)。
a.SO2和SO3浓度相等 b.SO2百分含量保持不变
c.容器中气体的压强不变 d.SO3的生成速率与SO2的消耗速率相等
(2)当该反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高SO2平衡转化率的
是______________(填字母)。
a.向装置中再充入N2 b.向装置中再充入O2
c.改变反应的催化剂 d.降低温度
(3)将0.050 mol SO2 (g)和0.030 mol O2 (g)放入容积为1L的密闭容器中,在一定条件下达到平衡,测得c(SO3) =0.040mol/L。计算该条件下反应的平衡常数K和SO2的转化率(不必写出计算过程)。
①平衡常数K=______________;
②平衡时,SO2的转化率α (SO2) =_____________。
(4)SO2尾气常用饱和Na2SO3溶液吸收,减少SO2气体污染并可得到重要的化工原料NaHSO3。己知NaHSO3溶液同时存在以下两种平衡:①HSO3-![]() SO32-+H+ ②HSO3-+H2O
SO32-+H+ ②HSO3-+H2O![]() H2SO3+OH-、常温下,0.1 mol/LNaHSO3溶液的 pH<7,则该溶液中 c (H2SO3)__________c (SO32-)(填“>”或“=”或“<”下同)。
H2SO3+OH-、常温下,0.1 mol/LNaHSO3溶液的 pH<7,则该溶液中 c (H2SO3)__________c (SO32-)(填“>”或“=”或“<”下同)。
查看答案和解析>>
科目: 来源: 题型:
【题目】氨化法是合成硫酰氯(SO2Cl2)的常用方法,实验室合成的酰氯的反应和实验装置如下所示:SO2(g)+Cl2(g) ![]() SO2Cl2(1) ΔH=-97.3KJ/mol。
SO2Cl2(1) ΔH=-97.3KJ/mol。

已知: 一般条件下,硫酰氯为无色气体,熔点为-541℃,沸点为69.1℃,在潮湿空气中会“发烟”;100℃以上开始分解,生成二氧化硫和氧气,长期放置会分解。
请回答下列问题:
(1)装置甲中,70%的硫酸体现的性质为_________。
(2)仪器己中盛放的试剂主要用于排气,该试剂最合适的是______(填名称);实验时,从仪器己中放出该试剂的操作方法是_________。
(3)①装置庚中的药品最合适的是________(填字母);
a.五氧化二磷 b. 碱石灰 c.无水氯化钙 d.硅胶
②装置丙的冷凝管中出水口是_______(填标号)
(4)活性炭的作用是____;若缺少装置乙和丁(均盛放浓硫酸),潮湿的氯气和二氧化硫发生反应的化学方程式是________。
(5)为提高本实验的硫酰氯的产率,在实验操作中还需要注意的有______。
a.控制气流速度,宜慢不宜快
b.保证装置的气密性良好
c.先向装置丙中通入一种气体,排出空气后再通入另一种气体
d.先通气体,再通冷凝水
查看答案和解析>>
科目: 来源: 题型:
【题目】某无色溶液甲中仅含有下列离子的几种( 不考虑水的电离以及离子的水解);
阳离子 | K+、Al3+、Fe3+、Ba2+、NH4+ |
阴离子 | Cl-、CO32-、HCO3-、SO42- |
取100mL溶液甲并分成两等份进行如下实验(假设每步完全反应):
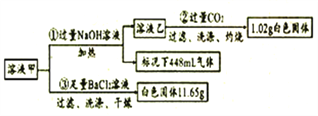
(1)由①可知,原溶液存在的离子有____,浓度为_____mol/L。
(2)写出实验②中生成沉淀的离子方程式_________。
(3)通入过量CO2充分反应后,需将反应后的混合溶液加热再过滤,其目的是_______。
(4)某同学通过分析认为该溶液中一定存在K+,其理由是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A、B、C、D、E为原子序数依次增大的五种短周期元素,A与B形成的共价化合物M的水溶液呈碱性,C原子的最内电子数是最外层电子数的2倍,D是同周期中单核离子半径最小的元素,E元素的最高正价与最低负价的代数和为6。请回答下列问题:
(1)化合物M的电子式为_________
(2)B、C所形成的简单离子中,半径较大的是________用离子符号表示)。
(3)E的单质与A的简单氧化物反应的离子方程式为________
(4)A、D形成的化合物DA3与水反应生成无色气体,则该反应的化学方程式为________,每生成1mol气体转移的电子数为_________。
(5)工业上,将CEO3与Na2SO3溶液混合,再加人转H2SO4制备净水剂EO2,则该反应的离子方程式为__________
(6)COA的水溶液和AE溶液反应,生成0.5mol水时放出的热量为28.65kJ,则该反应的热化学方程式为_________
查看答案和解析>>
科目: 来源: 题型:
【题目】pH=2的X,Y,Z三种酸的溶液各1mL,分别加水稀释到1 000mL,其pH与溶液体积(V)的变化关系如图所示,下列说法错误的是( ) 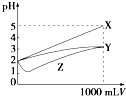
A.X是强酸,Y和Z是弱酸
B.稀释前的浓度大小为c(Z)>c(Y)>c(X)
C.稀释前电离程度大小为X>Y>Z
D.pH=2时,X,Y,Z都是稀溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是
A. 无色透明溶液中: Zn2+、SO42-、NH4+,Cl-
B. 0.1mol/L NaHCO3溶液中: Mg2+、Al3+、K+、NO3-
C. 能使甲基橙变黄的溶液中: Na+,CH3COO-、 MnO4-、 Fe3+
D. c(H+)/c(OH-)=1×1012的溶液中:NO3-、I-、K+、Fe2+
查看答案和解析>>
科目: 来源: 题型:
【题目】一定量CO2与足量C在体积可变的恒压密闭容器中发生反应:C(s)+CO2(g) ![]() 2CO(g),平衡时体系中气体体积分数与温度的关系如下图所示:
2CO(g),平衡时体系中气体体积分数与温度的关系如下图所示:

下列说法不正确的是
A. 550℃时,v逆小于925℃时v逆
B. 650℃时,反应达平衡后,CO2的转化率为25%
C. 由图中数据分析可得,该反应为放热反应
D. T℃时,若向平衡体系内充入惰性气体,化学平衡将向正反应方向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com