
科目: 来源: 题型:
【题目】1,4﹣戊二烯和X是有机合成的基础原料,用下列方法可以合成F如图1. 

(1)已知C与新制的氢氧化铜共热生成红色沉淀;X是分子中所有原子共平面的烃.则X的结构简式为 , X在一定条件下生成的高分子化合物的结构简式为 .
(2)①的反应类型是 , F中所含官能团的名称是 .
(3)1,4﹣戊二烯最多共面的碳原子数为 , 它的一种同分异构体为 ![]() ,该有机物的系统命名为 .
,该有机物的系统命名为 .
(4)与B互为同分异构体的T是有机合成的中间体,它的核磁共振氢谱如图2所示.则T的结构简式为 .
(5)反应②的化学方程式为 , 反应⑤生成物中除水外的无机物的化学式是 .
查看答案和解析>>
科目: 来源: 题型:
【题目】除去工业尾气中的氮氧化合物,常用氨催化吸收法,原理是NH3与NOx反应生成无毒物质.某同学在实验室里采用以下装置和步骤模拟工业上氮氧化合物的处理过程.
(1)Ⅰ.NH3的制取①若选择装置C制取氨气,则反应的化学方程式是 .
②若选择装置G制取氨气,固体用生石灰,则分液漏斗中盛放的液体试剂是 .
(2)Ⅱ.模拟尾气的处理选用上述部分装置,按下列顺序连接成模拟尾气处理装置,回答有关问题:
①装置A中反应的离子方程式为 . 反应过程中观察到的实验现象有铜片表面产生无色气体、铜片逐渐溶解、 .
②装置D中的液体可换成(填序号).
a.H2O b.CCl4 c.饱和食盐水 d.浓硫酸
③装置E中NO参加反应的化学方程式为 .
④该同学所设计的实验中存在的明显缺陷是 .
查看答案和解析>>
科目: 来源: 题型:
【题目】氢气是一种清洁能源,又是合成氨工业的重要原料.
(1)已知:CH4(g)+H2O(g)═CO(g)+3H2(g)△H=206.2kJmol﹣1CH4(g)+CO2(g)═2CO(g)+2H2(g)△H=247.4kJmol﹣1
甲烷和H2O(g)反应生成H2和CO2的热化学方程式为 .
(2)工业合成氨的反应原理为N2(g)+3H2(g)═2NH3(g)△H=﹣92.4kJmol﹣1 . 某温度下,把10mol N2与28mol H2置于容积为10L的密闭容器内,10min时反应达到平衡状态,测得氮气的平衡转化率为60%,则10min内该反应的平均速率v(H2)=molL﹣1min﹣1 , 则该温度下该反应的平衡常数K= . 欲增大氮气的平衡转化率,可采取的措施有(写一种措施即可).
(3)如图所示装置工作时均与H2有关. 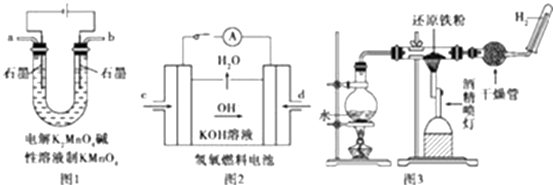
①图1所示装置中阳极的电极反应式为
②图2所示装置中,通入H2的管口是(选填字母代号).
③某同学按图3所示装置进行实验,实验结束后,将玻璃管内固体物质冷却后,溶于稀硫酸,充分反应后,滴加KSCN溶液,溶液不变红,再滴入新制氯水,溶液变为红色.该同学据此得出结论:铁与水蒸气反应生成FeO和H2 . 该结论(填“严密”或“不严密”),你的理由是(用离子方程式和必要的文字说明).
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组离子,在强碱性溶液中能大量共存的是( )
A. Na+、Ba2+、Cl-、SO42-B. Na+、Ba2+、AlO2-、NO3-
C. NH4+、K+、Cl-、NO3-D. Na+、K+、SiO32-、SO42-
查看答案和解析>>
科目: 来源: 题型:
【题目】将少量氯气通入KI溶液中,振荡,再加入CCl4,振荡,静置,观察到的现象是( )
A. 有紫黑色固体析出B. 形成均匀的紫红色溶液
C. 液体分层,下层紫红色D. 液体分层,上层紫红色
查看答案和解析>>
科目: 来源: 题型:
【题目】根据要求回答下列问题:
(1)生活中明矾常作净水剂,其净水的原理是________________________(用离子方程式表示)。
(2)已知MgO可溶于NH4Cl的水溶液,用化学方程式表示其原理________________________。
(3)去年8月12日晚,天津滨海新区危险品仓库发生爆炸事故,少量氰化物因爆炸冲击发生泄漏,CN一有剧毒,泄露会污染水源和空气,需要处理。
①已知HCN为一元弱酸,则NaCN溶液的pH _____________7(填“>”“=”或“<”),用离子方程式说明_____________________________。
②处理含CN一废水的方法之一是在微生物的作用下,CN-被氧气氧化成HCO3一,同时生成NH3,该反应的离子方程式为___________________________________________________。
(4)常温下,取0.2 mol·L-1 HCl溶液与0.2 mol·L-1 MOH溶液等体积混合,测得溶液混合后的pH=5,写出MOH的电离方程式:____________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某学生用0.2000mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作如下:
①用蒸馏水洗涤碱式滴定管,注入0.2000mol·L-1的标准NaOH溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴充满液体;
③调节液面至“ 0”或“0”刻度线稍下,并记下读数;
④量取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液;
⑤用标准液滴定至终点,记下滴定管液面读数;
⑥重复以上滴定操作2-3次;
请回答下列问题:
(1)以上步骤有错误的是(填编号)_____________,该错误操作会导致测定结果_________ (填“偏大”、“偏小”或“无影响”)。
(2)步骤④中,量取20.00mL待测液应使用________________ (填仪器名称),在锥形瓶装液前,留有少量蒸馏水,测定结果____________(填“大”、“偏小”或“无影响”)。
(3)步骤⑤滴定时眼睛应注视_______________________;判断到达滴定终点的依据是_______。
(4)以下是实验数据记录表
滴定次数 | 盐酸体积(mL) | NaOH溶液体积读数(mL) | |
滴定前 | 滴定后 | ||
1 | 20.00 | 0.00 | 18.10 |
2 | 20.00 | 0.00 | 16.30 |
3 | 20.00 | 0.00 | 16.22 |
从上表可以看出,第1次滴定记录的NaOH溶液体积明显多于后两次的体积,其可能的原因是(______)
A.滴定前滴定管尖嘴有气泡,滴定结束无气泡
B.锥形瓶用待测液润洗
C.NaOH标准液保存时间过长,有部分变质
D.滴定结束时,俯视读数
(5)根据上表记录数据,通过计算可得,该盐酸浓度为____________mol·L-1

(6)室温下,用0.100mol/L NaOH溶液分别滴定20.00mL0.100mol/L的盐酸和醋酸,滴定曲线如图所示,下列说法正确的是(______)
A.Ⅱ表示的是滴定醋酸的曲线
B.pH=7时,滴定醋酸消耗V(NaOH)小于20mL
C.V(NaOH) =20mL时,c( Cl- )=c(CH3COO- )
D.V(NaOH) =10mL时,醋酸溶液中:c( Na+ )> c(CH3COO-)> c( H+ )> c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com