
科目: 来源: 题型:
【题目】配制一定物质的量浓度的KOH溶液时,造成最终浓度偏低的原因可能是( )
A.容量瓶事先未烘干
B.定容时俯视观察液面
C.未用蒸馏水洗涤烧杯
D.定容后,摇匀时有少量液体流出
查看答案和解析>>
科目: 来源: 题型:
【题目】利用硫酸渣(主要含Fe2O3、FeO,杂质为Al2O3和SiO2等)生产铁基颜料铁黄(FeOOH)的制备流程如下:

(1)“酸溶”时,Fe2O3与硫酸反应的化学方程式为____。
(2)滤渣I的主要成分是FeS2、S和______(填化学式);Fe3+被FeS2还原的离子方程式为______。
(3)“氧化”中,生成FeOOH的离子方程式为_______________。
(4)滤液II中溶质是Al2(SO4)3和______(填化学式):“洗涤”时,检验铁黄表而已洗涤干净的操作是________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】锌锰电池(俗称干电池)在生活中的用量很大。两种锌锰电池的构造图如图(a)所示。
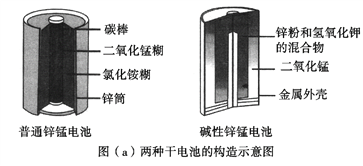
回答下列问题:
(1)普通锌锰电池放电时发生的主要反应为:Zn+2NH4Cl+2MnO2==Zn(NH3)2Cl2+2MnOOH
①该电池中,负极材料主要是________,电解质的主要成分是________,正极发生的主要反应是__________________________。
②与普通锌锰电池相比,碱性锌锰电池的优点有_____________________。(任写一条)
(2)图(b)表示回收利用废旧普通锌锰电池的一种工艺(不考虑废旧电池中实际存在的少量其他金属)。
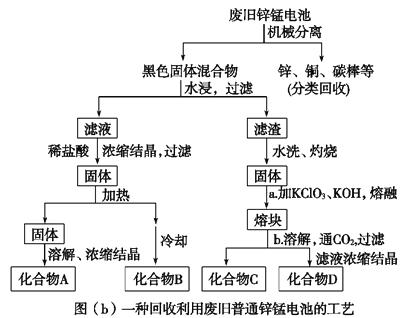
图(b)中产物的化学式分别为A_________________,B______________________。
(3)①操作a中得到熔块的主要成分是K2MnO4。操作b中,绿色的K2MnO4溶液反应后生成紫色溶液D和一种黑褐色固体C,该反应的离子方程式为_________________________。
②采用惰性电极电解K2MnO4溶液也能得到化合物D,则阴极处得到的主要物质是________。(填化学式)
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是实验室制取Na2S2O3·5H2O的装置图(略去部分夹持仪器)。
已知:Na2SO3 +S![]() Na2S2O3
Na2S2O3
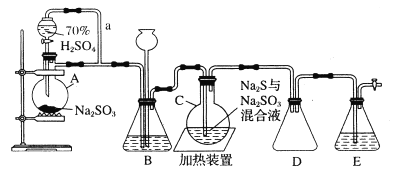
按要求回答下列问题:
(1)仪器A的名称是___________________。
(2)分液漏斗中用70%较浓硫酸的理由是___________________。
(3)装置C中生成S的离子反应方程式是___________________。
(4)E是SO2的尾气处理装置,则装置D的作用是___________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示是分离混合物时常用的仪器,从左至右,可以进行的混合物分离操作分别是( ) 
A.蒸馏、蒸发、萃取、过滤
B.蒸馏、过滤、萃取、蒸发
C.萃取、过滤、蒸馏、蒸发
D.过滤、蒸发、萃取、蒸馏
查看答案和解析>>
科目: 来源: 题型:
【题目】为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器己略去,气密性已检验)。
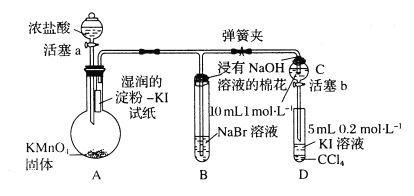
实验过程:
I.打开弹簧夹,打开活塞a,滴加浓盐酸。
II.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
III.当B中溶液由黄色变为红棕色时,关闭活塞a。
IV.……
(1)A中产生黄绿色气体的化学反应方程式是___________。
(2)验证氯气的氧化性强于碘的实验现象是___________。
(3)B中溶液发生反应的离子方程式是___________。
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作是___________,现象是___________。
(5)过程III实验的目的是___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】硫的化合物是常用的化工原料,但也是大气的主要污染物。综合治理其污染是环境化学当前的重要研究内容之一。
(1)一定温度下,将NH4HS固体放入定容真空容器中,可部分分解为硫化氢和氨气:NH4HS(s)![]() H2S(g)+NH3(g)
H2S(g)+NH3(g)
①可以判断上述分解反应已经达到化学平衡的是_____________(选填字母)
A. ![]() B.密闭容器中总压强不变
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变 D.密闭容器中氨气的体积分数不变
②当上述反应达平衡时:p(NH3)×p(H2S)=a(Pa2),则平衡时容器中的总压为_______________Pa(用含a的代数式表示);(p(NH3)、p(H2S)分别代表NH3、H2S的压强,Pa为压强的单位)
③实验测得不同温度下的平衡数据列于下表:
温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
平衡气体总浓度(×10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
④NH4HS分解反应的焓变△H_________0(填“>”、“=”或“<”)
下图是上述反应过程中生成物浓度随时间变化的示意图。若t2时增大氨气的浓度且在t3时反应再次达到平衡,请在图上画出t2时刻后硫化氢、氨气的浓度随时间的变化曲线.(要有必要标注)____________

(2)一定温度下,反应2SO2+O2![]() 2SO3,达到平衡时,n(SO2):n(O2):n(SO3)=2:3:4。缩小体积,反应再次达到平衡时,n(O2)=0.8mol,n(SO3)=1.4mol,此时SO2的物质的量应是____________。
2SO3,达到平衡时,n(SO2):n(O2):n(SO3)=2:3:4。缩小体积,反应再次达到平衡时,n(O2)=0.8mol,n(SO3)=1.4mol,此时SO2的物质的量应是____________。
(3)25℃,吸收液Na2SO3溶液在吸收SO2的过程中,pH随n(SO3- ):n(HSO3﹣)变化关系如下表:
n(SO32﹣):n(HSO3﹣) | 91:9 | 1:1 | 1:91 |
pH | 8.2 | 7.2 | 6.2 |
①当吸收液呈中性时,溶液中离子浓度关系正确的是:______(选填字母)
A.c(Na+)=2c(SO32- )+c(HSO3-)
B.c(Na+)> c(HSO3-)> c(SO32- )>c(H+)=c(OH-)
C.c(Na+)+c(H+)= c(SO32- )+ c(HSO3-)+c(OH-)
②当吸收液的pH降至约为6时,需送至电解槽再生。再生示意图如下,请写出HSO3- 在阳极放电的电极反应式是___________________。

(4)已知:CH4(g)+2O2(g) = CO2 (g) +2H2O (l) △H= - Q1 kJ/mol
2H2(g)+O2(g) = 2H2 O (g) △ H= - Q2 kJ/mol
2H2(g)+O2(g) =2H2 O (l) △ H= - Q3 kJ/mol,
常温下,取体积比4:1的甲烷和氢气的混合气体11.2L(标况),经完全燃烧恢复常温,放出的热为_______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组物质中,所含分子数相同的是( )
A.10g H2和10g O2
B.5.6L N2(标准状况)和22g CO2
C.9g H2O和0.5mol Br2
D.224mL H2(标准状况)和0.1mol N2
查看答案和解析>>
科目: 来源: 题型:
【题目】“84”消毒夜在日常生活中被广泛使用.该消毒液无色,pH大于7,对某些有色物质有漂白作用.你认为它可能的有效成分是( )
A.SO2
B.Na2CO3
C.氯水
D.NaClO
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定量的稀HNO3中慢慢加入铁粉,得到的Fe2+的物质的量(纵坐标)与所加铁粉的物质的量(横坐标)的关系如图所示。请将正确答案的序号填在相应的横线上。
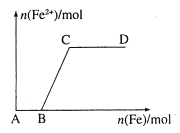
①Fe3+ ②Fe2+ ③Fe、Fe2+ ④Fe2+、Fe3+
(1)AB段铁元素以________形式存在。
(2)BC段铁元素以________形式存在。
(3)CD段铁元素以________形式存在。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com