
科目: 来源: 题型:
【题目】短周期元素A、B、C在周期表中的位置如下图所示,其中B、C元素的原子序数之和是A元素原子序数的4倍,则A、B、C是
A | ||
B | C |
A. B、Mg、Si B. Be、Na、Al C. O、P、Cl D. C、Al、P
查看答案和解析>>
科目: 来源: 题型:
【题目】微生物燃料电池是一种利用微生物将有机物中的化学能直接转化成电能的装置。如图是一种微生物燃料电池的工作原理示意图,下列有关说法不正确的是
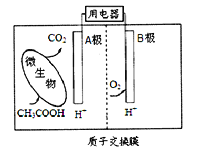
A. B电极是正极
B. 电池内H+从左侧向右侧迁移
C. A电极的电极反应式: CH3COOH + 8e-+ 2H2O=2CO2 +8H+
D. 该电池可利用有机废水等有机废弃物作为燃料
查看答案和解析>>
科目: 来源: 题型:
【题目】将一枚洁净的铁钉浸入稀硫酸中,下列叙述正确的是( )
①铁钉表面产生气泡 ②溶液由无色逐渐变为浅绿色 ③铁钉的质量减轻 ④溶液的质量减轻
A.②③B.①②④C.①②③D.①②③④
查看答案和解析>>
科目: 来源: 题型:
【题目】二氧化锰在生活和化学实验中有广泛应用。海底蕴藏着丰富的锰结核矿,其主要成分是MnO2。1991年由Allen等人研究,用硫酸淋洗后使用不同的方法可制备纯净的MnO2,其制备过程如下图所示:

(1)步骤Ⅰ中,试剂甲必须具有的性质是________(填序号)。
A.碱性 B.稳定性 C.氧化性 D.还原性
(2)用惰性材料作电极,电解硫酸锰溶液制二氧化锰,写出阳极反应式:_____________________。步骤Ⅲ中,以KClO3为氧化剂,当生成0.050 mol MnO2时,消耗0.10 mol·L-1的KClO3溶液200 mL,该反应的离子方程式为____________________________________________。
(3)用100 mL 12.0 mol·L-1的浓盐酸与足量MnO2混合后,加热,反应产生的氯气在标准状况下体积范围为________________。工业上可以用实验室制氯气的残余物质溶液吸收氯气,获得Mn2O3,Mn2O3广泛应用于电子工业、印染工业等领域。请写出该化学反应的离子方程式:__________________。
(4)二氧化锰是实验室制取氧气的催化剂。下列是某同学设计实验探究双氧水分解实验方案;
实验 | 20.0 mL双氧水溶液浓度 | 粉状MnO2 | 温度 | 待测数据 |
Ⅰ | 5% | 2.0 g | 20℃ | |
Ⅱ | 5% | 1.0 g | 20℃ | |
Ⅲ | 10% | 1.0 g | 20℃ | |
Ⅳ | ω | 2.0 g | 30℃ |
①实验Ⅱ和Ⅲ的结论是____________________________________________________。
②利用实验Ⅰ和Ⅳ探究温度对化学反应速率的影响,w=________。本实验待测数据是______。
查看答案和解析>>
科目: 来源: 题型:
【题目】I某课外小组模拟工业流程,设计了如下实验装置制备硝酸。
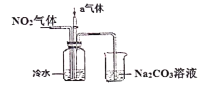
(1)通入的气体a是________(填化学式),通入a的目的是:_________。
(2)盛有Na2CO3溶液的烧杯为尾气处理装置,该装置中反应的化学方程式是: ______NO2+ ______Na2CO3+______ H2O= ______ NaNO2+ ______ + ______NaHCO3
(3)用N2O4代替NO2与水和a气体反应可生成硝酸,此反应的化学方程式是:_________________
Ⅱ按如图装置进行NH3性质实验。
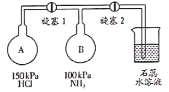
(4)先打开旋塞1,B瓶中的现象是_____________;原因是__________________。稳定后,关闭旋塞1。
(5)再打开旋塞2,B瓶中的现象是____________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】己知X、Y、Z都是金属,若把X浸入乙的盐溶液中,X的表面有乙析出;若X、Y和盐酸溶液形成原电池,Y为电池的负极。则X、Y、Z的金属活动顺序为
A. Y>X>Z B. X>Z>Y C. X>Y>Z D. Y>Z>X
查看答案和解析>>
科目: 来源: 题型:
【题目】氮的固定对人类的生存发展具有重要意义,科学家一直致力于“人工固氮”的新方法研究。
(1)豆科植物的根瘤菌含有一种固氮酶,能在常温下将空气中的氮气转化为自身生长所需的含氮化合物,下列说法错误的是________(填标号)。
a.固氮酶是一种蛋白质
b.固氮酶能降低固氮反应发生所需的能量
c.固氮酶能使固氮反应的平衡正向移动
d.固氮酶能加快固氮反应的速率
(2)合成氨是目前最重要的固氮方法。下图为合成氨反应N2(g)+3H2(g)![]() 2NH3(g)在不同温度和压强、使用相同催化剂条件下,初始时氮气、氢气的体积之比为1∶3时,平衡混合物中氨的体积分数的变化曲线如下图。
2NH3(g)在不同温度和压强、使用相同催化剂条件下,初始时氮气、氢气的体积之比为1∶3时,平衡混合物中氨的体积分数的变化曲线如下图。
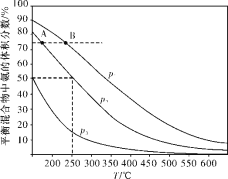
①A、B两平衡状态相比较,前者较大的是___________(填标号)。
a.平衡常数 b.平衡混合物的平均摩尔质量
c.氢气的转化率 d.从反应开始至达到平衡状态所需要的时间
②图中p1、p2、p3由大到小的顺序为_____________________。
③在250 ℃、p2下,H2的转化率为_____________%(结果保留小数点后一位)。
(3)据报道:在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3和一种单质。已知:①H2(g)+![]() O2(g)===H2O(l) ΔH1=-285.6 kJ/mol,②N2(g)+3H2(g)
O2(g)===H2O(l) ΔH1=-285.6 kJ/mol,②N2(g)+3H2(g)![]() 2NH3(g) ΔH2=-92.2 kJ/mol,写出此条件下氮气和水反应的热化学方程式:________________。
2NH3(g) ΔH2=-92.2 kJ/mol,写出此条件下氮气和水反应的热化学方程式:________________。
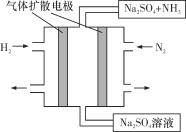
(4)下图为一种常温常压下水溶液中电化学合成氨的实验装置示意图。请据此写出其正极反应的电极反应式:_________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关加热操作正确的是( )
A.将烧杯放置在铁架台的铁圈上,直接用酒精灯火焰加热
B.将试管直接用酒精灯火焰加热
C.将蒸发皿放置在铁架台的铁圈上,并垫石棉网加热
D.将烧瓶放置在铁架台的铁圈上,直接用酒精灯火焰加热
查看答案和解析>>
科目: 来源: 题型:
【题目】已知反应C(s)+CO2(g)=2CO(g),下列措施能使其反应速率减小的是
A. 适当减少木炭的量 B. 将木炭块变为木炭粉
C. 加热反应物 D. 扩大反应容器的体积
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:25℃时 H2C2O4 的 pKa1=1.22,pKa2=4.19,CH3COOH 的 pK a=4.76,K 代表电离平衡常数,pK = -1gK。下列说法正确的是
A. 浓度均为 0.1mol·L-1NH4HC2O4 和 CH3COONH4 溶液中:c(NH4+)前者小于后者
B. 将 0.1mol·L-1 的 K2C2O4 溶液从 25℃升温至 35℃,c(K+)/c (C2O42-) 减小
C. 0.1 mol·L-1K2C2O4 溶液滴加盐酸至 pH=1.22:c(H+)-c(OH-)=c(Cl-)-3c(HC2O4-)
D. 向 0.1 mol·L-1CH3COONa 溶液中滴加少量 0.1 mol·L-1H2C2O4 溶液:CH3COO- + H2C2O4 = CH3COOH + HC2O4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com