
科目: 来源: 题型:
【题目】下列说法正确的是
A. 根据反应Cu+H2SO4![]() CuSO4+H2↑可推出Cu的还原性比H2的强
CuSO4+H2↑可推出Cu的还原性比H2的强
B. 电解含Pb(NO3)2和Cu(NO3)2的溶液,阴极上阳离子得电子次序依次是Cu2+、H+、Pb2+
C. 含amolNa2S的溶液最多能吸收2.5amol的二氧化硫气体(不考虑SO2在水中的溶解)
D. 由置换反应I2+2NaClO3===2NaIO3+Cl2可知I2的氧化性强于Cl2的氧化性
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中正确的是( )
A.金属只有正价,非金属只有负价
B.氟无正价,氧无最高正价
C.主族元素的最高正价等于其原子最外层电子数
D.同周期元素的最外层电子数越多,原子半径越大
查看答案和解析>>
科目: 来源: 题型:
【题目】硬脂酸甘油酯在NaOH的重水(D2O)溶液中加热水解,其产物是( )
A.C17H35COOD,CH2ODCHODCH2OD
B.C17H35COONa,CH2ODCHODCH2OD,HOD
C.C17H35COONa,CH2OHCHOHCH2OH,HOD
D.C17H35COONa,CH2ODCHODCH2OD,H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】如下图所示,A、F为石墨电极,B、E为铁片电极。按要求回答下列问题。

(1)打开K2,合并K1。B为________极,A的电极反应为________________________。最终可观察到的现象是___________________________________________。
涉及的化学反应方程式有_______________________________。
(2)打开K1,合并K2。E为________极,F极的电极反应为_____,检验F极产生气体的方法是____________________________。
(3)若往U形管中滴加酚酞,进行(1)(2)操作时,A、B、E、F电极周围能变红的是________,原因是___________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】铁除去废水中硝酸盐已成为环境修复研究的热点之一。某课题组拟探究影响铁除去硝酸盐速率的外界因素,设计如下实验方案:
实验 | 2 g 铁形状 | 0.1 mol·L-1 的KNO3溶液 | 0.1 mol·L-1 H2SO4溶液 | 蒸馏 水体积 | 恒温 水浴 | 1 h NO 除去率 |
1 | 粉末 | 20 mL | 20 mL | 0 | 20 ℃ | a |
2 | 颗粒 | 20 mL | 20 mL | 0 | 20 ℃ | b |
3 | 粉末 | 20 mL | 10 mL | V mL | 20 ℃ | c |
4 | 粉末 | 20 mL | 20 mL | 0 | 30 ℃ | d |
回答下列问题:
(1)在pH=2.5的废水中,24 h后,铁粉使![]() 除去率约100%,产物为Fe3O4、
除去率约100%,产物为Fe3O4、![]() 。写出该反应的离子方程式:_________________________________________________。
。写出该反应的离子方程式:_________________________________________________。
(2)上述实验中,V=________,理由是_____________________。
(3)由表中数据可知,a________b(填“>”“<”或“=”)。
(4)若a>c,可得出的结论是______________________________。
(5)设计实验1和实验4的目的是______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】实现 “节能减排” 和“低碳经济”的一项重要课题就是如何将CO2转化为可利用的资源。目前工业上有一种方法是用CO2来生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),下图1表示该反应过程中能量(单位为kJ·mol-1)的变化:
CH3OH(g)+H2O(g),下图1表示该反应过程中能量(单位为kJ·mol-1)的变化:
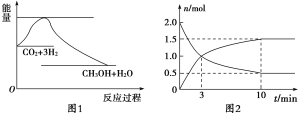
(1)为探究反应原理,现进行如下实验,在体积为2 L的密闭容器中,充入2 mol CO2和8 mol H2,一定条件下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如上图2所示。
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如上图2所示。
①从反应开始到平衡,CH3OH的平均反应速率v(CH3OH) =________;
②该反应的平衡常数表达式K=________。
(2)830 ℃,反应的平衡常数K=1,在恒容反应器中发生上述反应,按下表中的物质的量投入反应混合物,其中向正反应方向进行的有________(填“A”“B”“C”或“D”)。
物质 | A | B | C | D |
n(CO2) | 3 | 1 | 3 | 1 |
n(H2) | 2 | 2 | 4 | 2 |
n(CH3OH) | 1 | 2 | 3 | 0.5 |
n(H2O) | 4 | 2 | 3 | 2 |
(3)25 ℃,1.01×105Pa时,16g液态甲醇完全燃烧,当恢复到原状态时,放出363.3 kJ的热量,写出该反应的热化学方程式______________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】将铁粉和铜粉的均匀混合物平均分成四等份,分别加入同浓度的稀硝酸,充分反应,在标准状况下生成NO的体积和剩余金属的质量如下表(设硝酸的还原产物只有NO)。下列计算结果正确的是
编号 | ① | ② | ③ | ④ |
硝酸体积/mL | 100 | 200 | 300 | 400 |
剩余金属/g | 18.0 | 9.6 | 0 | 0 |
NO体积/L | 2.24 | 4.48 | 6.72 | V |
A. ①中溶液存在Fe3+ B. 硝酸的浓度为4mol/L
C. ②中溶解了9.6gCu D. ④中V=6.72
查看答案和解析>>
科目: 来源: 题型:
【题目】各式各样电池的迅速发展是化学对人类的一项重大贡献。下列有关电池的叙述正确的是()
A.手机上用的锂离子电池属于一次电池。B.锌锰干电池中,锌电极是负极
C.氢氧燃料电池工作时氢气在负极上被还原D.太阳能电池的主要材料是高纯度的二氧化硅
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com