
科目: 来源: 题型:
【题目】Ⅰ.有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6 mol·L-1的H2SO4溶液中,乙同学将电极放入6 mol·L-1的NaOH溶液中,如图所示。

(1)写出甲中正极的电极反应式:____。
(2)乙中负极为__,总反应的离子方程式:___。
(3)由此实验得出的下列结论中,正确的有____。
A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质
B.镁的金属性不一定比铝的金属性强
C.该实验说明金属活动性顺序表已过时,没有实用价值了
D.该实验说明化学研究对象复杂、反应受条件影响较大,因此应具体问题具体分析
Ⅱ.化学电池在通信、交通及日常生活中有着广泛的应用。目前常用的镍镉(NiCd)电池,其电池总反应可以表示为:Cd+2NiO(OH)+2H2O![]() 2Ni(OH)2+Cd(OH)2已知Ni(OH)2和Cd(OH)2均难溶于水但能溶于酸,以下说法正确的是____(填字母序号)。
2Ni(OH)2+Cd(OH)2已知Ni(OH)2和Cd(OH)2均难溶于水但能溶于酸,以下说法正确的是____(填字母序号)。
①放电时Cd作正极 ②放电时Ni元素被还原
③充电时化学能转变为电能 ④放电时化学能转变为电能
Ⅲ.氢气和氧气可形成氢氧燃料电池。通常氢氧燃料电池有酸式(当电解质溶液为硫酸时)和碱式(当电解质溶液为NaOH(aq)或KOH(aq)时)两种。试回答下列问题:
(1)酸式电池的电极反应:正极_____;
(2)碱式电池的电极反应:负极_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】以苯为基础原料,可以合成多种有机物。

回答下列问题:
(1)由苯合成有机物A用到的无机试剂为______________
(2)B分子中的官能团的名称为__________,生成PF树脂的反应类型为_____________
(3)由B生成C的化学方程式为_____________
(4)试剂D可以是___________________(填代号)
a.溴水 b.高锰酸钾溶液 c.Ag(NH3)2OH溶液 d.新制Cu(OH)2悬浊液
(5)写出同时满足下列条件的肉桂酸乙酯的一种同分异构体________________
①苯环上仅有2个取代基且处于对位
②能发生水解反应和银镜反应,其中一种水解产物遇FeCl3溶液显紫色
③为顺式异构
(6)以乙醇为原料合成CH3-CH=CH-COOCH2CH3,其他试剂任选,写出合成路线_____________
查看答案和解析>>
科目: 来源: 题型:
【题目】齐墩果酸临床用于治疗传染性急性黄疸型肝炎,其结构简式如图所示,下列说法不正确的是

A. 齐墩果酸能使酸性KMnO4溶液褪色 B. 齐墩果酸能和NaHCO3溶液反应产生气体
C. 齐墩果酸分子间能形成酯 D. 齐墩果酸能发生加成反应、取代反应、水解反应
查看答案和解析>>
科目: 来源: 题型:
【题目】将气体A、B置于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g)![]() 2C(g)+2D(g),反应进行到10 s末达到平衡,此时测得A的物质的量为1.8 mol,B的物质的量为0.6 mol,C的物质的量为0.8 mol。
2C(g)+2D(g),反应进行到10 s末达到平衡,此时测得A的物质的量为1.8 mol,B的物质的量为0.6 mol,C的物质的量为0.8 mol。
(1)用C表示10 s内反应的平均反应速率为________。
(2)10 s末,生成物D的浓度为________。
(3)A与B的平衡转化率之比为________。
(4)反应过程中容器内气体的平均相对分子质量变化是_____(填“增大”、“减小”或“不变”,下同),气体的密度变化是______。
(5)在一定温度下,体积不变的密闭容器中,上述反应达到平衡的标志是_______(填字母)。
A. 气体总质量保持不变 B. A、B、C、D的浓度都相等
C. 每消耗3 mol A的同时生成2 mol D D. A、B、C、D的分子数之比为3∶1∶2∶2
E. 3V正(A) = 2V逆(C) F. A的转化率保持不变
查看答案和解析>>
科目: 来源: 题型:
【题目】某科研小组公司开发了Li-SO2Cl2军用电池,其示意图如图所示,已知电池总反应为:2Li+ SO2Cl2= 2LiCl+SO2↑。下列叙述中错误的是( )
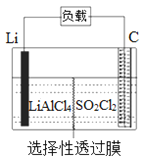
A. 电池工作时负极材料是Li,发生氧化反应
B. 电池工作时电子流向:锂电极→导线→负载→碳棒
C. 电池工作过程中,石墨电极反应式为SO2Cl2+2e-=2Cl-+SO2↑
D. 电池工作时,外电路流过0.2 mol电子,生成2.24 L气体
查看答案和解析>>
科目: 来源: 题型:
【题目】瓷器(英文名为________)成了中华民族文化的象征之一;作为陶瓷的故乡,我国陶都________的陶器和瓷都________的瓷器,在世界上都享有盛誉.
查看答案和解析>>
科目: 来源: 题型:
【题目】随着现代工业的发展,能源问题已经越来越引起人们的重视。科学家预言,未来最理想的燃料是绿色植物,即将植物的秸秆(主要成分是纤维素)用适当的催化剂水解成葡萄糖,再将葡萄糖转化为乙醇,用作燃料。
(1)写出绿色植物的秸秆转化为乙醇的化学方程式:
①____________________________________________;
②____________________________________________。
(2)乙醇除用作燃料外,还可以用它合成其他有机物。如图主要是以乙醇为起始原料的转化关系图,请在图中填上相应物质的结构简式___________________________。
![]()

(3)写出上面转化关系图中由CH2OHCH2OH![]() C4H4O4的化学方程式 (有机物用结构简式表示)________________________________________________________________。
C4H4O4的化学方程式 (有机物用结构简式表示)________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】一定量的甲烷在O2不足的情况下燃烧,得到CO、CO2和H2O的总质量为14.4 g,若其中水的质量为7.2 g,则CO的质量是 ( )。
A. 2.8 gB. 4.4 gC. 5.6 gD. 在2.8 g~5.6 g之间
查看答案和解析>>
科目: 来源: 题型:
【题目】周期表前四周期的元素A、B、C、D、E、F,原子序数依次增大,A是周期表中原子半径最小的元素,B的基态原子中只有1个未成对电子,C基态原子中有7种不同运动状态的电子,D的最外层电子数是其所处周期数的3倍,E与D同主族,F的一价阳离子最外层有18个电子。回答下列问题:
(1)F在周期表中的位置是_____________,它的基态原子的电子排布式为_____________
(2)A元素与其他元素形成的含氧酸中,酸根呈三角锥结构的酸是_________,该酸的中心原子的杂化方式为_________
(3)CA3极易溶于水,试从下图中判断CA3溶于水后形成CA3·H2O的合理结构为_____(填字母代号),推理依据是___________

(4)元素B可形成H3BO3,已知H3BO3的电离方程式为H3BO3+2 H2O![]() [B(OH)4]一+H3O+
[B(OH)4]一+H3O+
①基态B、D原子的第一电离能由小到大的顺序为__________(用元素符号表示)
②[B(OH)4]一中B原子的杂化类型为_______________
③写出一种与H3O+互为等电子体的分子的化学式:___________
④H3BO3晶体在热水中的溶解度大于冷水中的溶解度的原因为__________________
查看答案和解析>>
科目: 来源: 题型:
【题目】新型纳米材料氧缺位铁酸盐(MFe2Ox)(3<x<4;M表示Mn、Co、Zn或Ni的二价离子),常温下,它能使工业废气中的SO2、NO2等氧化物转化为单质。转化流程如图所示,下列有关该转化过程的叙述正确的是

A. MFe2O4表现了还原性
B. 若MFe2Ox 与H2发生反应的物质的量之比为2∶1,则x=3.5
C. 在该反应中每有1molNO2的废气被处理将转移电子数4NA个
D. SO2的还原性大于MFe2Ox
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com