
科目: 来源: 题型:
【题目】常温下,二氯化二硫(S2Cl2)是橙黄色有恶臭的液体,它的分子结构与H2O2相似,熔点为193K,沸点为411K,遇水水解产生的气体能使品红褪色。下列有关说法正确的是
A. S2Cl2晶体中存在离子键
B. S2Cl2在熔融状态下能导电
C. S2Cl2分子中各原子均达到8电子稳定结构
D. S2Cl2与水反应后生成的气体难溶于水
查看答案和解析>>
科目: 来源: 题型:
【题目】以下说法中正确的是( )
A.所有△H<0的反应均是自发反应 B.自发进行的反应一定能迅速进行
C.冰在室温下自动熔化成水,是熵增的过程 D.高锰酸钾加热分解是一个熵减小的过程
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:稀Na3AsO3溶液、稀碘水和稀NaOH溶液混合,发生如下反应:AsO33- (aq)+I2(aq)+2OH-(aq)![]() AsO43-(aq)+2I-(aq)+H2O(l) ,反应一段时间后测得c(AsO43-)为a mol·L-1。下列说法能判断反应达到平衡状态的是
AsO43-(aq)+2I-(aq)+H2O(l) ,反应一段时间后测得c(AsO43-)为a mol·L-1。下列说法能判断反应达到平衡状态的是
A. c(I) = 2a mol·L-1B. v(I-) = 2v(AsO33-)
C. c(AsO43-)/c(I)不再变化D. 溶液的pH不再变化
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)某小组的同学欲探究NH3经一系列反应得到HNO3和NH4NO3的过程,NH3的转化过程如下图所示。
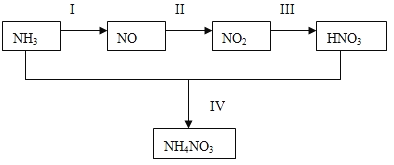
甲、乙两同学分别按下图所示装置进行实验。用于A、B装置中的可选药品:浓氨水、30%H2O2溶液、蒸馏水、NaOH固体、MnO2
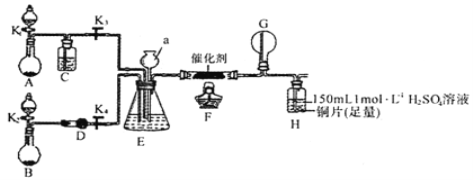
①装置A的圆底烧瓶中发生反应的化学方程式为__________。装置E有多种作用,下列关于装置E的作用或其中所盛液体的说法中,不正确的是_________(填下列序号字母)。
a.使氨气和氧气充分混合 b.控制通入氨气和氧气的体积比
c.平衡装置内的压强 d.锥形瓶内液体是饱和食盐水
②甲同学先点燃酒精灯,再打开K1、K2、K3、K4,反应一段时间后,成功模拟了反应过程,并将实验中产生的气体持续通入装置H一段时间后,H中的溶液变成蓝色,则其中铜片所参与反应的离子方程式为_______,若制得的氨气仅按I→Ⅱ→III的顺序完全转化为硝酸,欲使H装置中所得溶液为纯净的CuSO4溶液(忽略Cu2+的水解),理论上所需氨气在标准状况下的体积为______L(假设硝酸与铜反应产生的还原产物全部排出反应装置);
③乙同学为模拟过程IV的反应,在甲同学操作的基础上对该装置进行了下列各项中的一项操作,使G处圆底烧瓶中产生大量白烟,你认为这项操作是_________(填下列序号字母)。
a.关闭K3并熄灭酒精灯 b.关闭K4并熄灭酒精灯 c.关闭K3、K4并熄灭酒精灯
④丙同学认为该系列实验装置存在一处明显的设计缺陷,你认为该设计缺陷是__________。
(2)实验室可用铜和浓硫酸加热或硫酸和亚硫酸钠反应制取二氧化硫。
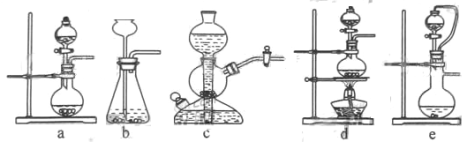
①如果用硫酸和亚硫酸钠反应制取二氧化硫,并希望能控制反应速度,上图中可选用的发生装置是 _____(填写字母)。
②若用硫酸和亚硫酸钠反应制取3.36L(标准状况)二氧化硫,如果已有40%亚硫酸钠(质量分数),被氧化成硫酸钠,则至少需称取该亚硫酸钠 _______ g(保留一位小数)。
③某热电厂上空大气中所含二氧化硫严重超标,现对该区域雨水样品进行探究。首先用pH试纸测定雨水样品的pH,操作方法为_______________,测得样品pH约为3;为进一步探究由SO2所形成酸雨的性质,将一定量的SO2通入蒸馏水中,配成pH为3的溶液,然后将溶液分为A、B两份,将溶液B久置于空气中,与密闭保存的A相比,久置后的溶液B中水的电离程度将_______(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是以芳香烃A为原料合成有机高分子化合物甲和乙的路线图。
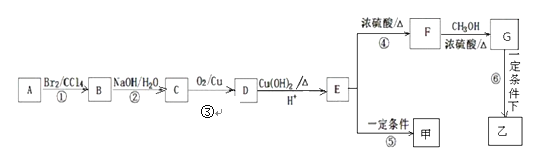
已知:①下图是A通过检测所得的质谱图,A分子中有5种不同化学环境的氢原子,它们的个数比为1:2:2:2:3;②甲乙均为有机高分子化合物;③A的分子结构中苯环上只有一个取代基。
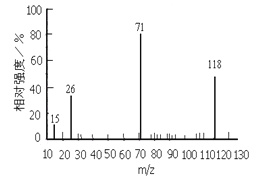
请根据信息,回答下列问题:
(1)A的化学式为______;
(2)C中所含官能团的名称是_____;
(3)反应④的反应类型为_____;
(4)甲的结构简式为______;
(5)写出有关反应的化学方程式:③的反应方程式__________,⑥的反应方程式__________;
(6)含有苯环、与F具体相同官能团的F的同分异构体有____种(不考虑立体异构、不含F),其中核磁共振氢谱为5组峰,面积比为2:2:2:1:1的为_____(写结构简式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】对CH4与CH3CH3的叙述错误的是
A. CH4与CH3CH3互为同系物
B. CH4与Cl2在光照下反应有四种产物
C. CH4与Cl2在光照下反应属于取代反应
D. CH3CH3与Cl2在光照下可以发生反应CH3CH3+Cl2![]() CH3CH2Cl+HCl
CH3CH2Cl+HCl
查看答案和解析>>
科目: 来源: 题型:
【题目】结构化学从原子、分子水平上帮助我们认识物质构成的规律;以微粒之间不同的作用力为线索,研究不同类型物质的有关性质;从物质结构决定性质的视角预测物质的有关性质。
(1)下列说法正确的是 ______(填字母)。
A、元素电离能由大到小的顺序:O>N>C
B、一个尿素(CO(NH2)2)分子中含1个π键和7个σ键
C、氯化钠和氯化铯晶体具有相同的晶胞
(2)根据等电子体原理,羰基硫(OCS)分子的电子式应为______。光气(COCl2)分子内各原子最外层都满足8电子稳定结构,则光气分子的空间构型为____(用文字描述)。
(3)Cu2+基态的电子排布式为______。将硫酸铜溶液蒸发浓缩后降温结晶,析出蓝色晶体,取25.0g晶体置于坩埚中在一定温度下灼烧,测得剩余固体质量始终保持为23.2g,进一步升高灼烧温度,固体变为白色且质量为16.0g,已知该晶体属于配合物(配合物的内界结构比较稳定),推测其合理的化学式可以表示为______。
(4)通常情况下,溶液中的Fe3+比Fe2+稳定,理由是______。
查看答案和解析>>
科目: 来源: 题型:
【题目】第四周期中的18种元素具有重要的用途,在现代工业中备受青睐。
(1)铬是一种硬而脆,抗腐蚀性强的金属,常用于电镀和制造特种钢,基态Cr原子中,电子占据最高能层的符号为___,该能层上具有的原子轨道数为___。
(2)第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的,30Zn与31Ga的第一电离能是否符合这一规律?___(填“是”或“否”),原因是______________(如果前一问填“是”,此问可以不答)。
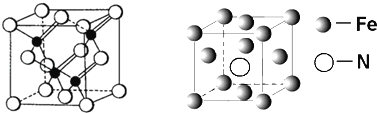
(3)镓与第VA族元素可形成多种新型人工半导体材料,砷化镓(GaAs)就是其中一种,其晶体结构如下图所示(白色球代表As原子).在GaAs晶体中,每个Ga原子与____个As原子相连,与同一个Ga原子相连的As原子构成的空间构型为_____;
(4)与As同主族的短周期元素是N、P.AsH3中心原子杂化的类型为____;一定压强下将AsH3、NH3和PH3的混合气体降温时首先液化的是_______,理由是__________;
(5)铁的多种化合物均为磁性材料,氮化铁是其中一种,某氮化铁的晶胞结构如图所示,则氮化铁的化学式为________;设晶胞边长为acm,阿伏加德罗常数为NA,该晶体的密度为__g.cm﹣3(用含a和NA的式子表示)
查看答案和解析>>
科目: 来源: 题型:
【题目】化学原理是中学化学学习的重要内容。请回答下列问题:
(1)①己知:CH4、H2的燃烧热(△H)分别为﹣890.3kJ/mol、﹣285.8kJ/mol,则CO2和H2反应生成CH4的热化学方程式是__________________________。
②有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示,电池正极的电极反应式是________,A是____。

(2)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上可用合成气制备甲醇,反应为CO(g)+2H2(g)![]() CH3OH(g),某温度下在容积为2L的密闭容器中进行该反应,其相关数据见图:
CH3OH(g),某温度下在容积为2L的密闭容器中进行该反应,其相关数据见图:

①从反应开始至平衡时,用CO表示化学反应速率为________,该温度下的平衡常数为__;
②5min至10min时速率变化的原因可能是__________________;
(3)①常温下,将V mL、0.1000mol/L氢氧化钠溶液逐滴加入到20.00mL、0.1000mol/L醋酸溶液中,充分反应(忽略溶液体积的变化);如果溶液pH=7,此时V的取值___20.00(填“>”、“=”或“<”),溶液中c(Na+)、c(CH3COO﹣)、c(H+)、c(OH﹣)的大小关系是_____________________;
②常温下,将a mol/L的醋酸与b mol/L的氢氧化钠溶液等体积混合,反应后,溶液呈中性,则醋酸的电离常数为_______(用含有a、b字母的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com