
科目: 来源: 题型:
【题目】实验室用有机含碘(主要以I2和IO3-的形式存在)废水制备单质碘的实验流程如下:

已知:Ⅰ.碘的熔点为113 ℃,但固态的碘可以不经过熔化直接升华;
Ⅱ.粗碘中含有少量的Na2SO4杂质。
下列说法正确的是
A. 操作①和③中的有机相从分液漏斗上端倒出
B. 操作②中发生反应的离子方程式为IO3-+3SO32-===I-+3SO42-
C. 操作④为过滤
D. 操作⑤可用如图所示的水浴装置进行
查看答案和解析>>
科目: 来源: 题型:
【题目】将下列各组物质,按单质、氧化物、酸、碱、盐分类顺序排列正确的是( )
A.银、二氧化硫、硫酸、烧碱、食盐
B.碘酒、冰、硫酸氢钠、烧碱、碳酸钙
C.氢气、干冰、硝酸、烧碱、硝酸钾
D.铜、氧化铜、醋酸、石灰水、碳酸氢钠
查看答案和解析>>
科目: 来源: 题型:
【题目】由CO2、CO、H2组成的混合气体在同温同压下与氮气的密度相同,则该混合气体中CO2、H2、CO的体积比可为( )
A. 13∶8∶29B. 22∶1∶14
C. 29∶8∶13D. 13∶16∶57
查看答案和解析>>
科目: 来源: 题型:
【题目】在0.1 molL1CH3COOH溶液中存在如下电离平衡:CH3COOH![]() CH3COO- + H+,对于该平衡,下列叙述正确的是
CH3COO- + H+,对于该平衡,下列叙述正确的是
A. 加热,平衡向逆反应方向移动
B. 加入少量0.05 molL﹣1 H2SO4溶液,溶液中c(H+)不变
C. 加入少量NaOH固体,平衡向正反应方向移动
D. 加入少量水,水的电离平衡不移动
查看答案和解析>>
科目: 来源: 题型:
【题目】Na2FeO4是制造高铁电池的重要原料,同时也是一种新型的高效净水剂。在工业上通常利用如图装置生产Na2FeO4,下列有关说法不正确的是

A. 右侧电极反应方程式:Fe+8OH--6e-=FeO42-+4H2O
B. 左侧为阳离子交换膜,当Cu电极生成1mol气体时,有2molNa+通过阳离子交换膜
C. 可以将左侧流出的氢氧化钠补充到该装置中部,以保证装置连续工作
D. Na2FeO4具有强氧化性且产物为Fe3+,因此可以利用Na2FeO4除去水中的细菌、固体颗粒以及Ca2+等
查看答案和解析>>
科目: 来源: 题型:
【题目】以下关于甲烷的说法中错误的是( )
A. 甲烷化学性质比较稳定,不被任何氧化剂氧化
B. 甲烷分子具有正四面体结构
C. 甲烷分子中具有极性键
D. 甲烷分子中四个C﹣H键是完全相同的键
查看答案和解析>>
科目: 来源: 题型:
【题目】36.5g氯化氢溶解在1L水中(水的密度近似为1g·mL-1),所得溶液的密度为ρg·mL-1,质量分数为w,物质的量浓度为cmol·L-1,NA表示阿伏加德罗常数的值,则下列叙述正确的是( )
A. 所得溶液的物质的量浓度为1mol·L-1B. 36.5g氯化氢含有NA个原子
C. 36.5gHCl气体占有的体积约为22.4LD. 所得溶液的质量分数w=36.5c/1000ρ
查看答案和解析>>
科目: 来源: 题型:
【题目】某学生设计如图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应)。请回答下列问题:
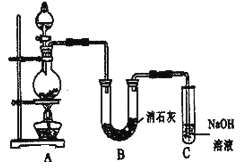
(1)A、B中的反应物分别是浓盐酸和MnO2。写出所发生的化学方程式__________,进入装置C的气体中所含杂质是_____、_____。
(2)漂白粉的有效成分是____(填化学式);D中所发生的化学反应的离子方程式是_______。
(3)此实验所得漂白粉的Ca(ClO)2产率偏低。该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应: ①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是__。②为避免另一副反应的发生,应采取的措施是________。
(4)若将该实验中残留的Cl2,缓慢通入KI溶液至过量,则溶液先变黄后变无色,且可检测到HIO3;写出并配平该“变无色”反应的化学方程式:________,若将KI改为KBr溶液,则溶液变为__色,未检测到HBrO3的存在。由上述事实推测,Cl2、HIO3、HBrO3的氧化性由强到弱的次序是______。
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物Z是合成平喘药沙丁胺醇的中间体,可通过下列路线制得:

下列说法正确的是
A. 1 mol Z最多能与2 mol NaOH反应
B. Y可以发生取代反应、氧化反应、消去反应
C. 可用FeCl3溶液鉴别Y和Z
D. X分子中所有原子在同一平面上
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,稀盐酸和氨水按不同体积比混合得到四种溶液,各取20mL溶液,用0.1molL﹣1NaOH溶液滴定,溶液的pH随NaOH溶液的体积变化如图所示,下列说法正确的是( )

A. 滴至pH=7时,四种溶液中均存在c(Na+)=c(Cl﹣)
B. 原盐酸的浓度是0.1molL﹣1
C. V(NaOH)=10mL,溶液中Na+浓度a>b
D. 当V(NaOH)>20mL时,四种溶液的pH相同,溶液中的NH4+浓度近似相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com