
科目: 来源: 题型:
【题目】25℃时,改变0.1mol/L弱酸RCOOH溶液的pH,溶液中RCOOH分子的物质的量分数δ(RCOOH)随之改变[已知![]() ,甲酸(HCOOH)]与丙酸(CH3CH2COOH)溶液中δ(RCOOH)与pH的关系如图所示。下列说法正确的是
,甲酸(HCOOH)]与丙酸(CH3CH2COOH)溶液中δ(RCOOH)与pH的关系如图所示。下列说法正确的是

A. 图中M、N两点对应溶液中的c(OH-)比较:前者>后者
B. 丙酸的电离常数K=10-4.88
C. 等浓度的HCOONa和CH3CH2COONa两种溶液的pH比较:前者>后者
D. 将0.1 mol/L的HCOOH溶液与0.1 mol/L的HCOONa溶液等体积混合,所得溶液中:c(Na+)>c(HCOOH)>c(HCOO-)>c(OH-)>c(H+)
查看答案和解析>>
科目: 来源: 题型:
【题目】利用CO和H2在催化剂的作用下合成甲醇,发生的反应如下:CO(g)+2H2(g)![]() CH3OH(g),在体积一定的密闭容器中按物质的量之比1:2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。下列说法正确的是
CH3OH(g),在体积一定的密闭容器中按物质的量之比1:2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。下列说法正确的是

A. 该反应的△H<0,且p1<p2
B. 反应速率:ν逆(状态A)>ν逆(状态B)
C. 在C点时,CO转化率为75%
D. 在恒温恒压条件下向密闭容器中充入不同量的CH3OH,达平衡时CH3OH的体积分数也不同
查看答案和解析>>
科目: 来源: 题型:
【题目】汽车尾气的治理是减轻空气污染的有效途径。科学家研究发现TiO2的混凝土或沥青可以适度消除汽车尾气中的氮氧化物,其原理如下。下列关于“消除”过程的叙述错误的是

A. 部分光能转变为化学能
B. 消除总反应为:4NOx+(5-2x)O2+2H2O![]() 4HNO3
4HNO3
C. 使用纳米TiO2,产生的光生电子和空穴更多,NOx消除效率更高
D. 1 mol![]() 比1 mol羟基(·OH)多9NA个电子(NA为阿伏伽德罗常数)
比1 mol羟基(·OH)多9NA个电子(NA为阿伏伽德罗常数)
查看答案和解析>>
科目: 来源: 题型:
【题目】向下列溶液中加入相应试剂后,发生反应的离子方程式正确的是
A. 向![]() 溶液中加入
溶液中加入![]() 溶液
溶液![]()
B. 向![]() 液中加入过量氨水Al3++3NH3
液中加入过量氨水Al3++3NH3![]() H2O=Al(OH)3↓+3NH4+
H2O=Al(OH)3↓+3NH4+
C. 向![]() 溶液中加入铁粉
溶液中加入铁粉![]()
D. 向![]() 溶液中加入足量新制氯水
溶液中加入足量新制氯水![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)同温同压下的两个相同容器中分别装有O2和O3气体,则两瓶气体中分子数之比是_______,原子数之比是_______,密度之比是___________。
(2)下列所给出的几组物质中:含有分子数最多的是_______;含有原子数最多的是________;标准状况下体积最大的是________。
① 1gH2; ② 2.408×1023个CH4;③ 10.8gH2O; ④ 标准状况下6.72LCO2
(3)配制100 mL 1mol/L的的稀H2SO4溶液,需要用量筒量取质量分数为98%的浓H2SO4(密度为1.84g/cm3)的体积为_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知某可逆反应mA(g)+nB(g)![]() pC(g)在密闭容器中进行,右图表示在不同反应时间t时,温度T和压强p与反应物B在混合气体中的体积分数B%的关系曲线,由曲线分析,下列判断正确的是
pC(g)在密闭容器中进行,右图表示在不同反应时间t时,温度T和压强p与反应物B在混合气体中的体积分数B%的关系曲线,由曲线分析,下列判断正确的是

A.T1<T2 p1>p2 m+n>p 放热反应
B.T1>T2 p1<p2 m+n>p 吸热反应
C.T1<T2 p1>p2 m+n<p 放热反应
D.T1>T2 p1<p2 m+n<p 吸热反应
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下,在某密闭容器中进行如下反应:
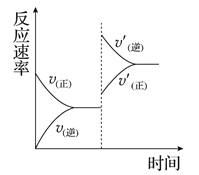
mA(g)+nB(g)![]() pC(g)+qD(g),若增大压强或升高温度,重新达到平衡,
pC(g)+qD(g),若增大压强或升高温度,重新达到平衡,
反应速率随时间的变化过程如图所示,则对该反应的叙述正确的是( )
A. 正反应是吸热反应 B. 逆反应是放热反应
C. m+n<p+q D. m+n>p+q
查看答案和解析>>
科目: 来源: 题型:
【题目】抗血栓药物氯贝丁酯( )的一种合成路线如下图,部分反应条件及部分反应物、生成物已略去。
)的一种合成路线如下图,部分反应条件及部分反应物、生成物已略去。

回答下列问题:
(1)E中官能团的名称为___________。
(2)有机物A的化学名称为___________,B的结构简式为___________,反应Ⅱ的反应类型为___________。
(3)要实现反应I的转化,加入下列物质能达到目的的是___________。
A. NaHCO. B NaOH C. Na2CO3 D. CH3COONa
(4)写出反应Ⅲ的化学方程式_________________________________。
(5)产物E有多种同分异构体,满足下列条件的所有同分异构体G有___________种。
①属于酯类且与FeCl3溶液显紫色:②能发生银镜反应;③1molG最多与2 molNaOH反应;④苯环上只有2个取代基且处于对位。
(6)结合以上合成路线信息,设计以 CH3CH2 COOH为原料(无机试剂任选),合成有机物 的合成路线_______________________________。
的合成路线_______________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】翡翠是玉石中的一种,其主要成分为硅酸铝钠NaAl(Si2O6),常含微量Cr、Ni、Mn、Mg、Fe等元素。回答下列问题:
(1)Cr3+电子排布式为______________________,基态Si原子中,电子占据的最高能层符号为______________________。
(2)翡翠中主要成分为硅酸铝钠,四种元素的第一电离能由大到小的顺序___________。
(3)锰的一种化合物的化学式为Mn(BH4)2(THF)3,THT的结构简式如图所示:

①THF中C原子的杂化轨道类型为___________,②BH4-的空间构型为___________
③NaBH4所含化学键类型有_____________
A、离子键 B、共价键 C、氢键 D、配位键
(4)MnO的熔点(1660℃)比MnS的熔点(1610℃)高,原因______________________。
(5)Ni可以形成多种氧化物,其中一种NixO晶体的晶胞结构为NaCl型,由于晶体缺陷,x为0.88,且晶体中Ni的存在形式为Ni2+、Ni3+,则晶体中N i2+和Ni3+最简整数比为___________,该晶体的晶胞参数为428pm,则晶体密度为___________g·cm-3(NA表示阿伏加德罗常数的值,列出表达式即可)
查看答案和解析>>
科目: 来源: 题型:
【题目】用无水Na2SO3固体配制 250 mL 0.1000 mol·L-1溶液的步骤如下图,请回答:

(1)在配制过程中必要的仪器有:烧杯、玻璃棒、胶头滴管、天平和____________;
(2)下列操作不会使配得的Na2SO3溶液浓度偏低的是__________。
A.容量瓶刚用蒸馏水洗净,没有烘干
B.图③没有用蒸馏水洗烧杯 2-3 次,并转移洗液
C.图⑤时仰视容量瓶的刻度线
D.图⑥后,发现液面略低于刻度线,再滴加少量水使液面凹面与刻度线相切
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com