
科目: 来源: 题型:
【题目】化学中常用图像直观地描述化学反应的进程或结果。下列图像描述正确的是
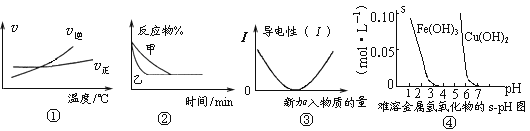
A. 根据图①可判断可逆反应“A2(g)+3B2(g)![]() 2AB3(g)”的ΔH>0
2AB3(g)”的ΔH>0
B. 图②表示压强对可逆反应2A(g)+2B(g)![]() 3C(g)+D(s)的影响,乙的压强大
3C(g)+D(s)的影响,乙的压强大
C. 图③可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化
D. 根据图④,若除去CuSO4溶液中的Fe3+可采用向溶液中加入适量CuO,至pH在4左右
查看答案和解析>>
科目: 来源: 题型:
【题目】海水中含有大量Na+、C1-及少量Ca2+、Mg2+、SO42-,用电渗析法对该海水样品进行淡化处理,如图所示。下列说法正确的是
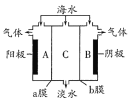
A. B极室产生的气体可使湿润的KI淀粉试纸变蓝
B. A极室产生氧气并伴有少量沉淀生成
C. 淡化工作完成后A、B、C三室中pH大小为pHA<pHB<pHC
D. b膜是阳离子交换膜
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期金属元素甲~戊在元素周期表中的相对位置如右表所示,下面判断正确的是
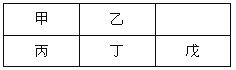
A. 原子半径:丙<丁<戊B. 金属性:甲>丙
C. 氢氧化物碱性:丙>丁>戊D. 最外层电子数:甲>乙
查看答案和解析>>
科目: 来源: 题型:
【题目】标准状况下,向100 mL H2S饱和溶液中通入SO2气体,所得溶液pH变化如图中曲线所示。

下列分析正确的是
A. 原H2S溶液的物质的量浓度为0.05 mol/L
B. 氢硫酸的酸性比亚硫酸的酸性强
C. b点水的电离程度比c点水的电离程度大
D. a点对应溶液的导电性比d点强
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)已知反应2HI(g)=H2(g) + I2(g)的△H=+11kJ·mol-1,1molH2(g)、1molI2(g)分子中化学键断裂时分别需要吸收436KJ、151KJ的能量,则1mol HI(g)分子中化学键断裂时需吸收的能量为______________kJ。
(2)某温度下,浓度都是l mol/L的两种单质气体X2和Y2,在密闭容器中反应生成气体Z。达到平衡时,X2、Y2、Z的浓度分别为0.4mol/L、0.8mol/L、0.4mol/L则该反应的化学方程式是____________________________。
(3)对反应N2O4(g)![]() 2NO2(g) △H > 0 ,在温度分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如右图所示,下列说法正确的是______。
2NO2(g) △H > 0 ,在温度分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如右图所示,下列说法正确的是______。

a.A、C两点的反应速率:A>C
b.A、C两点的化学平衡常数:A>C
c.A、C两点N2O4的转化率:A<C
d.由状态B到状态A,可以用加热的方法
查看答案和解析>>
科目: 来源: 题型:
【题目】830K时,在密闭容器中发生下列可逆反应CO(g)+H2O(g)![]() CO2(g)+H2(g) △H<0。试回答下列问题:
CO2(g)+H2(g) △H<0。试回答下列问题:
(1)若起始时c(CO)=2mol·L—1,c(H2O)=3mol·L—1,达到平衡时CO的转化率为60%,则平衡常数K=_____________,此时水蒸气的转化率为______________。
(2)在相同温度下,若起始时c(CO)=1mol·L—1,c(H2O)=2mol·L—1,反应进行一段时间后,测得H2的浓度为0.5mol·L—1,则此时该反应是否达到平衡状态_____(填“是”或“否”),此时v(正)__v(逆)(填“>”“<”或“=”)。
(3)若降低温度,该反应的K值将___________,化学反应速率将______。
查看答案和解析>>
科目: 来源: 题型:
【题目】天然铊有两种稳定同位素![]() Tl和
Tl和![]() Tl。下列有关铊的同位素说法中,不正确的是( )
Tl。下列有关铊的同位素说法中,不正确的是( )
A. ![]() Tl和
Tl和![]() Tl质子数相同B.
Tl质子数相同B. ![]() Tl和
Tl和![]() Tl互为同素异形体
Tl互为同素异形体
C. ![]() Tl和
Tl和![]() Tl中子数之差为2D.
Tl中子数之差为2D. ![]() Tl原子核内中子数与核外电子数之差为43
Tl原子核内中子数与核外电子数之差为43
查看答案和解析>>
科目: 来源: 题型:
【题目】已知下列热化学方程式:
①CH3COOH(l)+2O2(g)===2CO2(g)+2H2O(l) ΔH1=-870.3 kJ/mol
②C(s)+O2(g)===CO2(g) ΔH2=-393.5 kJ/mol
③H2(g)+![]() O2(g)===H2O(l) ΔH3=-285.8 kJ/mol
O2(g)===H2O(l) ΔH3=-285.8 kJ/mol
则反应④2C(s)+2H2(g)+O2(g)===CH3COOH(l)的焓变为
A.488.3 kJ/molB.-224.15 kJ/mol
C.-488.3 kJ/molD.244.15 kJ/mol
查看答案和解析>>
科目: 来源: 题型:
【题目】在t ℃时,AgBr在水中的沉淀溶解平衡曲线如图所示。已知t ℃时AgCl的Ksp=4×10-10,下列说法正确的是( )
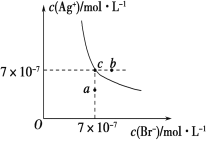
A. 加入NaBr固体,AgBr的溶解度减小,Ksp也减小
B. 在AgBr饱和溶液中加入固体NaBr,可使溶液中c点变到b点
C. 图中a点对应的是有AgBr沉淀生成
D. 在t ℃时,AgCl(s)+Br-(aq) AgBr(s)+Cl-(aq)的平衡常数K≈816
查看答案和解析>>
科目: 来源: 题型:
【题目】将气体A、B置于固定容积为2 L的密闭容器中,发生反应:3A(g)+B(g)2C(g)+2D(g),反应进行到10 s末,达到平衡,测得A的物质的量为1.8 mol,B的物质的量为0.6 mol,C的物质的量为0.8 mol。
(1)用C表示10 s内反应的平均反应速率为______。
(2)反应前A的物质的量浓度是_______。
(3)10 s末,生成物D的浓度为______。
(4)A与B的平衡转化率之比为_______。
(5)平衡后,若改变下列条件,生成D的速率如何变化(填“增大”、“减小”或“不变”):
①降低温度____;
②增大压强____
③增大A的浓度_____;
④恒容下充入Ne______。
(6)下列叙述能说明该反应已达到化学平衡状态的是(填标号)_____;
A.v(B)=2v(C)
B.容器内压强不再发生变化
C.A的体积分数不再发生变化
D.器内气体密度不再发生变化
E.相同时间内消耗n mol的B的同时生成2n mol的D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com