
科目: 来源: 题型:
【题目】I. 氢气是一种常用的化工原料,应用十分广泛。
(1)以H2合成尿素CO(NH2)2的有关热化学方程式有:
①N2(g)+3H2(g)===2NH3(g) ΔH1=-92.4 kJ·mol-1
②NH3(g)+1/2CO2(g)===1/2NH2CO2NH4(s) ΔH2=-79.7 kJ·mol-1
③NH2CO2NH4(s)===CO(NH2)2(s)+H2O(l) ΔH3=+72.5 kJ·mol-1
则N2(g)、H2(g)与CO2(g)反应生成CO(NH2)2(s)和H2O(l)的热化学方程式为_______________________________________________________。
II.某同学设计了一组电化学装置如下图所示,其中乙装置中X为阳离子交换膜,甲醇(CH3OH)具有可燃性。
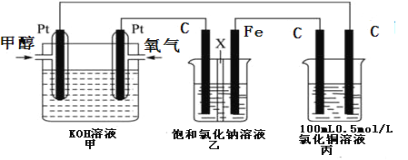
根据要求回答相关问题:
(2)写出装置甲中负极的电极反应式:_______________________________________。
(3)装置乙中石墨电极(C)的电极反应式为:_________________________________。
(4)当装置甲中消耗0.05molO2时,丙装置中阳极产生气体的体积___________L(标况下);装置乙中溶液的pH为___________(溶液体积为200mL不变),要使乙烧杯中的溶液恢复到原来的状态,需要加入的物质是___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某太阳能电池的工作原理如图所示。下列说法正确的是

A. 光照时,b极的电极反应式为VO2+-e-+H2O=VO2++2H+
B. 光照时,毎转移2mol电子,有2mol H+由a极区经质子交换膜向b极区迁移
C. 夜间,a极的电极反应式为V3++e-=V2+
D. 硅太阳能电池供电原理与该电池相同
查看答案和解析>>
科目: 来源: 题型:
【题目】如图为电解饱和食盐水装置,下列有关说法不正确的是

A. 左侧电极上发生氧化反应
B. 右侧生成的气体能使湿润的淀粉碘化钾试纸变蓝
C. 电解一段时间后,B口排出NaOH溶液
D. 电解饱和食盐水的离子方程式: 2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验误差分析错误的是( )
A.用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小
B.排水量气,左右液面相平后,未冷却到室温立即读数,所得气体的体积偏大
C.称取2.3gNaCl固体,砝码放在托盘天平的左边,所称量固体药品质量偏小
D.用量筒量取5.0mL浓硫酸,仰视读数,所得到浓硫酸的体积偏大
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA表示阿伏伽德罗常数的值,下列说法不正确的是( )
A.常温常压下,14g有N2与CO组成的混合气体含有的原子数目为NA个
B.0.5molO3与11.2LO2所含的分子数一定相等
C.10gCaCO3和KHCO3的固体混合物含有0.1NA个阳离子
D.用16.25gFeCl3制备Fe(OH)3胶体,Fe(OH)3胶体粒子数小于0.1NA个
查看答案和解析>>
科目: 来源: 题型:
【题目】为探究外界条件对反应:mA(g)+nB(s)![]() cZ(g) △H的影响,以A和B物质的量之比为m:n开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数。实验结果如图所示,下列判断正确的是
cZ(g) △H的影响,以A和B物质的量之比为m:n开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数。实验结果如图所示,下列判断正确的是

A. △H>0
B. m<c
C. 升温,正、逆反应速率都增大,平衡常数减小
D. 在恒温恒容下,向已达到平衡的体系中加入少量Z,达到平衡后Z的含量减小
查看答案和解析>>
科目: 来源: 题型:
【题目】某新型电池,以NaBH4(B的化合价为+3价)和H2O2作原料,该电池可用作深水勘探等无空气环境电源,其工作原理如图所示。下列说法正确的是
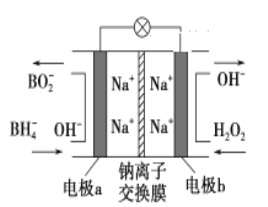
A. 电池工作时Na+从b极区移向a极区
B. a极上的电极反应式为:BH4-+8OH--8e-===BO2-+6H2O
C. 每消耗3 mol H2O2,转移3 mol e-
D. b极上的电极反应式为:H2O2+2e-+2H+===2H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.实验室里需要氯化钠溶液,但实验室只有混有硫酸钠、碳酸氢铵的氯化钠固体。某学生设计了如下方案进行提纯:

已知:碳酸氢铵受热容易分解,生成二氧化碳、氨气和水。
(1)操作②能否改为加硝酸钡溶液,___(填“能”或“否”),理由___。
(2)进行操作②后,如何判断SO42-已除尽,方法是___。
Ⅱ.硫酸亚铁铵(NH4)2SO4·FeSO4·6H2O为浅绿色晶体,实验室中常以废铁屑为原料来制备,其步骤如下:
步骤1:将废铁屑放入碳酸钠溶液中煮沸除油污,分离出液体,用水洗净铁屑。
步骤2:向处理过的铁屑中加入过量的3mol/L H2SO4溶液,在60℃左右使其反应到不再产生气体,趁热过滤,得FeSO4溶液。
步骤3:向所得FeSO4溶液中加入饱和(NH4)2SO4溶液,经过“一系列操作”后得到硫酸亚铁铵晶体。
请回答下列问题:
(1)在步骤1中,分离操作,所用到的玻璃仪器有___。(填仪器编号)
①漏斗 ②分液漏斗 ③烧杯 ④广口瓶 ⑤铁架台 ⑥玻璃棒
(2)在步骤3中,“一系列操作”依次为__、___和过滤、洗涤、干燥。
查看答案和解析>>
科目: 来源: 题型:
【题目】下面是实验室制取少量固体氧化铜的实验,根据实验步骤,回答有关问题。

(1)调整天平零点时,若指针偏向右边,应将左边的螺丝____________(填“向左”或“向右”)旋动。
(2)滴加NaOH溶液,生成沉淀的离子方程式为_______________________________。
(3)加热蒸发过程中要用到玻璃棒,其作用是_________________________________。
(4)洗涤该沉淀的方法是______________________________________________________,为了检验此沉淀是否洗涤干净,应取最后一次的洗涤液少许,加入__________溶液检验。
(5)若向CuSO4溶液中滴加了100mLNaOH溶液,则NaOH溶液的物质的量浓度至少为_________。
(6)理论上最多可以制得CuO的质量为 _______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com