
科目: 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增加,由这些元素组成的常见物质的转化关系如下图,其中a、b、d、g为化合物,a为淡黄色固体,c是Z的单质,在铝热反应中常做引发剂;e、f为常见气体单质。下列有关说法正确的是( )

A. 简单离子的半径:Y>Z>X
B. 简单氢化物的沸点:Y>X
C. 最高价氧化物对应水化物的碱性:Z> Y
D. Y、Z的氧化物所含化学键类型相同
查看答案和解析>>
科目: 来源: 题型:
【题目】下图表示有关物质的相互转化关系,其中A是由G和某淡黄色固体组成的混合物,I是常见的无色液体,反应①在化工生产中有着重要应用(部分产物和条件已略去)。

(1)写出以下物质的化学式:B_______、F_______。
(2)反应②的离子方程式为_______。
(3)我国首创的由G、空气和海水组成的电池,在航海领域有着极其重要的作用,其工作时正极反应式为_______,该电池最大的优点是只需补充_______〔填“正极”或“负极”〕材料就可接着使用。
(4)向M的水溶液中加入少量A中的淡黄色固体,反应的化学方程式为_______。
(5)25℃时,pH均为5的盐酸和M的水溶液中,由H2O电离出的H+物质的量浓度之比为_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】用中和滴定法测定某烧碱样品的纯度。有以下步骤:
(1)配制待测液:用5.0g含有少量杂质(杂质不与盐酸反应)的固体烧碱样品配制1000mL溶液。除烧杯和玻璃棒外,还需要的玻璃仪器有______;
(2)选择酚酞为指示剂进行滴定:
①盛装0.1000mol/L的盐酸标准液应该使用_____式滴定管;
②滴定时双眼应_______________;
③滴定终点的实验现象:___________。
(3)有关数据记录如下:
测定序号 | 待测溶液的体积(mL) | 所耗盐酸标准液的体积(mL) | |
滴定前读数 | 滴定后读数 | ||
① | 20.00 | 0.50 | 20.78 |
② | 20.00 | 1.20 | 21.32 |
计算纯度:烧碱样品的纯度是________;(取两次实验所耗盐酸的平均值进行计算)
(4)误差讨论:(选填“偏高”、“偏低”或“无影响”)
①用蒸馏水冲洗锥形瓶,会使测定结果__________;
②在滴定过程中不慎将数滴酸液滴在锥形瓶外,会使测定结果_______;
③读数时,滴定前仰视,滴定后俯视,会使测定结果__________;
④装标准液之前,没有用标准液润洗滴定管,会使测定结果__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是元素周期表的一部分,A、B、C、D、E、X是周期表给出元素组成的常见单质或化合物。
① | |||||||||||||||||
④ | ⑤ | ⑥ | |||||||||||||||
② | ③ | ⑦ | |||||||||||||||
Fe | As | ||||||||||||||||
I、元素周期表是人们研究物质性质的重要工具。Y由②⑥⑦三种元素组成,它的水溶液是生活中常见的消毒剂。As可与Y的水溶液反应,产物有As的最高价含氧酸,该反应的化学方程式为_______,当消耗1mol还原剂时,转移的电子个数为_______。
Ⅱ、A、B、C、D、E、X存在如下图转化关系〔部分生成物和反应条件略去〕。

(1)假设E为氧化物,那么A与水反应的化学方程式为_______。
①当X是碱性盐溶液,C分子中有22个电子时,那么C的电子式为_______。
②表示
③当X为金属单质时,那么X与B的稀溶液反应生成C的离子反应方程式为_______。
(2)假设E为单质气体,D为白色沉淀,B含有的化学键类型为_______,C与X反应的离子方程式为_______。
(3)①和⑤形成的化合物是一种可燃性液体,其燃烧产物之一是大气中的要紧成分,1.6克该物质在氧气中完全燃烧放出热量31.2kJ,写出热化学方程式_______。
(4)废印刷电路板上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现改用①和⑥组成的化合物和稀硫酸浸泡废印刷电路板既达到上述目的,又保护了环境,试写出反应的离子方程式_______。
(5)元素②的单质在一定条件下,能与①的单质化合生成一种化合物,熔点为800℃。该化合物能与水反应放氢气,假设将1mol该化合物和1mol③形成的单质混合加入足量的水,充分反应后生成气体的体积是(标准状况下)_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室有NH4HCO3和NaHSO3的干燥粉状混合物,某化学兴趣小组测定其中NH4HCO3的含量。小组的同学设计用在混合物中加酸的实验方法来测定其中NH4HCO3的质量分数。(SO2与酸性KMnO4的反应原理:SO2+MnO4-+H+—SO42-+Mn2++H2O)回答以下问题:
(1)化学小组要紧选用了以下药品和仪器进行实验(图中每种仪器装置只选用了一次,铁架台等固定仪器未画出)
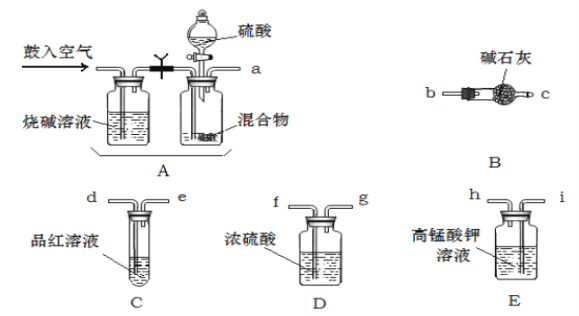
请按气流由左向右的方向,仪器连接顺序是〔填仪器的接口字母a、b...)a→_______f→g→_______。
(2)实验开始,混合物加酸前,A装置需要鼓入空气,作用是;加酸后A装置再次鼓入空气的作用是_______。
(3)E装置的作用是:_______。
(4)实验中,假设C试管中溶液褪色,那么测定结果可能会偏_______,为了确保实验中C试管中溶液不褪色,假设取样品的质量为mg,实验前E中所装amol·L-1的KMnO4溶液体积〔V〕应多于______mL;
(5)假设混合物样品质量为9.875g,充分作用后碱石灰增重4.4g,那么混合物中NH4HCO3的质量分数为_______。
(6)从定量测定的准确性的角度考虑,该套装置还应作进一步的改进,改进的措施是_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】I.用相应的方程式解释:
(1)NaHSO3溶液显酸性:___________________
(2)NaHCO3溶液显碱性:____________________
(3)NH4Cl溶液显酸性:______________________
(4)明矾[KAl(SO4)2]净水:___________________
(5)FeCl3溶液蒸干得到Fe2O3固体:____________(第一步反应)
II.向2份0.1mol/LCH3COONa溶液中分别加入少量NH4NO3、Na2CO3固体(忽略溶液体积变化),则CH3COO-浓度的变化依次为_______、______(填“减小”、“增大”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】I.碳酸钠是一种重要的化工原料,主要采用氨碱法生产。回答下列问题:
(1)已知:①2NaOH(s)+CO2(g)=Na2CO3(s)+H2O(g) ΔH1=127.4kJ/mol
②NaOH(s)+CO2(g) = NaHCO3(s) ΔH2=131.5kJ/mol
反应2NaHCO3(s)=Na2CO3(s) +H2O(g) +CO2(g)的ΔH=____kJ/mol,不同温度下NaHCO3分解反应的平衡常数K313K____K298K(填“大于"“小于”或“等于”),该反应的平衡常数表达式K=______。
(2)向含有BaSO4固体的溶液中滴加Na2CO3溶液,当有BaCO3沉淀生成时溶液中![]() =____。(保留一位小数,已知Ksp(BaCO3)=2.6×109 ,Ksp(BaSO4)=1.1×1010)
=____。(保留一位小数,已知Ksp(BaCO3)=2.6×109 ,Ksp(BaSO4)=1.1×1010)
II.Mg﹣H2O2电池可用于驱动无人驾驶的潜航器,该电池以海水为电解质溶液,其工作原理如图所示,电池总反应是:Mg+H2O2+2H+═ Mg2++2H2O

(1)负极材料为_____,发生___反应(填“氧化”或“还原”)
(2)两极电极反应式为:
负极:_________________;正极:_________________;
(3)有4.8gMg反应时时,外电路中转移电子数为______。
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,将3molSO2和1molO2充入一定容密闭容器中,在催化剂存在下进行下列反应:2SO2(g)+O2(g)![]() 2SO3(g);△H=-197kJ/mol,当达到平衡状态时,下列说法中正确的是( )
2SO3(g);△H=-197kJ/mol,当达到平衡状态时,下列说法中正确的是( )
A.达到反应限度时,生成SO3为2mol
B.达到反应限度时,反应放出的热量一定小于197kJ
C.达到反应限度时SO2、O2、SO3的分子数之比一定为2∶1∶2
D.达到反应限度时SO2的消耗速率必定等于SO3的消耗速率
查看答案和解析>>
科目: 来源: 题型:
【题目】氢溴酸在医药和石化工业上有广泛用途。下图是模拟工业制备氢溴酸粗品并精制流程:

依照上述流程回答以下问题:
(1)混合①中发生反应的化学方程式为_______。
(2)操作Ⅱ和操作Ⅲ的名称分别是_______、_______。操作Ⅲ一般适用于分离____________混合物。〔选填编号〕
a、固体和液体b、固体和固体c、互不相溶的液体d、互溶的液体
(3)混合②中加入Na2SO3的目的是_______。
(4)纯净的氢溴酸应为无色液体,但实际工业生产中制得的氢溴酸〔工业氢溴酸〕带有淡淡的黄色。因此甲乙两同学设计了简单实验加以探究:甲同学假设工业氢溴酸呈淡黄色是因为含Fe3+,那么用于证明该假设所用的试剂的名称为_______。乙同学假设工业氢溴酸呈淡黄色是因为________,其用于证明该假设所用的试剂的化学式_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】一定量CO2通入某浓度的NaOH溶液得溶液A,向A溶液中逐滴滴入稀盐酸,加入n(HCl)与生成n(CO2)的关系如图。以下有关表达正确的选项是

A.通入的CO2气体在标准状况下等于22.4L
B.溶液中n(NaOH)=2n(Na2CO3)
C.A溶液中既含Na2CO3,又含NaHCO3
D.A溶液中一定只有Na2CO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com