
科目: 来源: 题型:
【题目】(1)中国的高铁技术居于国际领先地位。
①高铁座椅内填充有聚氨酯软质泡沫。聚氨酯属于____(填字母)。
a.金属材料 b.无机非金属材料 c.有机高分子材料
②高铁信息传输系统中使用了光导纤维。光导纤维的主要成分是____(填字母)。
a.铜 b.石墨 c.二氧化硅
③高铁轨道建设需用大量水泥。生产水泥的主要原料为黏土和____(填字母)。
a.石灰石 b.粗盐 c.纯碱
(2)营养均衡有利于身体健康。
①人体内提供能量的主要营养物质为____、糖类和蛋白质。淀粉在人体内水解的最终产物是____。
②维生素是人体需要的营养物质。如图为某品牌维生素C泡腾片说明书的部分内容。该泡腾片中添加的着色剂是____,甜味剂是___。泡腾片溶于水时产生“沸腾”效果,是由于添加的酒石酸和___反应释放出了气体。

(3)煤炭在我国能源结构中占有重要地位,合理使用有利于社会可持续发展。
①控制燃煤产生的SO2排放,能够减少____型酸雨的形成。燃煤排放的烟气中还含有其他污染物,请列举一种:_____。
②燃煤产生的CO2用NH3处理可生产多种化工产品。用氨水吸收CO2可制得碳铵(NH4HCO3),写出该反应的化学方程式_____。用液氨与CO2反应可制备尿素[CO(NH2)2]。尿素和碳铵这两种氮肥中,氮元素的质量分数较高的是_____。
③煤的气化和液化是实现能源清洁化的重要途径。水煤气中CO和H2在加热、加压和催化剂存在条件下可以合成液体燃料(CH3OH),该反应的化学方程式为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)2015年11月首架C919打飞机总装下线,标志着我国跻身飞机研制先进国家行列。
①机身蒙皮使用的是第三代铝锂合金材料。下列不属于铝锂合金性质的是___(填字母)。
a.密度大 b.硬度大 c.抗腐蚀
②飞机轮胎属于橡胶制品。下列材料可用来合成橡胶的是____(填字母)。
a.石英砂 b.石灰石 c.异戊二烯
③机体先进复合材料的使用率达12%。下列属于复合材料的是___(填字母)。
a.钛合金 b.玻璃钢 c.普通陶瓷
(2)秋葵是一种大众喜爱的食材,含有蛋白质、维生素A、维生素C、纤维素、阿拉伯果糖和丰富的铁、锌、钙等元素,其中:

①属于人体所需微量元素的是____。
②属于水溶性维生素的是____,属于糖类的有阿拉伯果糖、___。
③蛋白质在人体内最终的水解产物是_____。
(3)化学能帮助我们更好地认识生活、改善生活。
①家用铁锅未洗净晾干,放置一段时间后出现红褐色锈斑,其主要的原因是铁发生了____腐蚀。
②乘车禁止携带物品的部分标识如图所示。在浓硝酸、食盐、汽油、石膏四种物品中,不能携带上车的是_____。

③过氧乙酸(![]() )易分解为乙酸和氧气,其稀溶常用于餐具、器械的消毒。写出过氧乙酸分解的化学方程式______。某胃药的主要成分是AlbMgc(OH)mCO3,常用于治疗胃酸过多,写出其中与胃酸反应的化学方程式_______。
)易分解为乙酸和氧气,其稀溶常用于餐具、器械的消毒。写出过氧乙酸分解的化学方程式______。某胃药的主要成分是AlbMgc(OH)mCO3,常用于治疗胃酸过多,写出其中与胃酸反应的化学方程式_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】LED产品具有耗电量低、寿命长的特点。下图是氢氧燃料电池驱动LED屏发光的装置,下列有关叙述错误的是( )
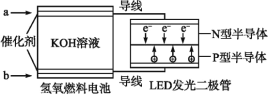
A.a处通入的气体是氢气,电极反应式为H2+2OH-2e=2H2O
B.装置中电子的流向为a极→N型半导体→P型半导体→b极
C.装置中的能量转化至少涉及三种形式的能量
D.图中![]() 表示来自氢氧燃料电池中的K+的移动方向
表示来自氢氧燃料电池中的K+的移动方向
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)积极保护生态环境可实现人与自然的和谐共处。
①下列做法会加剧温室效应的是__________(填字母)。
a.植树造林 b.燃煤供暖 c.风力发电
②下列防治“白色污染”的正确方法是_____________(填字母)。
a.使用可降解塑料 b.露天焚烧废旧塑料 c.直接填埋废旧塑料
③为减轻大气污染,多个城市已禁止燃放烟花爆竹。“禁止燃放烟花爆竹”的标识是_____(填字母)。

(2)合理使用化学知识可提高人们的生活质量。
某品牌牙膏的成分有甘油、山梨酸钾、氟化钠等。
①在上述牙膏成分中,属于防腐剂的是_______________。
②甘油的结构简式为____________;油脂水解可生成甘油和_____________。
③氟化钠(NaF)可与牙齿中的羟基磷酸钙[Ca5(PO4)3OH]反应,生成更难溶的氟磷酸钙[Ca5(PO4)3F],从而达到防治龋齿的目的。写出该反应的化学方程式:____________________。
(3)创新发展材料技术科推动人类社会的进步。
①石墨烯(见下图)可用作太阳能电池的电极,这里主要利用了石墨烯的______________性。

②基础工程建设中常用到水泥、玻璃、钢材等。生成水泥和玻璃都用到的原料是__________;在钢材中添加铬、镍等元素的目的是___________。
③新型战斗机常用纳米SiC粉体作为吸波材料。高温下焦炭和石英反应可制得SiC,石英的化学式为________________;高温分解Si(CH3)2Cl2也可制得SiC,同时还生成CH4和一种常见酸性气体,写出该反应的化学方程式:____________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】将1 mol甲烷与一定量的氯气混合于一量筒中,倒立于盛有饱和食盐水的水槽(如图所示),对于此反应,有关叙述不正确的是( )
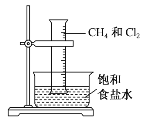
A.该反应的生成物只有四种
B.该反应的条件是光照
C.该反应属于取代反应
D.该反应现象有量筒内气体颜色变浅,器壁上有油状液滴
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学设计的微型实验装置验证SO2的性质,通过分析实验,下列结论表达正确的是( )

A.a棉球褪色,验证SO2具有氧化性
B.c棉球蓝色褪去,验证SO2漂白性
C.b棉球褪色,验证SO2具有酸性氧化物的通性
D.可以使用浓硫酸吸收尾气
查看答案和解析>>
科目: 来源: 题型:
【题目】2019年3月8日,联合国妇女署在推特上发布了一张中国女科学家屠呦呦的照片。致敬她从传统中医药中找到了治疗疟疾的药物----青蒿素。
已知:青蒿素是烃的含氧衍生物,为无色针状晶体。乙醚沸点为35℃。
(1)我国提取中草药有效成分的常用溶剂有:水;或亲水性溶剂(如乙醇,与水互溶);或亲脂性溶剂(如乙醚,与水不互溶)。诺贝尔奖获得者屠呦呦及其团队在提取青蒿素治疗疟疾过程中,记录如下:“青蒿素的水煎剂无效;乙醇提取物的效用为30%~40%;乙醚提取物的效用为95%”。下列推测不合理的是_____;
A | 青蒿素在水中的溶解度很大 | B | 青蒿素含有亲脂的官能团 |
C | 在低温下提取青蒿素,效果会更好 | D | 乙二醇提取青蒿素的能力强于乙醚 |
(2)用下列实验装置测定青蒿素实验式的方法如下:
将28.2g青蒿素样品放在硬质玻璃管C中,缓缓通入空气数分钟后,再充分燃烧,精确测定装置E和F实验前后的质量,根据所测数据计算。
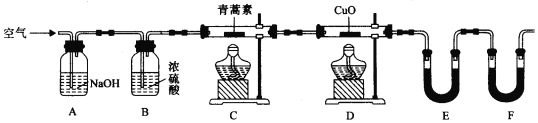
①装置D的作用是______,装置E中吸收的物质是______,装置F中盛放的物质是______。
②实验装置可能会产生误差,造成测定含氧量偏低,改进方法是______。
③合理改进后的装置进行实验,称得:
装置 | 实验前/g | 实验后/g |
E | 22.6 | 42.4 |
F | 80.2 | 146.2 |
则测得青蒿素的实验式是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】某天然黄铜矿主要成分为![]() (含
(含![]() ),为测定该黄铜矿的纯度,某同学设计了如下实验:
),为测定该黄铜矿的纯度,某同学设计了如下实验:
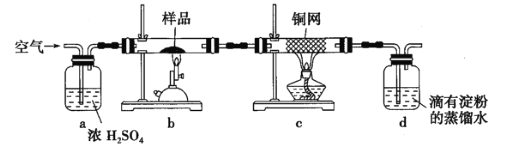
称取硏细的黄铜矿样品![]() 煅烧,生成
煅烧,生成![]() 、
、![]() 、
、![]() 和
和![]() 气体,实验后取
气体,实验后取![]() 中溶液的1/10置于锥形瓶中,用
中溶液的1/10置于锥形瓶中,用![]() 标准碘溶液进行滴定,初读数为
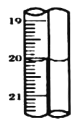
标准碘溶液进行滴定,初读数为![]() ,末读数如图所示,完成下列填空:
,末读数如图所示,完成下列填空:
(1)实验中称量样品所需定量仪器为____________。
(2)装置![]() 的作用是____________。
的作用是____________。
(3)上述反应结束后,仍需通一段时间的空气,其目的是____________。
(4)滴定时,标准碘溶液所耗体积为______![]() 。用化学方程式表示滴定的原理:____________。
。用化学方程式表示滴定的原理:____________。
(5)计算该黄铜矿的纯度____________。
(6)工业上利用黄铜矿冶炼铜产生的炉渣(含![]() ,
,![]() ,
,![]() ,
,![]() )可制备
)可制备![]() 。选用提供的试剂:稀盐酸、稀硫酸、
。选用提供的试剂:稀盐酸、稀硫酸、![]() 溶液、
溶液、![]() 溶液、
溶液、![]() 溶液,设计实验验证炉渣中含有
溶液,设计实验验证炉渣中含有![]() 。所选试剂为____________,证明炉渣中含有
。所选试剂为____________,证明炉渣中含有![]() 的实验方案为____________。
的实验方案为____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】阿伏加德罗常数的值为NA,下列叙述中错误的是( )
①标准状况下,2.24 L水中含有0.1 NA个水分子
②常温常压下,32g SO2 含有的分子数为0.5NA
③2 mol NaOH的摩尔质量为80g/mol
④H2的气体摩尔体积约为22.4L/mol
⑤2mol/L的CaCl2溶液中Cl-的数目为4NA
⑥常温常压下,1mol氦气含有的原子数为NA
A.2个B.3个C.4个D.5个
查看答案和解析>>
科目: 来源: 题型:
【题目】生产自来水最重要的两步工序是净化和消毒,净化一般使用![]() ,消毒一般使用
,消毒一般使用![]() 。
。
(1)![]() 溶液呈酸性的原因是(用离子方程式表示)____________;
溶液呈酸性的原因是(用离子方程式表示)____________;![]() 具有净水作用,但会腐蚀钢铁设备,除
具有净水作用,但会腐蚀钢铁设备,除![]() 作用外,另一主要原因是(用离子方程式表示):____________。
作用外,另一主要原因是(用离子方程式表示):____________。
(2)氯气的水溶液称为氯水,氯水中存在多个平衡,写出其中两个含氯元素的平衡方程式:____________、____________。氯水中存在![]() 分子、
分子、![]() 分子和
分子和![]() 分子,不存在
分子,不存在![]() 分子的原因是_______,除水分子外,新制氯水中含量最多的微粒是__________。
分子的原因是_______,除水分子外,新制氯水中含量最多的微粒是__________。
(3)次氯酸有漂白杀菌作用,其作用原理是![]() ,该变化是____________反应(选填“氧化”、“还原”、“氧化还原”);在
,该变化是____________反应(选填“氧化”、“还原”、“氧化还原”);在![]() 溶液中通入少量
溶液中通入少量![]() 气体,只发生如下反应:
气体,只发生如下反应:![]() ,由此判断
,由此判断![]() 、
、![]() 和
和![]() 的酸性由强到弱的顺序是____________。
的酸性由强到弱的顺序是____________。
(4)![]() 能用于自来水消毒,还能除去水中的
能用于自来水消毒,还能除去水中的![]() 杂质,产物为
杂质,产物为![]() 和盐酸。写出该反应的离子方程式__________________。
和盐酸。写出该反应的离子方程式__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com