
科目: 来源: 题型:
【题目】分枝酸可用于生化研究。其结构简式如图。下列关于分枝酸的叙述正确的是

A. 分子中含有2种官能团
B. 可与乙醇、乙酸反应,且反应类型相同
C. 1mol分枝酸最多可与3molNaOH发生中和反应
D. 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
查看答案和解析>>
科目: 来源: 题型:
【题目】下表列出了10种元素在元素周期表中的位置:
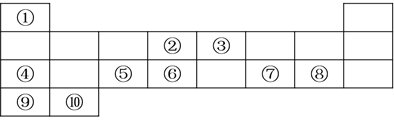
请用相应的化学用语回答下列问题:
(1)元素②在元素周期表中处于第________________周期,第________________族;
(2)上述10种元素中,金属性最强的元素的符号为________________,最高价氧化物对应水化物中,酸性最强的物质的分子式为________________;
(3)②、③、⑥三种元素按原子半径由大到小的顺序排列为________________(用元素符号表示);
(4)④在空气中燃烧的化学方程式为________________;
(5)元素④、⑦的最高价氧化物对应水化物发生反应的离子方程式为________________;
(6)⑧与⑨形成的化合物的电子式为________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】25 ℃时,在“H2A—HA-—A2-”的水溶液体系中,H2A、HA-和A2- 三者中各自所占的物质的量分数(α)随溶液pH变化的关系如图所示。下列说法正确的是

A. 在含H2A、HA-和A2- 的溶液中,加入少量NaOH固体,α(HA-)一定增大
B. 将等物质的量的NaHA和Na2A混合物溶于水,所得溶液中α(HA-)=α(A2-)
C. NaHA溶液中,HA-的水解能力大于HA-的电离能力
D. 在含H2A、HA-和A2-的溶液中,若c(H2A)+2c(A2-)+c(OH-)=c(H+),则α(H2A)与α(HA-)不一定相等
查看答案和解析>>
科目: 来源: 题型:
【题目】对利用甲烷消除NO2污染进行研究,CH4+2NO2 ![]() N2+CO2+2H2O。在1L密闭容器中,控制不同温度,分别加入0.50molCH4和1.2molNO2,测得n(CH4)随时间变化的有关实验数据见下表。
N2+CO2+2H2O。在1L密闭容器中,控制不同温度,分别加入0.50molCH4和1.2molNO2,测得n(CH4)随时间变化的有关实验数据见下表。
组别 | 温度 | 时间/min n/mol | 0 | 10 | 20 | 40 | 50 |
① | T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
② | T2 | n(CH4) | 0.50 | 0.30 | 0.18 | … | 0.15 |
下列说法正确的是
A. 组别①中,0~20min内,NO2的降解速率为0.0125 mol·L-1·min-1
B. 由实验数据可知实验控制的温度T12
C. 40min时,表格中T2应填的数据为0.18
D. 0~10min内,CH4的降解速率①>②
查看答案和解析>>
科目: 来源: 题型:
【题目】下列对实验的装置、药品、操作和现象的预测中都正确的是( ):
A. 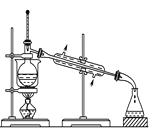 可从含碘的苯溶液里分离出碘单质并回收苯溶剂
可从含碘的苯溶液里分离出碘单质并回收苯溶剂
B. 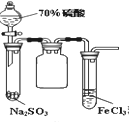 当70%H2SO4跟Na2SO3粉末混合后,可观察到右端试管内出现淡黄色浑浊
当70%H2SO4跟Na2SO3粉末混合后,可观察到右端试管内出现淡黄色浑浊
C. 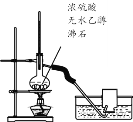 当将烧瓶内液体迅速升温至170℃时,可用排水法收集到乙烯气体
当将烧瓶内液体迅速升温至170℃时,可用排水法收集到乙烯气体
D. 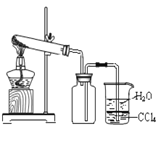 将盛氯化铵和消石灰固体的试管加热,可制取并收集到干燥的NH3
将盛氯化铵和消石灰固体的试管加热,可制取并收集到干燥的NH3
查看答案和解析>>
科目: 来源: 题型:
【题目】非金属单质A经过如图所示的过程转化为含氧酸D。已知D为强酸,请回答下列问题:
![]()
(1)A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体。
①D的化学式是___。
②在工业生产中气体B大量排放后,被雨水吸收形成了污染环境的___。
(2)A在常温下为气体,C是红棕色的气体。
①A的化学式是___;C的化学式是___。
②在常温下D的浓溶液可与铜反应并生成气体C,请写出该反应的化学方程式:___,该反应__(填“属于”或“不属于”)氧化还原反应。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验“操作和现象”与“实验目的、结论”的对应关系中正确的是( )
操作和现象 | 实验目的或结论 | |
A | 将H2S气体通入CuSO4溶液中,产生黑色沉淀 | H2S的酸性比H2SO4的强 |
B | 固体溶解于水后的溶液中加入澄清的石灰水 | 探究家庭“食用碱”的成分是 碳酸钠还是碳酸氢钠 |
C | 某溶液先加稀硝酸,再加BaCl2溶液,产生白色沉淀 | 能证明该溶液中一定含有Ag+ |
D | 向MgCl2溶液(含FeCl3)中加入足量MgCO3粉末 | 除去MgCl2溶液中少量FeCl3 |
A. AB. BC. CD. D
查看答案和解析>>
科目: 来源: 题型:
【题目】乳酸亚铁晶体{[CH3CH(OH)COO]2Fe·3H2O}(相对分子质量:288),可由乳酸与FeCO3反应制得,它易溶于水,几乎不溶于乙醇,是一种很好的补铁剂,但其水溶液易被氧化,光照可促进氧化。
I.制备碳酸亚铁:装置如图所示。
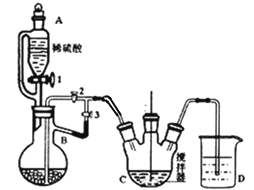
锌铁 NH4HCO3溶液
(1)仪器B的名称是________。
(2)实验操作如下:关闭活塞2,打开活塞1、3,加入适量稀硫酸反应一段时间,其目的是____________________________,然后关闭活塞1,接下来的操作是____________________,此后,C装置溶液中有沉淀生成,并有大量气泡冒出,则C中发生反应的离子方程式为_____________________________________。
Ⅱ.制备乳酸亚铁:
(3)向纯净的FeCO3固体加入足量乳酸溶液,在75℃下搅拌使之充分反应。该反应的加热方式为____________。为防止乳酸亚铁变质,在上述体系中还应加入适量铁粉。反应结束后,将所得溶液隔绝空气低温浓缩、_________、过滤、洗涤、干燥,得乳酸亚铁晶体。该晶体存放时应注意_________________________。
III.乳酸亚铁晶体纯度的测量:
(4)某同学查阅文献后,用(NH4)4Ce(SO4)4滴定法测定样品中Fe2+的含量并计算样品纯度(反应中Ce4+还原为Ce3+),他称取6.00g样品,配制成250.00mL溶液,取出25.00mL,用浓度为0.10mol·L-1的(NH4)4Ce(SO4)4标准溶液滴定至终点,消耗标准液20.00mL。则产品中乳酸亚铁晶体的纯度为________(以质量分数表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)有机物的结构可用“键线式”简化表示。如CH3—CH=CH-CH3可简写为![]() ,若有机物X的键线式为:
,若有机物X的键线式为: ![]() ,则该有机物的分子式为_______,其二氯代物有_______种;Y是X的同分异构体,分子中含有1个苯环,写出Y的结构简式________。Y在一定条件下发生加聚反应,写出其反应的化学方程式:______________________________________。
,则该有机物的分子式为_______,其二氯代物有_______种;Y是X的同分异构体,分子中含有1个苯环,写出Y的结构简式________。Y在一定条件下发生加聚反应,写出其反应的化学方程式:______________________________________。
(2)以乙烯为原料合成化合物C的流程如下所示:
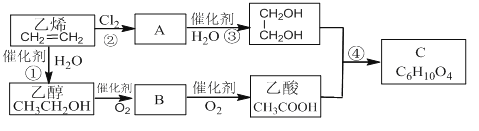
a A和B中所含官能团的名称分别为________和________。
b B物质的结构简式为________。
c ① 、④的反应类型分别为________和________。
d 反应②和④的化学方程式分别为:
②______________________________________________________。
④______________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示的装置中,A是用二氧化锰制取氯气发生装置,C、D为气体净化装置(C中装有饱和食盐水,D中装有浓硫酸),E是硬质玻璃管装有细铁丝网,F为干燥的空广口瓶,烧杯G中装有氢氧化钠溶液。
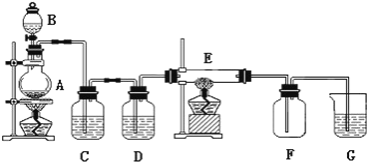
请回答下列问题:
(1)仪器B的名称是________________;
(2)实验室制氯气的化学方程式:________________;
(3)C装置的作用是________________;D装置的作用是________________;
(4)E中发生化学反应的方程式为:________________;
(5)烧杯G中发生反应的化学方程式为:________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com