
科目: 来源: 题型:
【题目】下列有关电解质溶液的说法正确的是
A. 在蒸馏水中加入NH4NO3固体,Kw不变
B. 加水稀释FeCl3溶液,c(Fe3+)/ c(Cl-)的值减小
C. 加热蒸干并灼烧Al(NO3)3溶液得到Al(OH)3固体
D. 浓度均为0.1 mol·L-1的Na2CO3和NaHCO3的混合溶液中:3c(Na+)=2[c(CO32- )+c(HCO3-)+ c(H2CO3)]
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A. 浓度是影响化学反应速率的本质因素
B. 在容积可变的密闭容器中,发生反应H2(g)+I2(g) ![]() 2HI(g),把容积缩小一倍,正反应速率加快,平衡正向移动
2HI(g),把容积缩小一倍,正反应速率加快,平衡正向移动
C. 反应 MgCl2(l)=Mg(l)+Cl2(g)的 △H<0、△S>0
D. 化学反应速率可用单位时间内反应物的浓度变化量来表示
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )


A. 图①中ΔH1=ΔH2+ΔH3
B. 图②在催化剂条件下,反应的活化能等于E1+E2
C. 图③表示醋酸溶液滴定 NaOH溶液和氨水混合溶液的电导率变化曲线
D. 图④可表示由CO(g)生成CO2(g)的过程中要放出566 kJ 热量
查看答案和解析>>
科目: 来源: 题型:
【题目】下表是关于农作物A、B在相同土壤中N、P、K三元素肥效实验的结果记录,“+”表示施肥,“―”表示未施肥)。请据表中的数据,判断正确的结论是( )
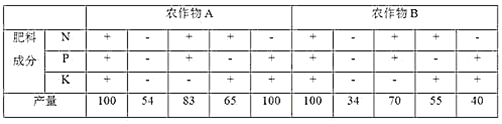
A. 对于农作物A来说,其生长发育不需要N元素
B. 对农作物A来说,施肥时最重要的是施加P肥
C. 对农作物B来说,三种元素中K最重要
D. 两种农作物对土壤中N、P、K的需求量基本相同
查看答案和解析>>
科目: 来源: 题型:
【题目】下列操作中,完全正确的一组是
①用试管夹夹持试管时,试管夹从试管底部往上套,夹在试管的中上部
②给盛有液体的体积超过![]() 容积的试管加热
容积的试管加热
③把鼻孔靠近容器口去闻气体的气味
④将试管平放,用纸槽往试管里送入固体粉末后,然后竖立试管
⑤加热坩埚要垫上石棉网
⑥将烧瓶放在桌上,用力塞紧塞子
⑦用坩埚钳夹取加热后的蒸发皿
⑧将滴管竖直伸入试管内滴加液体
⑨稀释浓硫酸时,应沿器壁缓缓地将水加入浓硫酸中
⑩用镊子从煤油中取出金属钠,再用小刀切一小块,然后将剩下的钠放回原瓶
A.①④⑦⑩B.①④⑤⑦⑩C.①④⑤⑦⑧⑩D.④⑤⑦⑩
查看答案和解析>>
科目: 来源: 题型:
【题目】硼酸(H3BO3)是一种片层状结构的白色晶体(下图),有油腻感,可做润滑剂。硼酸对人体受伤组织有缓和和防腐作用,故可以用于医药和食品防腐等方面。回答下列问题:
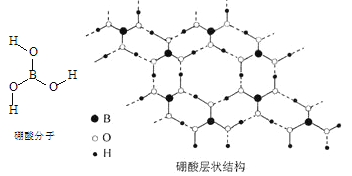
(1)B原子的结构示意图为_____________________;
(2)硼酸为一元弱酸,在水中电离方程式为H3BO3+H2O![]() [B(OH)4]-+H+,写出硼酸与NaOH溶液反应的离子方程式_________________________;
[B(OH)4]-+H+,写出硼酸与NaOH溶液反应的离子方程式_________________________;
(3)下列有关硼酸晶体的说法正确的是__________;
A.H3BO3分子的稳定性与氢键有关
B.含1 molH3BO3的晶体中有3 mol氢键
C.分子中B、O最外层均为8e-稳定结构
D.B原子杂化轨道的类型sp2,同层分子间的主要作用力是范德华力
(4)根据对角线规则,与B性质相似的元素是__________。
(5)含氧酸的通式为(HO)mROn,根据非羟基氧原子数判断,与H3BO3酸性最接近的是________;
A.HClO B.H4SiO4 C.H3PO4 D.HNO2
(6)一种硼酸盐的阴离子为B3O6n-,n=_____________;B3O6n-结构中只有一个六元环,B的空间化学环境相同,O有两种空间化学环境,画出B3O6n-的结构图(注明所带电荷数); _____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示。已知W 一种核素的质量数为 18,中子数为 10;X 和 Ne 的核外电子数相差1;在Z所在的周期中,Z元素的原子得电子能力最强;四种元素的最外层电子数之和为18。 请回答下列问题:
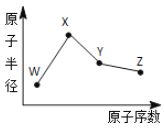
(1)X元素位于元素周期表中位置为_____________。
(2)X的单质和 Y 的单质相比,熔点较高的是____________(写化学式) 。Z所在族的简单氢化物中,沸点最高的是________(写化学式),原因为______________________。
(3)W、X、Z三种元素形成的化合物中化学键类型为_______;X2W2的电子式为_______。
(4)Z的氧化物很多,其中一种黄绿色气体 M,其氧含量为 47.41%,可用于水处理, M 在液态和浓缩气态时具有爆炸性 。 M 的化学式为___________。M可与NaOH溶液反应生成两种稳定的盐,它们的物质的量之比为 1︰5,该反应的化学方程式为___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】FeCl3在现代工业生产中应用广泛。某化学研究性学习小组模拟工业流程制备无水FeCl3,再用副产品FeCl3溶液吸收有毒的H2S。
Ⅰ.经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。他们设计了制备无水FeCl3的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
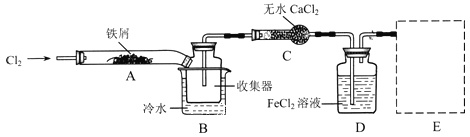
①检验装置的气密性;
②通入干燥的Cl2,赶尽装置中的空气;
③用酒精灯在铁屑下方加热至反应完成;
④……
⑤体系冷却后,停止通入Cl2,并用干燥的H2赶尽Cl2,将收集器密封。
请回答下列问题:
(1)装置A中反应的化学方程式为________________。
(2)第③步加热后,生成的烟状FeCl3大部分进入收集器,少量沉积在反应管A右端,要使沉积的FeCl3进入收集器,第④步操作是_______________。
(3)操作步骤中,为防止FeCl3潮解所采取的措施有(填步骤序号)_____________。
(4)装置B中冷水浴的作用为________________;装置C的名称为_____________;装置D中FeCl2全部反应后,因失去吸收Cl2的作用而失效,写出检验FeCl2是否失效的试剂:____________。
(5)在虚线框中画出尾气吸收装置E并注明试剂_____________。
Ⅱ.该组同学用装置D中的副产品FeCl3溶液吸收H2S,得到单质硫;过滤后,再以石墨为电极,在一定条件下电解滤液。
(6)FeCl3与H2S反应的离子方程式为____________。
(7)综合分析实验Ⅱ的两个反应,可知该实验有两个显著优点:①H2S的原子利用率为100%;②___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室制取Fe(OH)3胶体的方法是把______逐滴加在_______中,继续煮沸,待溶液呈____ 色时停止加热,其反应的离子方程式为_______________,用 __________(方法)可证明胶体已经制成,用_____方法精制胶体。
查看答案和解析>>
科目: 来源: 题型:
【题目】由P、S、Cl、Ni等元素组成的新型材料有着广泛的用途,回答下列问题。
(1)基态 Cl原子核外电子排布式为__________________________,P、S、Cl的第一电离能由大到小顺序为____________________,P、S、Cl的电负性由大到小顺序为_______________。
(2)SCl2分子中的中心原子杂化轨道类型是_____________,该分子构型为__________。
(3)Ni与CO能形成配合物Ni(CO)4,该分子中配位键个数为_______;以“—”表示σ键、“→”表示配位键,写出CO分子的结构式__________。
(4)已知MgO与NiO的晶体结构(如图1)相同, 其中Mg2+和Ni2+的离子半径分别为66 pm和69pm。则熔点:MgO_____NiO(填“>”、“<”或“=”),理由是_______________________________。
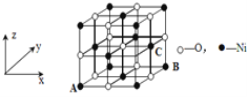
(5)若NiO晶胞中离子坐标参数A为(0,0,0),B为(1,1,0),则C离子坐标参数为_______。
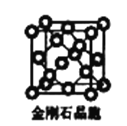
(6)金刚石晶胞含有____个碳原子。若碳原子半径为r,金刚石晶胞的边长为a,根据硬球接触模型,则r= ______a,列式表示碳原子在晶胞中的空间占有率____(请用r和a表示不要求计算结果)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com