
科目: 来源: 题型:
【题目】SAH(NaAlH4)还原性非常强。纯的四氢铝钠是白色晶状固体,在干燥空气中相对稳定,但遇水即爆炸性分解,NaH遇水蒸气也发生剧烈反应。以铝合金废边脚料为原料(主要成分为Al,含有少量Al2O3、Fe2O3、MgO、PbO和SiO2等杂质)制备四氢铝钠:
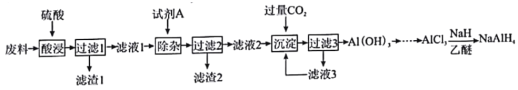
请回答下列问题:
(1)滤渣1的主要成分为____________(填化学式)。试剂A中溶质的阴、阳离子所含电子数相等,其电子式为____________。
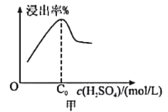
(2)已知废料接触面积、接触时间均相同,“酸浸”中铝元素浸出率与硫酸浓度的关系如图甲所示。当硫酸浓度大于C0mol/L时,浸出率降低的原因可能是__________________。
(3)滤液3可以循环利用,写出滤液2与滤液3反应的离子方程式__________________。
(4)NaAlH4与水反应的化学方程式为__________________。
(5)测定NaAlH4粗产品的纯度。
称取mgNaAlH4粗产品按如图乙所示装置进行实验,测定产品的纯度。
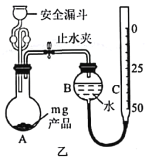
①“安全漏斗”中“安全”的含义是__________________。
②已知实验前C管读数为V1mL,向A中加入适量蒸馏水使NaAlH4完全反应,当A中反应完全后,冷却至室温后C管读数为V2mL(均折合成标准状况)。则该产品的纯度为_____________(用含m、V1和V1的代数式表示,忽略加入蒸馏水的体积)。
③若实验前读数时B管和C管液面相平,实验后读数时B管液面高于C管,则测得的结果_____________(填“偏高”“偏低”或“无影响”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】合成涤纶的流程图如下所示。
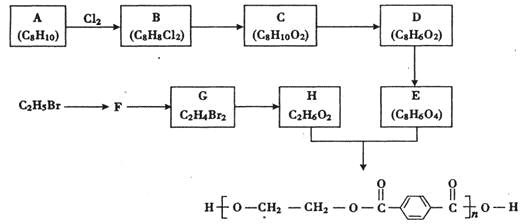
回答下列问题:
(1)A的名称为 ;
(2) F的结构简式是 ;
(3) C→D的反应类型是 ;F→G的反应类型为 ;
(4)E与H反应的化学方程式为 :
(5)E有多种同分异构体,符合下列条件的同分异构体有 种,其中在核磁共振氢谱中出现四组峰的是 (写出结构简式)。
①芳香族化合物;②红外光谱显示含有羧基;③能发生银镜反应;④能发生水解反应
(6) A也能一步转化生成E:![]() .试剂a可以用 溶液。
.试剂a可以用 溶液。
查看答案和解析>>
科目: 来源: 题型:
【题目】对于反应MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(1)MnO2在反应中____电子(填“得到”或“失去”),所含元素化合价______(填“升高”或“降低”),发生_____反应(填“氧化”或“还原”)。
(2)HCl在反应中_____电子(填“得到”或“失去”),所含元素化合价_____(填“升高”或“降低”),发生____反应(填“氧化”或“还原”)。
(3)该反应中氧化剂是___;还原剂是____;氧化产物是___ ;还原产物是____。
查看答案和解析>>
科目: 来源: 题型:
【题目】磷酸亚铁锂(LiFePO4)是目前使用量最多的一种锂电池电极材料,LiFePO4废料中(含Al、石墨)磷、铁、锂的综合回收工艺流程图:
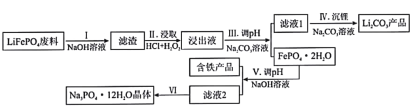
已知:①![]() ,
,![]()
②常温下,![]() ,
,![]() ,
,![]()
(1)过程I“碱浸”的目的是____________,该过程发生反应的离子方程式为_________________。
(2)过程II“酸浸”加人双氧水的目的是_________________。
(3)①浸出液中存在大量![]() 、
、![]() 离子,从平衡移动角度解释过程Ⅲ得到磷酸铁晶体的原因_________________。
离子,从平衡移动角度解释过程Ⅲ得到磷酸铁晶体的原因_________________。
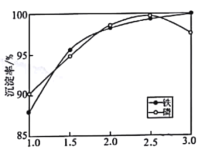
②一定条件下,探究了pH对磷酸铁沉淀的影响,结果如图所示。由图可知,过程Ⅲ应选取的最佳沉淀pH为____。随pH的增加,磷的沉淀率开始下降,而铁沉淀率未下降,分析原因为_________________。
(4)测得滤液1中c(Li+)=0.l5mol/L,某同学取该100mL滤液进行“沉锂”反应.加入50mlNa2CO3溶液却未见沉淀,若不考虑Na2CO3的水解和液体混合时的体积变化,则该同学加入的Na2CO3溶液最大浓度为c(Na2CO3)=_____________mol/L
(5)过程Ⅵ将滤液2________,________,经过滤、干燥后得Na3PO4·12H2O晶体。
查看答案和解析>>
科目: 来源: 题型:
【题目】(14分)溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
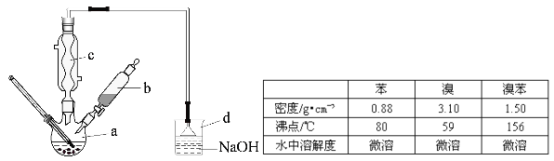
按下列合成步骤回答问题:
(1)在a中加入15mL无水苯和少量铁屑,在b中小心加入4.0mL液态溴,向a中滴入几滴溴,有白色烟雾产生,是因为生成了 气体。继续滴加至液溴滴完,装置d的作用是 ;
(2)液溴滴完后,经过下列步骤分析提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤。NaOH溶液洗涤的作用是 ③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤,加入氯化钙的是 ;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为 ,要进一步提纯,下列操作中必须的是 (填入正确选项前的字母);
A.重结晶 B.过滤 C.蒸馏 D.萃取
(4)在该实验中,a的容积最适合的是 (填入正确选项前的字母)。
A.25mL B. 50mL C.250mL D.500mL
查看答案和解析>>
科目: 来源: 题型:
【题目】H2C2O4是一种二元弱酸。常温下向H2C2O4溶液中滴加KOH溶液,混合溶液中离子浓度与pH的关系如图所示,其中![]() 或
或![]() 。下列说法正确的是
。下列说法正确的是
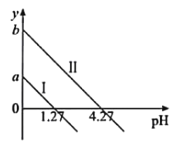
A.直线I表示的是![]() 与pH的变化关系
与pH的变化关系
B.图中纵坐标应该是a=1.27,b=4.27
C.c(![]() )>c(
)>c(![]() )>c(H2C2O4)对应1.27<pH<4.27
)>c(H2C2O4)对应1.27<pH<4.27
D.c(K+)=c(![]() )+c(
)+c(![]() )对应pH=7
)对应pH=7
查看答案和解析>>
科目: 来源: 题型:
【题目】为探究不溶性盐X(仅含四种元素)的组成和性质,设计并完成如图实验:
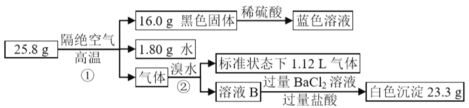
请回答:
(1)X的化学式为______________。
(2)请写出反应①的化学方程式:______________。
(3)请写出反应②的离子方程式:______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列由实验操作得到的实验现象或结论不正确的是
实验操作 | 实验现象或结论 | |
A | 向某溶液中加入稀硫酸,生成淡黄色沉淀和有刺激性气味的气体 | 该溶液中一定含有S2O32- |
B | 向3ml KI溶液中滴加几滴溴水,振荡,再滴加1mL淀粉溶液,溶液显蓝色 | 氧化性:Br2>I2 |
C | 相同条件下,测定等浓度的Na2CO3溶液和Na2SO4溶液的pH,前者呈碱性,后者呈中性 | 非金属性:S>C |
D | 将镁条点燃后迅速伸入集满CO2的集气瓶 | 集气瓶中产生浓烟并有黑色颗粒产生 |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】高纯氢的制备是目前的研究热点,利用太阳能光伏电池电解水制高纯氢,工作示意图如图所示。下列有关说法正确的是
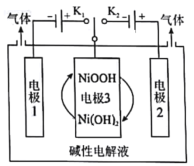
A.连接K1可以制取O2
B.电极2发生反应2H2O+2e-=H2↑+2OH-
C.电极3的主要作用是通过NiOOH和Ni(OH)2相互转化提供电子转移
D.连接K2溶液的pH减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com