
科目: 来源: 题型:
【题目】硫酸铜是一种应用极其广泛的化工原料;以下是某工厂用含铁废铜为原料生产胆矾(CuSO45H2O)和副产物石膏(CaSO42H2O)的生产流程示意图:
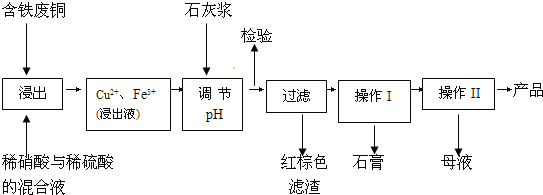
胆矾和石膏在不同温度下的溶解度(g/100g水)见表。
温度(℃) | 20 | 40 | 60 | 80 | 100 |
石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
胆矾 | 32 | 44.6 | 61.8 | 83.8 | 114 |
请回答下列问题:
(1)红棕色滤渣的主要成分是___;
(2)写出浸出过程中生成硫酸铜的离子方程式___;
(3)操作I包括蒸发浓缩、__等操作,温度应该控制在__℃左右;
(4)从溶液中分离出硫酸铜晶体的操作Ⅱ应为__、___、洗涤、干燥;晶体用无水乙醇作洗涤液而不用蒸馏水的原因是__;干燥时采用晾干,不用加热烘干的原因是___。
(5)取样检验是为了确认Fe3+是否除净。有同学设计了以下两种方案,在实验室分别对所取样品按下列方案进行操作:
方案一:取样于试管→滴加KSCN溶液; 方案二:纸层析→喷KSCN溶液;
①你认为上述两种方案设计更合理的是__;
②指出你认为不合理方案存在的问题是__。
查看答案和解析>>
科目: 来源: 题型:
【题目】—股淡淡清香能给人心旷神怡的感觉,主要由香精、酒精和水构成的香水备受爱美人士的青睐。香精里面含有酯类物质,工业上以A为主要原料来合成乙酸乙酯,其合成路线如下图所示,其中A是石油裂解气的主要成分,A的产量通常用来衡量一个国家的石油化工水平。又知2CH3CHO+O2![]() 2CH3COOH。请回答下列问题:
2CH3COOH。请回答下列问题:
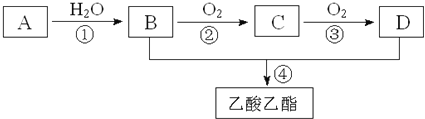
(1)写出A的电子式__________;
(2)B、D分子内含有的官能团分别是__________、__________(填名称);
(3)写出下列反应的反应类型:①______________,④______________;
(4)写出下列反应的化学方程式:
①__________________________________________________;
②__________________________________________________;
④__________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】现有NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂除去杂质,从而得到纯净的NaNO3晶体,相应的实验流程如图所示。

请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X___,沉淀A____。
(2)上述实验流程中①②③步均要进行的实验操作是___(填操作名称)。
(3)上述实验流程中加入过量Na2CO3溶液的目的是______________________________。
(4)按此实验方案得到的溶液3中肯定含有______(填化学式)杂质。为了解决这个问题,可以向溶液3中加入适量的___(填化学式),之后若要获得NaNO3晶体,需进行的实验操作是____(填操作名称)。
查看答案和解析>>
科目: 来源: 题型:
【题目】钠、铝、铁是三种重要的金属。请回答:
(1)三种金属与同浓度盐酸反应,反应最慢的是___(填选项)。
a.钠 b.铝 c.铁
(2)金属钠与水发生反应的离子方程式为___;(填选项)
a.2Na +2H2O=2NaOH+H2↑
b.2Na+2H2O=2Na++2OH-+H2↑
c.2Na +2H2O=2Na++2OH-+O2↑
(3)可观察到的实验现象正确的是__(填选项)。
a.钠沉到水底 b.钠熔成小球 c.小球四处游动
(4)填写a、b、c化学式并书写①的化学方程式(a、b、c均为含Al化合物);
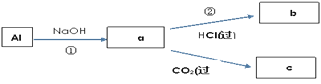
a:___,b:___,c:___;
①____________;
(5)Fe跟Cl2在一定条件下反应,所得产物为___。
(6)将该产物溶于水配成溶液,分装在两支试管中。请回答:
a.若向其中一支试管中滴加KSCN溶液,则溶液变成__色。
b.向另一支试管中滴加NaOH溶液,产生__色沉淀。
查看答案和解析>>
科目: 来源: 题型:
【题目】请根据物质的量的相关公式,完成下列问题。(注意书写单位)
(1)3.01×1023个NH3分子的物质的量__。
(2)0.5molH2SO4含有的氧原子的物质的量__。
(3)2.3gNO2的物质的量__。
(4)标况下,33.6LN2的物质的量___。
(5)0.5mol /LK2SO4溶液中,c(K+)=__。
查看答案和解析>>
科目: 来源: 题型:
【题目】现用Na2SO4固体来配制480mL0.2mol·L-1的Na2SO4溶液。可供选择的仪器如图:
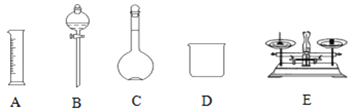
(1)如图所示的仪器中配制溶液不需要的是__ (填选项),配制上述溶液还需用到的玻璃仪器是___、__ (填仪器名称)。
(2)使用容量瓶之前必须进行的操作是___。(填选项)
A.检查气密性 B.检查是否漏水 C.烘干
(3)经计算,需Na2SO4的质量为___g。
(4)你选用的容量瓶规格为___mL。
(5)配制溶液时,一般可分为以下几个步骤:
①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容
其操作顺序:②→__→__→__→__→__→__(填序号)。___
(6)在配制过程中,其他操作都准确,定容时俯视刻度线会使所配溶液浓度__(填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】金属在人类社会发展进程中发挥了重要作用,钠、镁、铝、铁、铜是最重要的几种金属。
(1)上述五种金属中人们发现并最早制得其单质的是_____________。
(2)这五种金属单质都具有的性质是_________________(填下列选项的序号)。
a.导电性 b.延展性 c.银白色 d.熔点高 e.硬度大
(3)钠、镁、铝、铁四种金属中,不能用于从氯化铜溶液中置换出铜的金属是_________,原因是 _________(用必要的化学方程式表示)。
(4)上述金属中,有一种金属的氧化物能在另一种金属的氢氧化物的水溶液中溶解,写出反应的离子方程式:_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】K3[Fe(C2O4)3]·3H2O〔三草酸合铁(Ⅲ)酸钾晶体〕是制备负载型活性铁催化剂的主要原料,也是一些有机反应很好的催化剂。下图是在实验室制备K3[Fe(C2O4)3]·3H2O的流程:
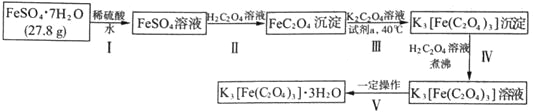
回答下列问题:
(1)步骤I中加入稀硫酸的目的是_______________。
步骤II中发生的主要化学反应为一可逆过程,其离子方程式为_______________。
常温下,该反应的平衡常数K=_______________[已知常温下:Ka1(H2C2O4)=5.6×10-2、Ka2(H2C2O4)=5.4×10-5、Ksp(FeC2O4)=2.1×10-7]
(2)下列试剂均可将FeC2O4氧化为K3[Fe(C2O4)3],最适宜作为“试剂a”的是_______________(填序号)
a.氯水b.酸性KMnO4溶液c.H2O2溶液d.稀硝酸
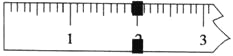
(3)使用托盘天平称量制得的K3[Fe(C2O4)3]·3H2O的质量。天平平衡时,右盘内砝码的总质量为20 g.游码示数如图所示,则制得晶体的质量为___________g,该实验中K3[Fe(C2O4)3]·3H2O的产率为_______________。(已知: K3[Fe(C2O4)3]·3H2O的相对分子质量为491,FeSO4·7H2O的相对分子质量为278)
(4)某研究小组将K3[Fe(C2O4)3〕在一定条件下加热分解后,利用下图所示装置(可重复使用)确认所得含碳元素的气体产物为CO和CO2。
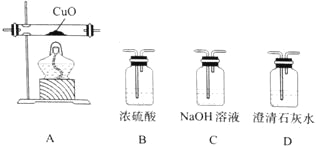
按气流从左到右的方向,装置的连接顺序为_______________(填装置序号) ;确认气体产物中含CO的现象为_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A是一种不溶于水的固体非金属氧化物,根据图中的转化关系,回答:
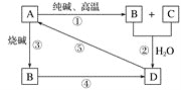
(1)A是______,B是_____,D是_____。
(2)写化学方程式:
①_________;
⑤_________。
(3)写离子方程式:
②__________;
③________;
④________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)合成氨工业生产中所用的αFe催化剂的主要成分是FeO、Fe2O3。
①某FeO、Fe2O3混合物中,铁原子、氧原子的物质的量之比为4∶5,其中FeO、Fe2O3的物质的量之比为________。
②当催化剂中+2价铁与+3价铁的物质的量之比为1∶2 时,其催化活性最高,此时铁的氧化物的混合物中铁的质量分数为________(用小数表示,保留两位小数)。
(2)电子工业常用30%的FeCl3溶液腐蚀绝缘板上的铜箔,制造印刷电路板。
①用FeO、Fe2O3和稀盐酸、氯气制取FeCl3溶液的离子方程式包括_______________
②写出FeCl3溶液与金属铜发生反应的化学方程式:____
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com