
科目: 来源: 题型:
【题目】NH3分解的热化学方程式为![]() .在Co-Al催化剂体系中,压强P0下,氨气以一定流速通过反应器,得到不同催化剂下氨气的转化率随温度的变化曲线如图所示。
.在Co-Al催化剂体系中,压强P0下,氨气以一定流速通过反应器,得到不同催化剂下氨气的转化率随温度的变化曲线如图所示。
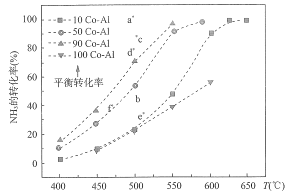
下列说法错误的是
A.活化能最小的催化剂是 90 Co-A1
B.如果增大气体流速,则b点对应的点可能为e
C.温度为T时,向体积为1L的恒容容器中加入0.8 molNH3和0.1molH2,达到平衡时,NH3的转化率为75%,则平衡常数为K=7.5
D.在两个体积均为VL的绝热密闭容器中分别投入①2 mol NH3,②3 mol H2和1mol N2,达到平衡时,NH3的体积分数相同
查看答案和解析>>
科目: 来源: 题型:
【题目】300℃下,在一容积为2 L的恒容密闭容器中加入0.2 mol CO和0.4 mol H2,发生如下反应:CO(g)+2H2(g) ![]() CH3OH(g) 。下列各物理量随反应时间变化趋势的曲线不正确的是
CH3OH(g) 。下列各物理量随反应时间变化趋势的曲线不正确的是
A. 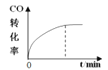 B.
B. 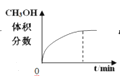
C. 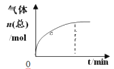 D.
D. 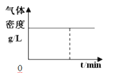
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下,体积为5L的密闭容器中,0.5molX和0.5molY进行反应:
2X(g)+Y(g)![]() 2Z(g),经60s达到平衡,生成0.2molZ。下列说法正确的是:
2Z(g),经60s达到平衡,生成0.2molZ。下列说法正确的是:
A. 将容器体积变为10L,Z的平衡浓度变为原来的![]()
B. 在该温度下,该反应的平衡常数K=0.011
C. 达到平衡时,容器内气体的压强是原来的90%
D. 若降低温度,X的体积分数增大,则该反应的△H<0
查看答案和解析>>
科目: 来源: 题型:
【题目】铁是人类较早使用的金属之一。运用铁及其化合物的知识,完成下列问题。
(1)向沸水中逐滴滴加1 mol/L FeCl3溶液,至液体呈透明的红褐色,该分散系中粒子直径的范围是____________nm。
(2)电子工业需要用30 %的FeCl3溶液腐蚀敷在绝缘板上的铜片制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式______________________________________。某同学对FeCl3腐蚀铜后所得溶液的组成进行测定:取少量待测溶液,滴入KSCN溶液呈红色,则溶液中所含金属阳离子有________________。
(3)若要验证该溶液中含有Fe2+,正确的实验方法是________(用字母代号填)。
A.向试管中加入试液,滴入KSCN溶液,若显血红色,证明含有Fe2+。
B.向试管中加入试液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+。
C.向试管中加入试液,先滴入KSCN溶液,无现象,再滴加氯水,若显血红色,证明原溶液中含有Fe2+
(4)欲从废液中回收铜,并重新获得FeCl3溶液设计实验方案如下:
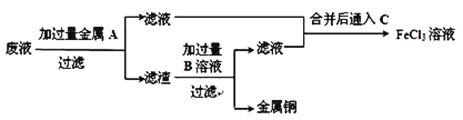
①写出上述实验中有关物质的化学式:A:__________;B:__________。
②写出通入 C的化学方程式_____________________________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】铬矿是冶金、国防、化工等领域不可缺少的矿产资源,其中的铬铁矿是唯一可开采的铬矿石。工业上常用铬铁矿(主要含Fe2O3、FeO和Cr2O3,还含有MgO、Al2O3、SiO2等杂质)为原料制备重铬酸钾和三氧化二铁,其流程如图所示。

已知常见离子开始生成沉淀和沉淀完全的pH如下表所示。

请回答下列问题:
(1)铬铁矿与熔融 NaOH 和 NaCIO3的反应是在坩埚中进行的,可用作此坩埚材料的是___________.
A.镍 B.刚玉(Al2O3) C. 陶瓷 D.石英
(2)写出铬铁矿中的Cr2O3与熔融 NaOH和NaCIO3反应的化学方程式:___。由于在该过程中铁元素会大量转变为NaFeO2,所以加水的作用为__________________(用离子方程式表示)。
(3)“滤渣 2”的主要成分为_________(填化学式)。
(4)利用化学平衡移动原理解释调节pH2约至4.5的原因是;再向其中加入KC1固体,蒸发浓缩至液体表面有晶膜产生,冷却结晶,过滤得到粗重铬酸钾晶体。为获得高纯度重铬酸钾晶体,可采取___________(填操作名称)。
(5)调节pH3的范围为__________
(6)已知铬铁矿中铁、铬元素的质量比为14:13.上述流程中铁元素转化为Fe2O3的利用率为60%,提取铬元素的转化率为90%,如果得到Fe2O3的质量为32t,则可以制备K2Cr2O7的质量为______t(结果保留1位小数)。
查看答案和解析>>
科目: 来源: 题型:
【题目】1mol过氧化钠与1.6mol碳酸氢钠固体混合后,在密闭的容器中加热充分反应,排出气体物质后冷却,残留的固体物质是 ( )
A. Na2CO3 B. NaOH、Na2CO3 C. Na2O2、 Na2CO3 D. Na2O2、 NaOH 、Na2CO3
查看答案和解析>>
科目: 来源: 题型:
【题目】磷酸氯喹在细胞水平上能有效抑制新型冠状病毒的感染,可由氯喹(H)与磷酸在一定条件下制得,它的一种合成方法如下:
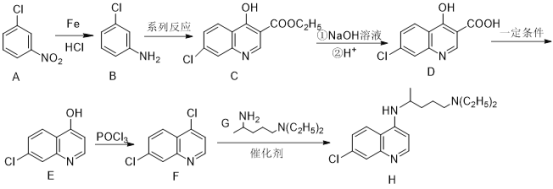
已知: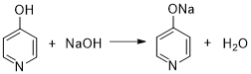
回到下列问题:
(1)A中含有的官能团名称为_____________。
(2)B的分子式为_____________。
(3)碳原子上连有4个不同的原子或基团时,该碳原子称为手性碳原子,H中有_________个手性碳原子。
(4)F→H的反应类型为_____________。
(5)C与NaOH溶液反应的化学方程式为___________________________________________。
(6)E与氢气反应后的产物M的分子式为C9H8NOCl,符合下列条件的M有__________种。
①遇FeCl3溶液发生显色反应 ②除苯环外不含其他环状结构
③苯环上只有2个取代基 ④含有-NH2和![]()
其中核磁共振氢谱有5组峰,且峰面积之比为1:2:2:1:2的M的结构简式为___________。(任写2种)
查看答案和解析>>
科目: 来源: 题型:
【题目】H2NCOONH4(59℃时升华并分解)可用作磷化铝中间体及医药等。可由干燥的NH3与CO2在低温下(或冰水浴)制取,装置如图所示:
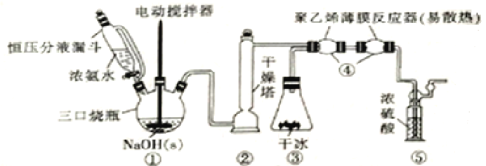
回答下列问题:
(1)装置①中用“恒压分液漏斗”代替普通的分液漏斗,其优点是_____________,滴入浓氨水并搅拌能产生大量NH3的原因是____________________,装置②干燥塔中盛放的合适干燥剂是_____________(填名称)。
(2)装置③用盛干冰装置代替实验室制备CO2的常见制备及纯化转置,其优点除装置简洁且可产生纯净干燥的CO2外,还具有的优点是____________________________________。
(3)装置④用“聚乙烯薄膜反应器”代替反应管的优点是____________,“聚乙烯薄膜反应器”中发生反应的化学方程式为_____________________________________________。
(4)从环境保护角度分析,装置⑤的作用是_____________,还可以通过观察气泡确定NH3和CO2的比例是否合适,判断的依据及不合适时的调节方案为________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验是化学研究的基础。关于下列各实验装置图的叙述中正确的是( )

A. 装置①常用于分离互不相溶的液态混合物
B. 装置②可用于吸收氨气,且能防止倒吸
C. 用装置③不可以完成“喷泉”实验
D. 用装置④稀释浓硫酸和铜反应冷却后的混合液
查看答案和解析>>
科目: 来源: 题型:
【题目】CS2是一种常见溶剂,还可用于生产人造粘胶纤维等。回答下列问题:
(1)CS2与酸性KMnO4溶液反应,产物为CO2和硫酸盐,该反应中还原剂与氧化剂的物质的量之比为__________(MnO4-被还原为Mn2+)。
(2)甲烷硫磺法制取CS:的反应为CH4(g)+2S2(g)![]() CS2(g)+2H2S(g) △H
CS2(g)+2H2S(g) △H
①在恒温恒容密闭容器中进行该反应时,能说明该反应已达到平衡状态的是_________(填字母)。
A.v正(S2)=2v逆(CS2)
B.容器内气体的密度不再随时间变化
C.容器内气体的总压强不再随时间变化
D.单位时间内断裂C-H键数目与断裂H-S键数目相等
②已知下列键能数据:
共价键 | C-H | S=S | C=S | H-S |
键能/ | 411 | 425 | 573 | 363 |
该反应的△H=_________kJ·mol-1。
(3)在一密闭容器中,起始时向该容器中充入H2S和CH4且n(H2S):n(CH4)=2:1,发生反应:CH4(g)+2H2S(g)![]() CS2(g)+4H2(g)。0.1MPa时,温度变化对平衡时产物的物质的量分数的影响如图所示:
CS2(g)+4H2(g)。0.1MPa时,温度变化对平衡时产物的物质的量分数的影响如图所示:
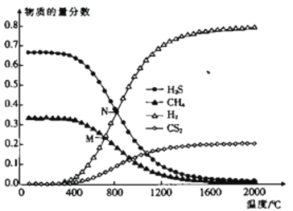
①该反应△H_________(填“>”或“<”)0。
②M点对应温度下,H2S的平衡转化率为_________,为提高H2S的平衡转化率,除改变温度外,还可采取的措施是___________________________(列举一条)。
③N点,平衡分压p(CS2)=_________MPa,对应温度下,该反应的Kp=_________(MPa)2。(Kp为以分压表示的平衡常数)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com