
科目: 来源: 题型:
【题目】将2.32g碳酸钠、氢氧化钠的固体混合物完全溶解于水,制成溶液,然后向该溶液中逐滴加入1mol/L的盐酸,所加盐酸的体积与产生CO2的体积(标准状况)关系如图所示,下列说法中正确的是
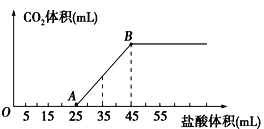
A.OA段发生反应的离子方程式为:H++OH-=H2O
B.当加入35mL盐酸时,产生CO2的体积为224mL
C.A点溶液中的溶质为NaC1、Na2CO3
D.混合物中NaOH的质量0.60g
查看答案和解析>>
科目: 来源: 题型:
【题目】废物利用有利于环境保护、资源节约,一种从废催化剂(含ZnO、CuO及少量石墨、Fe2O3及MnO2等)回收铜并制取活性氧化锌的工艺流程如图:
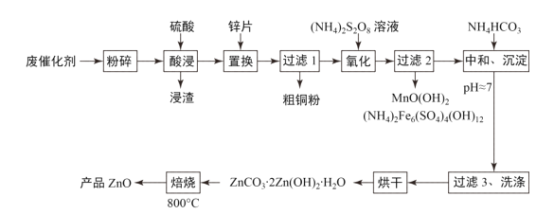
(1)为提高酸浸的速率,还可采取的措施为___。
(2)“氧化”时2molMn2+被氧化为MnO(OH)2,需要(NH4)2S2O8的物质的量为___。
(3)已知Zn(OH)2性质与Al(OH)3类似,在“中和、沉淀”时pH不能过大,请用文字结合离子方程式解释原因___。
(4)“过滤3、洗涤”时,对所得滤液蒸发浓缩、冷却结晶可得___(填主要物质的化学式)固体。
(5)“焙烧”过程中化学方程式为___。
(6)经测定,1kg废催化剂可得160g粗铜粉,又知粗铜粉中铜的质量分数为80%,则废催化剂中铜的质量分数为___%,若“酸浸”时硫酸浓度变小而又没有及时补充,则测定结果会比实际情况___(填“偏大”“偏小”或“无影响”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】向300 mL 1 mol·L-1的稀硝酸中,加入5.6 g铁粉,充分反应后,铁粉全部溶解(假设还原产物只有NO),下列说法不正确的是( )
A. 最终所得溶液中既有Fe2+又有Fe3+
B. 最终溶液中,硝酸无剩余
C. 标准状况下生成NO的体积为1.68 L
D. 再向最终所得溶液中滴加稀硝酸,无明显变化
查看答案和解析>>
科目: 来源: 题型:
【题目】炼铁的矿物主要有赤铁矿、磁铁矿和菱铁矿等。目前主要采用以下流程测定铁矿石中铁元素的含量,流程分为两个环节:铁矿石预处理和重铬酸钾滴定。
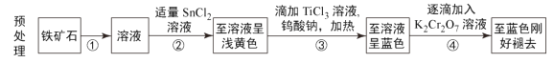
滴定过程:向预处理结束的溶液中加入适量蒸馏水和硫酸磷酸混合酸,滴加数滴二苯胺磺酸钠,用重铬酸钾标准溶液滴定,记录终点体积V。
已知:i.钨酸钠(Na2WO4)可用作指示剂,若钨由+6价变为+5价,则溶液变为蓝色。
ii.Sn2+和Ti3+均具有还原性。
iii.氧化性顺序为Cr2O72->Fe3+>WO42-。
iV.二苯胺磺酸钠可用作氧化还原指示剂,本身无色,被氧化后呈现紫红色。
请回答下列问题:
(1)①过程需要加入过量的___(填试剂名称),试剂过量的理由为___。
(2)②过程后的浅黄色溶液中铁的存在形式为___,③过程后的蓝色溶液中铁的存在形式为___。
(3)④过程中K2Cr2O7的作用为___。
(4)滴定时,滴定管应选用___(填“甲”或“乙”);若滴定结束时,仰视读数,则测得结果___(填“偏大”“偏小”或“无影响”)
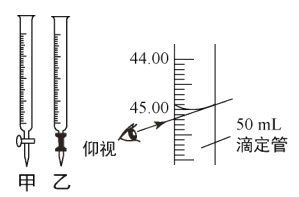
(5)滴定过程中,以二苯胺磺酸钠为指示剂,滴定终点观察到的现象为___。
(6)现称取0.4g铁矿石进行测定,滴定时共消耗45.00mL0.01mol·L-1K2Cr2O7溶液,则该铁矿石中铁的质量分数为___ %(保留1位小数)。
查看答案和解析>>
科目: 来源: 题型:
【题目】有机化合物是工业上合成锅炉防腐剂的中间体,E(![]() )的一种合成路线如下:
)的一种合成路线如下:
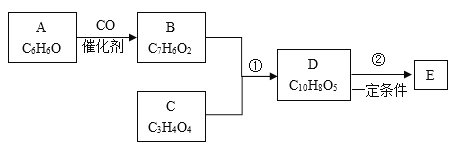
已知:
①R1CHO+R2CH2COOH![]() R1CH=CR2COOH;
R1CH=CR2COOH;
②RCH=C(COOH)2![]() RCH=CHCOOH+CO2
RCH=CHCOOH+CO2
回答下列问题:
(1)有机物A的化学名称为___________。
(2)1mol有机物C最多能与2molNaHCO3反应,C的结构简式为_____,有机物B中含有官能团的名称为_______。
(3)有机物D能发生的化学反应有____(填字母)。
a.加成反应b.消去反应c.水解反应d.氧化反应
(4)写出E在一定条件下生成聚酯的化学方程式:_______。
(5)有机物F分子比化合物B多了一个CH2原子闭,满足下列条件的F的同分异构体有_____种(不含立体异构),其中核磁共振氢谱为五组峰的物质的结构简式为_______。
①遇氯化铁溶液发生显色反应;②能发生银镜反应。
(6)已知:CH3CH=CH2+Cl2![]() ClCH2CH=CH2+HCl。以丙烯为原料(其他无机物任选)涉及制备化合物C的合成路线__________________________。
ClCH2CH=CH2+HCl。以丙烯为原料(其他无机物任选)涉及制备化合物C的合成路线__________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】溴化苯(基)硒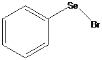 有剧毒,是一种合成有机硒化合物的重要中间体。可由乙酸基笨基硒在四氯化碳中与溴反应经乙酸处理得到,回答下列问题:
有剧毒,是一种合成有机硒化合物的重要中间体。可由乙酸基笨基硒在四氯化碳中与溴反应经乙酸处理得到,回答下列问题:
(1)Br原子核外能量高的能层符号是__________,其基态原子价电子排布式为_______。
(2)C、N、O三种原子的第一电离能由大到小的顾序为_______。
(3)乙酸分子中碳原子的杂化方式为_______。
(4) H2Se的沸点_______(填“>”“<”或“=”)H2S,原因是_______。
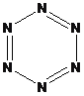
(5)晶体氮(N6)的结构如下图所示,其熔点为70℃,晶体氮中存在的作力有_______。
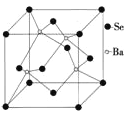
(6)BaSe可用于光电池,其晶胞结构如上图所示,晶胞参数a=0.786nm,NA代表阿伏加徳罗常数,列式计算BaSe晶胞密度为____gcm-3。
查看答案和解析>>
科目: 来源: 题型:
【题目】等质量的镁分别在足量的二氧化碳、氧气中燃烧,有关叙述正确的是( )
A.在二氧化碳中燃烧产生的固体质量大
B.在氧气中产生的氧化镁质量大
C.氧化剂与还原剂物质的量之比都是2∶1
D.反应中都是氧元素被还原
查看答案和解析>>
科目: 来源: 题型:
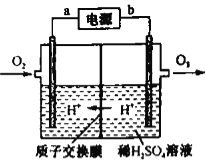
【题目】臭氧(O3)主要分布在大气层的平流层中,能够吸收紫外线,被称为地球的保护伞。回答下列问题:
(1)NOx对臭氧层的破坏作用极大,已知:①NO+O3=NO2+O2 K1;NO2+O2=NO+O3; K2;③O2+O=O3 K3,反应2O3=3O2的平衡常数K=_______ (用K1、K2、K3表示),写出一种保护臭氧层的措施:__________。
(2)用臭氧氧化烟气中的SO2的主要反应为SO2(g)+O3(g)=SO3(g)+O2(g) △H,已知①2SO2(g)+O2(g)=2SO3(g) △H1=-198kJ/mol,②2O3(g)=3O2(g) △H2=+284.2kJ/mol
①上述反应中△H= ____kJmol-1。
②一定温度下,向2L固定容积的密闭容器中加入2molO3和2molSO2发生上述反应,5min后达到平衡,测得容器中含有0.4molL-1SO3,此时SO2的转化率为_______,欲提高O3的利用率可采取的措施有_______(填字母)。
a.适当增大压强 b.升高温度 c.使用优质催化剂 d.及时分离出SO3
(3)工业上用CaSO3悬浊液吸收上述转化生成的SO3可制备石膏。已知:298K时Ksp(CaSO4)=9.0×10-6,Ksp(CaSO3)=1.5×10-7,向1LCaSO3悬浊液中加入Na2SO4,若有0.1molCaSO3参与反应,则需加入_______molNa2SO4。
 ,
,
(4)工业上可采用惰性电极电极电解稀硫酸的方法制备O3,反应装置如上图所示,电源的a极为_____极,通入O2的电极反应式为_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】钒(V)是人体必需的微量元素,能预防突发性心脏病等疾病,其常见化合价有+2、+3、+4、+5,实验室模拟工业生产制备V2(CO3)3的步骤如下:
I.取18.20gV2O5放入水中搅拌形成悬浊液,在酸性条件下,通入二氯化硫充分反应可得V2(SO4)3溶液;
II.将V2(SO4)3溶液与足量的碳酸钠溶液混合,充分反应后过滤,洗涤、干燥,得V2(CO3)3固体22.56g。
已知:+5价V具有氧化性,+3价V具有还原性,易被氧气氧化。
回答下列问题:
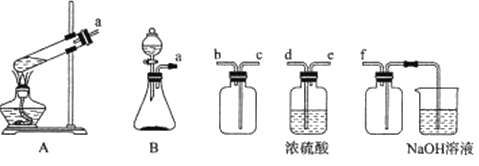
(1)实验室用Na2SO3固体和H2SO4(浓)制取SO2,可选用的发生装置是_____(填“A”或“B”),利用下述装置制取并收集干燥的SO2,连接顺序为a—____—____—____—_____—f。
(2)步骤I的装置如下;
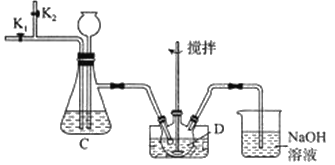
①盛放V2O5的仪器D的名称是_____,装置C中长颈漏斗的作用是_______。
②通入二氧化硫前和实验结束后都要通入N2,目的是________。
③写出步骤I中反应的离子方程式:___________。
(3)步骤II的洗涤操作中,证明已经洗净的方法是_________;实验中V2(CO3)3的产率为_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D四种化合物,其中B、C、D 焰色反应均为黄色,而A的焰色反应为紫色,B、D和盐酸反应均得到C,将固体B加热分解可得到D,若在D的溶液中通入一种无色无味气体,又可得到B的溶液;若A的溶液滴加到FeCl2溶液中,先出现白色沉淀迅速变成灰绿色,最后变成红褐色沉淀E。
(1)试推断各物质的化学式:
A:___ B:___ C:___
(2)按要求写出下列方程式:
①D与盐酸反应的离子方程式:___;
②E固体受热分解的化学方程式:___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com