
科目: 来源: 题型:
【题目】按要求填写下列空白
(1)写出Na2O2的电子式_____
(2)Al(OH)3在碱性溶液中的电离方程式为_____
(3)用离子方程式表示Na2S溶液呈碱性的原因_____
(4)在锌粒与稀硫酸的反应体系中,若滴加几滴CuSO4溶液,发现放出气体的速率明显加快,说明其原因:_____;若加入少量醋酸钠固体,发现放出气体的速率明显减慢,说明其原因_____。
(5)用惰性电极电解U形管中的饱和食盐水(已滴加酚酞),_____极附近溶液会变红。写出用惰性电极电解氯化铜溶液的化学反应方程式_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室用碳酸钠晶体配制1.00mol/L的Na2CO3溶液100mL,造成所配溶液浓度偏高的原因是( )
A. 烧杯和玻璃棒没有洗涤
B. 向容量瓶转移液体时,容量瓶事先用蒸馏水洗涤
C. 定容时俯视刻度线
D. 称量碳酸钠晶体(Na2CO310H2O)的烧杯未干燥
查看答案和解析>>
科目: 来源: 题型:
【题目】将含amol金属钠和bmol金属铝的合金投入mg足量水中,完全溶解,无金属剩余,所得溶液密度为dgcm﹣3,下列相关计算式子中错误的是( )
A.NaOH的物质的量:(a﹣b)mol
B.NaAlO2的物质的量浓度:![]() mol/L
mol/L
C.标况下生成H2的体积:![]() L
L
D.参加反应的水的质量:18(a+1.5b)g
查看答案和解析>>
科目: 来源: 题型:
【题目】实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。现有一定量的铁铝合金与很稀的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液x中,逐滴加入4molL﹣1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。则下列有关计算和判断正确的是( )
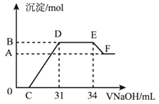
A.溶液x中所含的阳离子有:Al3+、H+、Fe3+、Fe2+
B.在DE段,发生反应的离子方程式为NH4++OH﹣→NH3H2O
C.无法求出B点对应的沉淀的物质的量
D.C点对应的氢氧化钠溶液的体积为7mL
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙两烧杯中各盛放有100mL2mol/L的盐酸和NaOH溶液,向两烧杯中分别加入等质量的铝粉,充分反应结束后测得生成的气体体积比为甲:乙=3:4,则加入铝粉的质量为( )
A.4.8gB.3.2gC.2.4gD.1.6g
查看答案和解析>>
科目: 来源: 题型:
【题目】从铝土矿中提取铝的工艺流程如下图所示,回答下列问题:
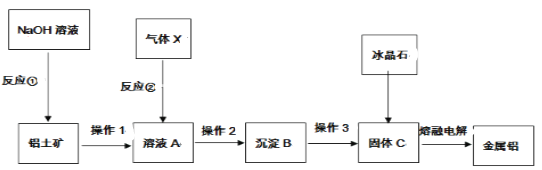
(1)气体X是___________(填化学式)。
(2)写出反应①、反应②的离子方程式:
①_________________________________;②_________________________________。
(3)操作1和操作2都是_____________,该操作要用到的玻璃仪器是:_______、____、_______。
(4)冰晶石的作用是_____________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃时,在20mL0.1molL﹣1NaOH溶液中逐滴加入0.2molL﹣1的某一元弱酸HX溶液,曲线如图所示,有关粒子浓度关系的比较中,错误的是( )

A.在A点:c(Na+)>c(OH﹣)>c(X﹣)>c(H+)
B.在B点:c(OH﹣)=c(H+)=c(Na+)=c(X﹣)
C.在C点:c(X﹣)>c(Na+)>c(H+)>c(OH﹣)
D.在C点:c(X﹣)+c(HX)=2c(Na+)
查看答案和解析>>
科目: 来源: 题型:
【题目】研究电化学腐蚀及防护的装置如右图所示。下列有关说法错误的是( )

A. d为石墨,铁片腐蚀加快
B. d为石墨,石墨上电极反应为:O2 + 2H2O + 4e == 4OH–
C. d为锌块,铁片不易被腐蚀
D. d为锌块,铁片上电极反应为:2H+ + 2e == H2↑
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物M的结构结构简式如图所示。关于M,下列说法正确的是( )
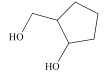
A.分子中所有碳原子可能共平面
B.M的同分异构体中,能与饱和NaHCO3溶液反应有9种
C.可使酸性高锰酸钾溶液褪色
D.1molM与足量的钠反应可以生成22.4LH2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com