
科目: 来源: 题型:
【题目】根据下列事实书写的离子方程式正确的是( )
A.用酸性高锰酸钾标准溶液滴定草酸:![]()
B.向![]() 溶液中加入
溶液中加入![]() 溶液得到
溶液得到![]() 沉淀:
沉淀:![]()
C.向![]() 溶液中加入足量稀氨水:
溶液中加入足量稀氨水:![]()
D.用铁电极电解饱和食盐水:![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上合成氨反应的能量变化如图所示,该反应的热化学方程式是
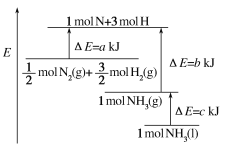
A. N2(g)+3H2(g)=2NH3(l) ΔH=2(a-b-c)kJ·mol-1
B. N2(g)+3H2(g)=2NH3(g) ΔH=2(b-a)kJ·mol-1
C. ![]() N2(g)+
N2(g)+![]() H2(g)=NH3(l) ΔH=(b+c-a)kJ·mol-1
H2(g)=NH3(l) ΔH=(b+c-a)kJ·mol-1
D. ![]() N2(g)+
N2(g)+![]() H2(g)=NH3(g) ΔH=(a+b)kJ·mol-1
H2(g)=NH3(g) ΔH=(a+b)kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物G是一种重要的有机产品,其合成路线如下:
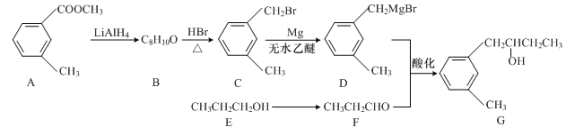
(1)E→F的反应还需的反应物和反应条件为_____。
(2)B的结构简式是_____。
(3)写出同时满足下列条件的A的一种同分异构体的结构简式:_______。
①分子中有4种不同化学环境的氢;
②能发生银镜反应和水解反应,且1mol该物质最多能与2mol NaOH反应。
(4)写出以![]() 和CH3CHO为原料,制备
和CH3CHO为原料,制备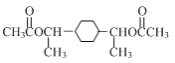 的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。_____
的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。_____
查看答案和解析>>
科目: 来源: 题型:
【题目】研究化学反应中的能量变化有利于更好的开发和使用化学能源。
(1)金属镁[Mg(s)]分别与卤素单质[F2(g)、Cl2(g)、Br2(l)、I2(s)]反应的能量变化如图所示。

①写出Mg(s)和I2(s)反应的热化学方程式:_______。
②反应:MgCl2(s)+F2 (g)=MgF2(s)+Cl2 (g)的ΔH=___________。
(2)CH4用NiO作载氧体的化学链燃烧示意图如图所示。

主要热化学反应如下:2Ni(s)+O2(g)=2NiO(s) ΔH=-479.8 kJ·mol-1;CH4(g)+4NiO(s)=CO2(g)+2H2O(l)+4Ni(s) ΔH=+68.9 kJ·mol-1
①CH4的燃烧热是_______。
②CH4的“化学链燃烧”有利于二氧化碳的分离与回收,所放出的热量在相同条件下与CH4的直接燃烧相比_________(填“前者大”、“后者大”、或“相同”)。
(3)已知H2、CO的燃烧热分别为285.8 kJ·mol-1、283.0 kJ·mol-1,25℃时,4 g H2和28 g CO的混合气体充分燃烧,恢复至原温,能放出的热量为_______kJ。
查看答案和解析>>
科目: 来源: 题型:
【题目】过氧化钠是一种淡黄色固体,能与水反应,常用在呼吸面具和潜水艇里作为氧气的来源,还可用作熔矿剂,使某些不溶于酸的矿物分解。用脱脂棉包住约0.2 g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来。
请回答:(1)由实验现象所得出的有关过氧化钠与水反应的结论是:
a.有氧气生成;b.__________。
(2)某研究性学习小组拟用如图所示装置进行实验,以证明上述结论。
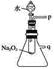
①用以验证结论a的实验方法是:__________;
②用以验证结论b的实验方法是:______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下列实验装置和操作,回答有关问题。
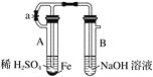
按图中所示装置,用两种不同的操作分别进行实验,观察B容器中的现象。
(1)先夹紧止水夹a,再使A容器中开始反应:①实验中B容器中观察到的现象是_________________;
②B容器中发生反应的离子方程式是____________________________________。
(2)打开止水夹a,使A容器开始反应一段时间后再夹紧止水夹a,①实验中观察到的现象是__________;②B容器中发生反应的离子方程式是________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】粮食仓储常用磷化铝(AlP)熏蒸杀虫,AlP遇水即产生强还原性的PH3气体。国家标准规定粮食中磷化物(以PH3计)的残留量不超过0.05mg·kg-1为合格。某小组同学用如图所示实验装置和原理测定某粮食样品中磷化物的残留量。C中加入100g原粮,E中加入20.00mL 2.50×10-4mol·L-1 KMnO4溶液(H2SO4酸化),向C中加入足量水,充分反应后,用亚硫酸钠标准溶液滴定E中的溶液。
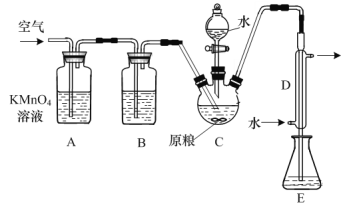
(1)反应后继续通入空气的作用是_______。
(2)装置B中盛装焦性没食子酸的碱性溶液,其作用是吸收空气中的_______(填化学式)。
(3)装置E中PH3被氧化成磷酸,MnO![]() 被还原为Mn2+,则PH3和MnO
被还原为Mn2+,则PH3和MnO![]() 反应的物质的量之比为_______。
反应的物质的量之比为_______。
(4)收集装置E中的吸收液,加水稀释至250mL,移取其中的25.00mL于锥形瓶中,用6.0×10-5mol·L-1的Na2SO3标准溶液滴定,消耗Na2SO3标准溶液20.00 mL,反应原理是:SO![]() +MnO
+MnO![]() +H+= SO
+H+= SO![]() +Mn2++H2O(未配平)。通过计算判断该样品是否合格(写出计算过程)_____。
+Mn2++H2O(未配平)。通过计算判断该样品是否合格(写出计算过程)_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】四氧化三铁俗称为磁性氧化铁,通常用作颜料、抛光剂和电讯器材等。某化学兴趣小组取磁性氧化铁进行铝热反应实验并对产物进行探究。
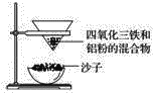
(1)取磁性氧化铁按图装置进行铝热反应,引发铝热反应的实验操作是__________。
(2)取少许反应生成的“铁块”溶于盐酸,滴加硫氰化钾溶液后溶液不变红,则______(填“能”或“不能”)说明“铁块”一定不含四氧化三铁,理由是_________。
(3)设计一个简单的实验方案,证明上述所得的“铁块”中含有金属铝,该实验所用的试剂是__________,反应的离子方程式为___________。
(4)请写出此铝热反应的化学方程式:_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】用![]() 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是
A.![]() 的过氧化氢溶液中氧原子数为
的过氧化氢溶液中氧原子数为![]()
B.通过核反应![]() 生成
生成![]() 镆,同时产生中子数为
镆,同时产生中子数为![]()
C.常温常压下,![]() 由
由![]() 与
与![]() 组成的混合物中含有的质子总数为
组成的混合物中含有的质子总数为![]()
D.![]() 雄黄(
雄黄(![]() ,
,![]() )中含有
)中含有![]() 个共价键
个共价键
查看答案和解析>>
科目: 来源: 题型:
【题目】有一无色溶液,其中可能含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 等离子中的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如下:
等离子中的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如下:

第③个实验中,生成白色沉淀的量与加入![]() 的量有如下图所示的相互关系。据此可知:
的量有如下图所示的相互关系。据此可知:

(1)在原溶液中一定存在的离子有______;一定不存在的离子有______;不能确定是否存在的离子有______。
(2)写出第③个实验中发生反应的离子方程式____________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com