
科目: 来源: 题型:
【题目】下列实验中,现象及结论都正确,且二者之间有因果的是( )
选项 | 实验操作 | 现象 | 结论 |
A | 将少量Na2SO3样品溶于水,滴加足量盐酸酸化的Ba(NO3)2溶液 | 有白色沉淀产生 | Na2SO3已变质 |
B | 将AlCl3溶液加热蒸干 | 得到白色固体 | 成分为纯净的AlCl3 |
C | 蘸有浓氨水的玻璃棒靠近X | 有白烟产生 | X一定是浓盐酸 |
D | 常温下,向等体积、等浓度的NaHCO3和CH3COONa溶液中分别滴加2滴酚酞 | 两份溶液均变红,NaHCO3溶液红色更深 | 常温下的水解平衡常数: |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】二氧化硫是硫的重要化合物,在生产、生活中有广泛应用。二氧化硫有毒,并且是形成酸雨的主要气体。无论是实验室制备还是工业生产,二氧化硫尾气吸收或烟气脱硫都非常重要。
完成下列填空:
(1)实验室可用铜和浓硫酸加热或硫酸和亚硫酸钠反应制取二氧化硫。
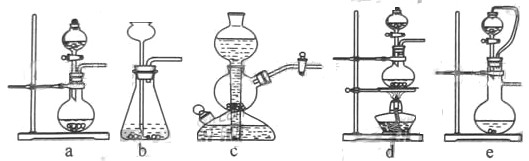
如果用硫酸和亚硫酸钠反应制取二氧化硫,并希望能控制反应速度,上图中可选用的发生装置
是________(填写字母)。
(2)若用硫酸和亚硫酸钠反应制取3,36L(标准状况)二氧化硫,至少需要称取亚硫酸钠______g(保留一位小数);如果已有4.0%亚硫酸钠(质量分数),被氧化成硫酸钠,则至少需称取该亚硫酸钠______g (保留一位小数)。
(3)实验室二氧化硫尾气吸收与工业烟气脱硫的化学原理相通。石灰-石膏法和碱法是常用的烟气脱硫法。
石灰-石膏法的吸收反应为SO2+Ca(OH)2→CaSO3↓+H2O。吸收产物亚硫酸钙由管道输送至氧化塔氧化,反应为2CaSO3+O2+4H2O→2CaSO4·2H2O。其流程如下图:
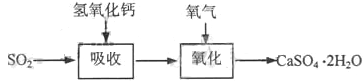
碱法的吸收反应为SO2+2NaOH→Na2SO3+H2O。碱法的特点是氢氧化钠碱性强、吸收快、效率高。其流程如下图:
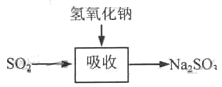
已知:
试剂 | Ca(OH)2 | NaOH |
价格(元/kg) | 0.36 | 2.9 |
吸收SO2的成本(元/mol) | 0.027 | 0.232 |
石灰-石膏法和碱法吸收二氧化硫的化学原理相同之处是____________________。和碱法相比,石灰-石膏法的优点是________________,缺点是________________。
(4)在石灰-石膏法和碱法的基础上,设计一个改进的、能实现物料循环的烟气脱硫方案(用流程图表示)________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】2019年2月27日至3月1日,第十届日本国际二次电池展在日本东京举行,各种新型二次电池在东京有明展览中心展出,其中以![]() 为代表的新型可充电钠离子电池,格外引人注意,其放电工作原理如图所示。下列说法正确的是( )
为代表的新型可充电钠离子电池,格外引人注意,其放电工作原理如图所示。下列说法正确的是( )

A.放电时,正极反应式为:![]()
B.放电时,电子自Mg箔流出,经含Na+的电解质流向Mo箔
C.充电时,Na+通过离子交换膜从右室移向左室
D.充电时,Mo箔接电源的负极
查看答案和解析>>
科目: 来源: 题型:
【题目】运用化学反应原理研究碳、氮等元素的单质及其化合物的反应有重要意义。
(1)如图表示金刚石、石墨在相关反应过程中的能量变化关系。写出石墨转化为金刚石的热化学方程式:____________________。
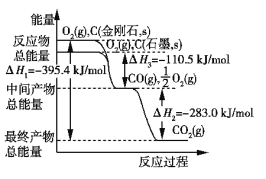
(2)CO与H2可在一定条件下反应生成燃料甲醇:CO(g)+2H2(g)![]() CH3OH(g) ΔH<0。将2 mol CO和4 mol H2置于一体积不变的1 L密闭容器中,测定不同条件、不同时间段内CO的转化率,得到下表数据。
CH3OH(g) ΔH<0。将2 mol CO和4 mol H2置于一体积不变的1 L密闭容器中,测定不同条件、不同时间段内CO的转化率,得到下表数据。

则温度为T1时该反应的平衡常数为____________。a1、a2、80%三者的大小关系为______________。根据温度为T1时的数据作出的下列判断中正确的是__________。
A.反应在2小时的时候混合气体的密度和相对分子质量均比1小时的大
B.反应在3小时的时候,v正(H2)=2v逆(CH3OH)
C.若其他条件不变,再充入6 mol H2,则最多可得到64 g CH3OH
D.其他条件不变,若最初加入的H2为2.4 mol,则达平衡时CO的转化率为50%
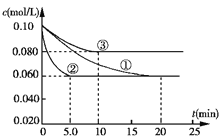
(3)工业中常用以下反应合成氨:N2(g)+3H2(g)![]() 2NH3(g) ΔH<0。在三个不同条件的密闭容器中加入N2和H2进行反应,起始时c(N2)均为0.10 mol/L,c(H2)均为0.30 mol/L,N2的浓度随时间的变化如图①、②、③曲线所示。计算③中产物NH3在0~10 min的平均反应速率:_______;②相对于①条件不同,②的条件是______,理由是___________________。
2NH3(g) ΔH<0。在三个不同条件的密闭容器中加入N2和H2进行反应,起始时c(N2)均为0.10 mol/L,c(H2)均为0.30 mol/L,N2的浓度随时间的变化如图①、②、③曲线所示。计算③中产物NH3在0~10 min的平均反应速率:_______;②相对于①条件不同,②的条件是______,理由是___________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】设![]() 为阿伏加德罗常数的值。下列叙述正确的是( )
为阿伏加德罗常数的值。下列叙述正确的是( )
A.已知![]() ;
;![]() 将2NA个CO与NA个O2混合充分反应放出akJ的热量
将2NA个CO与NA个O2混合充分反应放出akJ的热量
B.t℃时,1LpH=6的纯水中含OHˉ数为10-6NA
C.标准状况下,2.24L甲醇中含有C-H键的数目为0.3NA
D.1L0.1mol/L的氢碘酸中含碘化氢分子数为0.1NA
查看答案和解析>>
科目: 来源: 题型:
【题目】已知浓硫酸和木炭粉在加热条件下反应:C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O,根据如图回答问题:
CO2↑+2SO2↑+2H2O,根据如图回答问题:
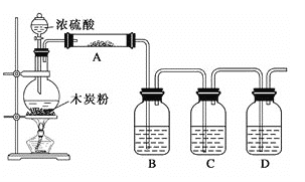
(1)上述装置中,在反应前用手掌紧贴烧瓶外壁检查装置的气密性,如观察不到明显的现象,还可以用什么简单的方法证明该装置不漏气?__。
(2)如果用图中的装置检验上述反应的全部产物,写出下面标号所表示的仪器中应加入的试剂的名称及其作用:
①A中加入的试剂是___,作用是___;
②B中加入的试剂是___,作用是___;
③C中加入的试剂是___,作用是___;
④D中加入的试剂是___,作用是___。
(3)实验时,C中应观察到的现象是___。
查看答案和解析>>
科目: 来源: 题型:
【题目】氮氧化物(用NOx表示)是大气污染的重要因素,根据NOx的来源和性质特点,已开发出多种化学治理其污染的方法。
(1)汽车尾气中的NO2是城市大气污染的主要污染物之一。在日光照射下,NO2发生一系列光化学烟雾的循环反应,从而不断产生O3,加重空气污染。反应过程为①2NO2→2NO+2O,②2NO+O2→2NO2,③O+O2→O3。下列关于该反应过程及生成物的叙述正确的是____(填序号)。
A.NO2起催化作用
B.NO起催化作用
C.NO2只起氧化作用
D.O3与O2互为同素异形体
(2)汽车尾气中的CO来自于____,NO来自于____。
(3)汽车尾气中的CO、NOx可在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出NO被CO还原的化学方程式:_____。
(4)工业尾气中氮氧化物常采用碱液吸收法处理。NO2被烧碱溶液吸收时,生成两种钠盐,其物质的量之比为1∶1,该反应的离子方程式为____;1molNO2被完全吸收时,转移电子的物质的量为____。NO与NO2按物质的量之比1∶1被足量NaOH溶液完全吸收后只得到一种钠盐,该钠盐的化学式为____。
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,在10 L密闭容器中加入5 mol SO2和3 mol O2,发生反应:2SO2(g)+O2(g)![]() 2SO3(g),10 min时,反应达到平衡状态,此时有3 mol SO2发生了反应。
2SO3(g),10 min时,反应达到平衡状态,此时有3 mol SO2发生了反应。
(1)反应生成了________ mol SO3,v(SO2)=________。
(2)平衡时SO3的浓度是________,SO2的转化率是________。
(3)平衡时容器内气体的总物质的量为________mol。
(4)物质的浓度不再改变标志着该反应已达平衡,下列还可以说明该反应已达平衡的是______(填序号)。
①体系内压强不再改变 ②容器内气体的密度不再改变
③混合气体的平均相对分子质量不再改变
④v正(SO3)=2v逆(O2) ⑤n(SO3)∶n(O2)∶n(SO2)=2∶1∶2
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定体积的密闭容器中进行化学反应:CO2(g)+H2(g)![]() CO(g)+H2O(g),其化学平衡常数和温度的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数和温度的关系如下表所示:
t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=____________。
(2)该反应为____________(填“吸热”或“放热”)反应。
(3)某温度下,平衡浓度符合下式c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为____________℃。
(4)在800 ℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)=2 mol·L-1,c(H2)=1.5 mol·L-1,c(CO)=1 mol·L-1,c(H2O)=3 mol·L-1,则下一时刻,反应____________(填“正向”或“逆向”)进行。
查看答案和解析>>
科目: 来源: 题型:
【题目】某兴趣小组探究SO2气体还原Fe3+,他们使用的药品和装置如下图所示,下列说法不合理的是( )
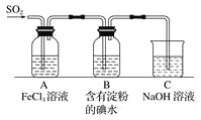
A.能表明I-的还原性弱于SO2的现象是B中蓝色溶液褪色
B.装置C的作用是吸收SO2尾气,防止污染空气
C.为了验证A中发生了氧化还原反应,加入KMnO4溶液,紫红色褪去
D.为了验证A中发生了氧化还原反应,加入用稀盐酸酸化的BaCl2溶液,产生白色沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com