
科目: 来源: 题型:
【题目】A、B、C、D都是中学化学中常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如下(部分反应中的水已略去)。根据题意回答下列问题:
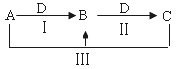
(1)若A、B、C的焰色反应均为黄色,C为厨房中的用品,D的过度排放会造成温室效应。
①A的化学式______________、B的俗名____________;
②反应II的离子方程式是__________________________________。
(2)若A、D均为单质,且A为气体,D元素的一种红棕色氧化物常用作颜料。
①反应II的离子方程式是_____________________________;
②反应Ⅲ的离子方程式是_____________________________;
③检验B中阳离子最好的方法是_____________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】五种短周期元素A、B、C、D、E的原子序数依次增大,A和C同族,B和D同族,C离子和B离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,C和E形成的化合物是日常生活中的常用调味品。回答下列问题:
(1)五种元素中,原子半径最大的是________,非金属性最强的是________(填元素符号)。
(2)由A分别和B、D、E所形成的共价型化合物中,热稳定性最差的是__________(用化学式表示)。
(3)A、B、E形成的离子化合物电子式为____________,其中存在的化学键类型为____________。
(4)D最高价氧化物的水化物的化学式为________________。
(5)单质D在充足的单质E中燃烧,反应的化学方程式为__________________;D在不充足的E中燃烧,生成的主要产物的化学式为__________。
(6)单质E与水反应的离子方程式为____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】NA为阿伏加德罗常数的值,下列说法不正确的是( )
A.标准状况下3.6gH2O含有的电子数为2NA
B.2.8g乙烯与聚乙烯的混合物含有的极性键为0.4NA
C.0.lmolCl2与足量的铁粉充分反应转移的电子数为0.2NA
D.1L0.2mol/l的K2SO3溶液中SO![]() 的数目为0.2NA
的数目为0.2NA
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物X可通过如下方法合成。
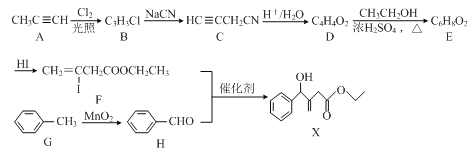
(1)G→H的反应类型为____反应。
(2)B的结构简式为____,E的结构简式为____。
(3)M与E互为同分异构体,且具有完全相同的官能团。M能发生银镜反应,核磁共振氢谱显示三种不同化学环境的氢,其峰面积之比为6∶1∶1。写出一种符合上述条件的M的结构简式____。
(4)请写出以CH3C≡CH、CH3OH为原料制取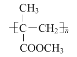 的合成路线示意图(无机试剂任用。合成示例例见本题题干)____。
的合成路线示意图(无机试剂任用。合成示例例见本题题干)____。
查看答案和解析>>
科目: 来源: 题型:
【题目】完成下列小题。
(1)某有机物X含有C、H元素,可能含有O元素。取0.46g X在氧气中完全燃烧,将燃烧后的产物依次通过浓硫酸和碱石灰,测得浓硫酸增重0.54g,碱石灰增重0.88g。由实验分析计算可得X的____(填“实验式”、“分子式”或“结构简式”)为____。
(2)有机物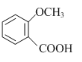 含有多种同分异构体,写出同时满足下列条件的一种同分异构体的结构简式:____。①能发生银镜反应;②与FeCl3发生显色反应;③苯环上的一元取代物只有1种
含有多种同分异构体,写出同时满足下列条件的一种同分异构体的结构简式:____。①能发生银镜反应;②与FeCl3发生显色反应;③苯环上的一元取代物只有1种
(3)化合物D是合成神经保护剂依那朵林的中间体,合成路线如下:
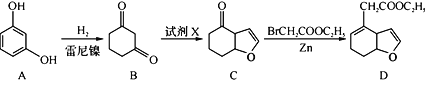
请写出以![]() 和BrCH2COOC2H5为原料制备
和BrCH2COOC2H5为原料制备![]() 的合成路线流程图(无机试剂任用。合成示例例见本题题干)____。
的合成路线流程图(无机试剂任用。合成示例例见本题题干)____。
查看答案和解析>>
科目: 来源: 题型:
【题目】ClO2是一种易溶于水的黄绿色气体,可用作安全高效的水处理剂,某溶液X中所含ClO2浓度(g·L-1)的实验测定步骤如下:步骤1. 配制Na2S2O3溶液:准确称取1.984 0 g Na2S2O3·5H2O,用新煮沸并冷却的蒸馏水配成100.00 mL溶液。步骤2. 准确移取1.00 mL溶液X加入锥形瓶中,加入丙二酸静置后,再加入适量硫酸及稍过量的KI溶液(2ClO2+10I-+8H+===5I2+2Cl-+4H2O),在暗处放置5 min。步骤3. 向步骤2的锥形瓶的反应液中加入1 mL淀粉溶液作指示剂,再向其中滴加步骤1配制的Na2S2O3溶液(发生反应I2+2Na2S2O3===2NaI+Na2S4O6),至恰好完全反应时消耗Na2S2O3溶液25.00 mL。
(1)步骤1中所配Na2S2O3溶液的物质的量浓度为____mol·L-1,所用玻璃仪器除烧杯、胶头滴管外还有____。(2)配制Na2S2O3溶液时,蒸馏水需煮沸的原因是____。
(3)计算溶液X中所含ClO2浓度(g·L-1)(写出计算过程)____。
查看答案和解析>>
科目: 来源: 题型:
【题目】硼是一种奇特的元素,它来自超新星爆发和宇宙射线的散列辐射。
(1)写出BF3电子式___________,B与F形成共价键时,共用电子对偏向_____原子,判断依据是_________________。
(2)硼酸(H3BO3)在水中电离出阴离子[B(OH)4]-,请写出硼酸的电离方程式___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】乙醛是一种重要的烃类衍生物,广泛应用于纺织、医药、化纤、染料和食品工业。
(一)以乙烯和氧气(或空气)为原料,在由PdCl2、CuCl2、盐酸组成的催化剂水溶液中,进行液相氧化生产乙醛,工业上一般控制反应温度在120~130℃,压强在300~350KPa。又称Wacker法。其反应式为:
主反应:CH2═CH2(g) +![]() O2(g)
O2(g) ![]() CH3CHO(g) ΔH=-243.2 kJ·mol-1
CH3CHO(g) ΔH=-243.2 kJ·mol-1
副反应:![]() CH2═CH2(g) +
CH2═CH2(g) + ![]() O2(g)
O2(g) ![]() CO2(g)+H2O(g) ΔH=-705.5kJ·mol-1
CO2(g)+H2O(g) ΔH=-705.5kJ·mol-1
(1)已知:水的汽化热是44.0 kJ·mol-1,请计算乙烯的燃烧热:ΔH =__________ kJ·mol-1
汽化热:在标准大气压(101KPa)下,使1mol物质在一定温度下蒸发所需要的热量。
(2)Wacker法乙烯氧化制乙醛过程,按照以下机理进行:
①乙烯羰基化反应:_____________________________
②金属钯的再氧化反应:Pd + 2CuCl2 = PdCl2 + 2CuCl
③氯化亚铜的氧化反应:2CuCl + ![]() O2 + 2HCl = 2CuCl2 + H2O
O2 + 2HCl = 2CuCl2 + H2O
请写出①的反应方程式__________________________。
(3)下列有关说法正确的是_______________
A.Wacker法制乙醛反应中,氯化钯是反应催化剂,氯化铜的作用是使催化剂再生,没有氯化铜的存在,就不能完成此催化过程。
B.工业上采用的原料气中乙烯大量过量,并有大量未反应的乙烯气要循环使用,这样可提高乙烯利用率,同时原料气中加入CO2有利于提高乙醛选择性。
C.原料气中乙烯大量过量的原因可能是为了让乙烯的体积分数处在爆炸极限范围之外,以避免危险的发生。
D.乙烯氧化生成乙醛的反应是在气-液相中进行的,加压和升温都有利于提高乙烯和氧在液体中的溶解度,加快反应速率。
(4)控制反应条件在120~130℃和300~350KPa,原料气的体积比是V(C2H4):V(O2):V(CO2):V(N2) = 15:10.5:9.5:65,以一定流速通入催化剂水溶液中,一段时间后反应达平衡,测得乙烯的体积分数是0.1,氧气的体积分数是0.05,如果充入100mol原料气,请计算反应达平衡时,n(CH3CHO) =
___________ mol。(不考虑HCl的挥发)
(二)实际工业生产要求有较高产量,速率不能太低,转化率尽可能大,所以应尽量使平衡正向移动。
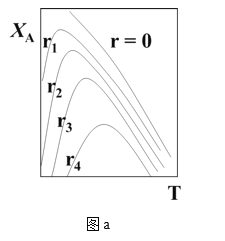
(1)可逆反应:aA+bB![]() rR +s S ,对反应物A,净反应速率为rA = r正(XA) – r逆(XA),XA为反应物A的转化率,图a表示反应物A的转化率和A的净反应速率与温度(T)的关系图。图a分析可知,在相同温度下,净反应速率为________时,XA最大(从“r=0、r1、r2、r3、r4”选填);由图a判断该反应是__________反应(填“吸热”或“放热”),并简述原因__________。
rR +s S ,对反应物A,净反应速率为rA = r正(XA) – r逆(XA),XA为反应物A的转化率,图a表示反应物A的转化率和A的净反应速率与温度(T)的关系图。图a分析可知,在相同温度下,净反应速率为________时,XA最大(从“r=0、r1、r2、r3、r4”选填);由图a判断该反应是__________反应(填“吸热”或“放热”),并简述原因__________。
(2)请在图a中绘制:在不同r下,符合工业生产要求的最佳温度__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】结合氯气的相关知识解决下列问题。
(1)在实验室中制取Cl2,下列收集Cl2的装置中正确的是_______(填字母)。
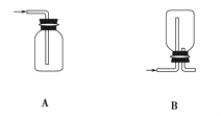

漂白粉能与盐酸发生反应,但盐酸浓度不同时,漂白粉与盐酸混合发生反应的类型不同。
漂白粉与稀盐酸发生复分解反应,化学方程式为_________________________。漂白粉与浓盐酸发生氧化还原反应,化学方程式为____________________________________。
(2)氯水中含有多种成分,因而具有很多性质,根据氯水分别与如图四种物质发生的反应填空(a、b、c、d重合部分代表物质间反应,且氯水足量)。
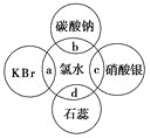
①能证明氯水具有漂白性的是______(填“a”“b”“c”或“d”)。
②c过程中的现象是________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】I.X是一种集洗涤、漂白、杀菌于一体的新型漂白剂(由四种短周期元素组成的纯净物),无毒无味,性能温和,且对环境友好。X从组成形式上可看成是某种正盐M与活性物质N的加合产物(mM·nN ,类似于结晶水合物,相对分子量不超过400)。现将X按如下流程实验,气体A能使带火星的木条复燃,固体B溶于水所得溶液显碱性,且焰色反应呈黄色。

请回答:
(1) X中含有的非金属元素是________,写出X灼烧的化学方程式是_________________。
(2)向X的溶液中通入少量SO2,请写出离子方程式__________________。
II .某化学兴趣小组为了探究硫酸铁溶液与铜粉反应的限度问题,向一定量的硫酸铁溶液中加入过量的铜粉,充分振荡后溶液逐渐变蓝,过滤,向滤液中滴加2滴0.2mol/L KSCN溶液。实验现象为:溶液变为红色,但振荡后红色迅速褪去并有白色沉淀生成。甲同学猜想出现异常现象是由于溶液中的Cu2+干扰了Fe3+的检验,查阅相关资料如下:
①CuSCN是一种白色沉淀物
②硫氰[(SCN)2]:是一种拟卤素,性质与卤素单质相似,其氧化性介于Br2和I2之间。
(1)该兴趣小组所记录的实验现象说明铜与铁离子的反应__________(填有或没有)限度。
(2)请用离子方程式分别解释“溶液变为红色”、“振荡后红色迅速褪去并有白色沉淀生成”现象的原因:___________________________________、_________________________________。
(3)为了进一步探究,该小组向盛有2mL 0.5mol/L FeSO4和0.2mol/L KSCN混合溶液的试管中,滴加5滴0.05mol/L硫酸铜溶液,有白色沉淀生成,且溶液变红。请解释溶液变红的可能原因(可以不止一种):
①____________,②___________,③_________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com